Clear Sky Science · tr
Fe/αKG-bağımlı dekarboksilaz TraH’de kapak döngüsü aracılı proton transferi ortaya kondu
Neden küçük bir hareketli döngü önemli?
Mikropların içinde, özelleşmiş proteinler potansiyel antibiyotikler de dahil olmak üzere karmaşık molekülleri sessizce inşa eder ve yeniden şekillendirir. Bu çalışma, yaygın bir gıda bozucu fungustan gelen TraH adlı böyle bir proteine odaklanıyor. Araştırmacılar, TraH’deki küçük esnek “kapak”ın, enzimin bir molekülden bir parçayı nasıl kopardığını kontrol eden hareketli bir kapı gibi davrandığını ve bazı durumlarda hangi kimyasal dönüşümün gerçekleşeceğini belirlemeye dahi yardımcı olduğunu ortaya koyuyor. Bu hareketli parçayı anlamak, doğanın katalizörlerinin nasıl çalıştığına dair resmimizi derinleştirmenin yanı sıra, bilim insanlarının ilaç ve diğer değerli bileşikleri üretmek için yeni enzimler tasarlamasına yardımcı olabilir.
Molekül yapımında mantar kaynaklı bir yardımcı
TraH, demir ve α‑ketoglutarat adlı yardımcı bir molekülü kullanarak güçlü oksidasyon reaksiyonları gerçekleştiren geniş bir enzim ailesine aittir. Bu enzimler, pigmentler, toksinler ve ilaç benzeri moleküller gibi “ikincil metabolitlerin” inşasında mikropların merkez oyuncularıdır. Penicillium crustosum mantarında TraH, antibakteriyel ve antiviral özellik vaat eden terrestric asidin üretimine yardımcı olur. TraH’nin ana görevi, crustosic asit adı verilen bir öncüden karbondioksit grubunu koparmak ve aynı zamanda moleküle çift bağ kazandırmaktır. İlginç olan, TraH’nin aynı bileşiğin yakın akraba bir metil‑ester versiyonuna da etki edebilmesidir; bu durumda karbondioksit uzaklaşmaz, yalnızca çift bağ oluşur.
Aktif bölgeyi yeniden şekillendiren kapanan kapak
X‑ışını kristalografisi kullanarak yazarlar TraH’nin farklı durumlarına ilişkin yüksek çözünürlüklü anlık görüntüler yakaladılar: boş hali, yalnızca metallle bağlı hali ve metal artı ya crustosic asit ya da onun metil esterine bağlı halleri. Tüm formlar, kimyanın gerçekleştiği demir atomunu tutan çift katmanlı beta‑heliks biçimli sert bir çekirdeğe sahiptir. Bu çekirdeğin etrafı, proteinin uçlarında ekstra segmentlerle sarılıdır; önde yer alan ve kapak gibi davranan bir döngü de bunların arasındadır. Bağlanmamış durumda bu kapak gevşektir ve kristal yapıda kısmen görünmez, bu da dolaştığını gösterir. Gerçek karboksilat substrat bağlandığında kapak aşağı doğru sallanır, iyi düzenlenir ve yakınlardaki helikslerle birlikte aktif bölgeyi mühürleyerek molekülün kapalı bir cebin derinliğine oturmasını sağlar. Metil‑ester substrat söz konusu olduğunda ise kapakta büyük ölçüde düzensiz kalan ve geri çekilmiş parçalar kalır; bu da kapamanın bağlı molekülün doğasına bağlı olduğunu gösterir.
Protonları hareket ettiren su temelli bir röle
Kapatılmış kapaklı crustosic asit yapısının daha yakından incelenmesi, kapağı enzim çekirdeğindeki korunan bir lizin (K191) ile ve substratın karboksil grubuyla bağlayan karmaşık bir hidrojen bağı ağı ortaya çıkardı. Anahtar kapak kalıntıları, K191 ile substratın reaksiyona giren ucu arasında bir veya iki su molekülünü konumlandırmaya yardımcı olur. Bu ağın ne kadar önemli olduğunu test etmek için ekip kapağın ve yakın çekirdeğin bireysel amino asitlerini değiştirdi. Özellikle Q99, D112, K114, K191 ve Y214 konumlarındaki ağ bozucu mutasyonlar dekarboksilasyon reaksiyonunu keskin şekilde azalttı ya da yok etti; komşu, ağ dışında kalan kalıntılardaki değişikliklerin ise çok az etkisi oldu. Buna karşılık, bu bozucu mutasyonların çoğu metil‑ester substrat üzerindeki desaturasyon yeteneğini neredeyse etkilemedi; bu durum su aracılı ağın özellikle karbondioksit kaybı için kritik olduğunu düşündürüyor.
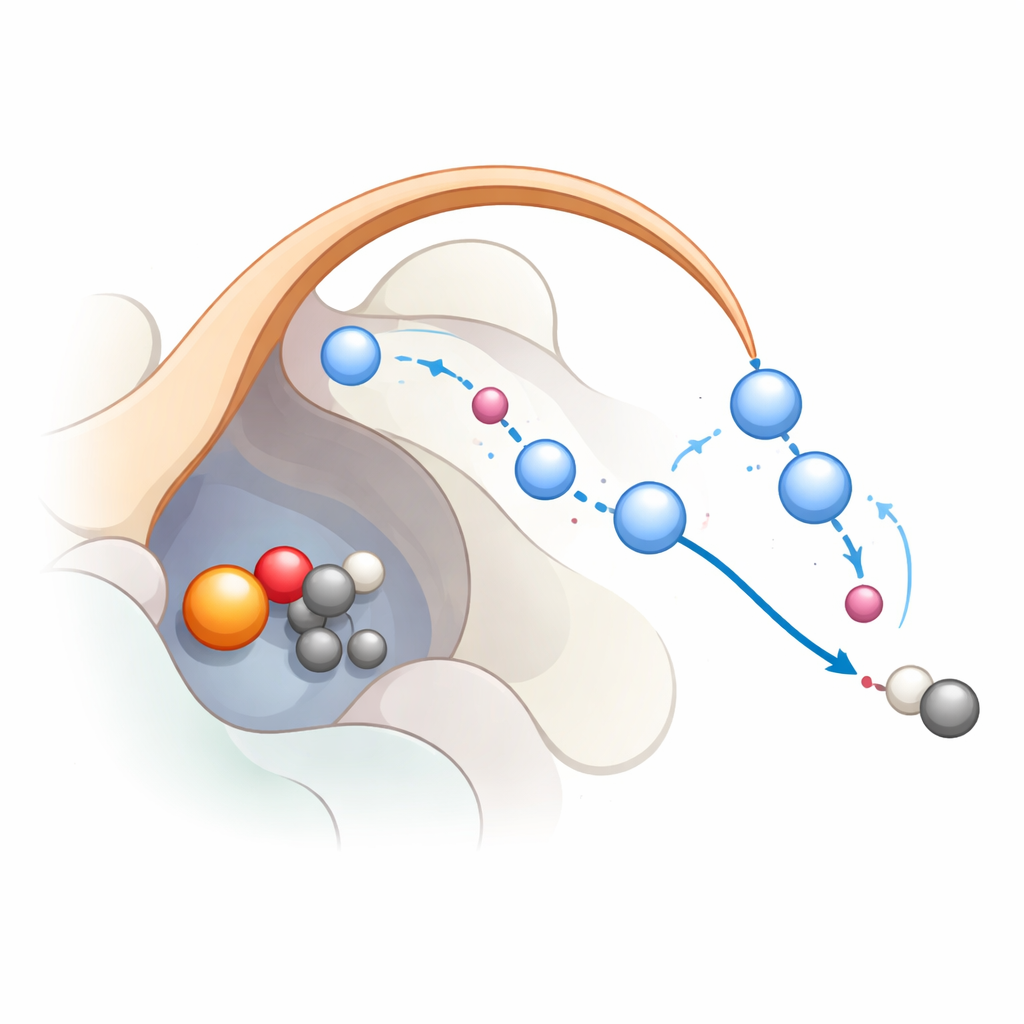
Reaksiyonu adım adım izlemek
Bu ağın reaksiyon sırasında gerçekten nasıl çalıştığını görmek için araştırmacılar klasik moleküler dinamiği daha gelişmiş kuantum‑mekanik simülasyonlarla birleştirdiler. Hesaplamalara, demirin zaten bu enzim ailesinde yaygın bir ara ürün olan yüksek reaktiviteye sahip bir demir‑okso türü oluşturduğu bir durumdan başladılar. Hesaplamalar üç adımlı bir yolu destekliyor: ilk olarak demir‑okso substrattan bir hidrojen atomu çeker ve bir radikal oluşturur; ikinci olarak bir elektron demire geri kayar ve substratın karbondioksiti atmasına yardım eder; üçüncü olarak demire bağlı hidroksil grubu tekrar protonlanır ve demir dinlenme durumuna döner. Simülasyonlar, K191 ve kapak döngüsü tarafından stabilize edilen su zincirinin son adımlarda protonları verimli şekilde taşıyan bir proton rölesi oluşturduğunu gösteriyor. Bu röle kırıldığında reaksiyon enerjik olarak elverişsiz hale geliyor; bu da mutasyon verileriyle güzelce örtüşüyor.
Enzimin evrimini yönlendiren uyarlanabilir bir döngü
TraH’nin ötesinde yazarlar aynı demir‑bağlayıcı çekirdeği paylaşan ancak farklı kimyasal görevleri gören ilişkili enzimleri karşılaştırdılar. Bu enzimlerin birçoğunda da kapak‑benzeri döngüler bulunuyor, ancak bunların uzunlukları, dizileri ve hareket dereceleri büyük ölçüde değişiyor. Bazılarında döngü substratlar üzerinde sıkıca kapanıp önemli hidrojen bağları oluşturuyor; bazılarında ise açık kalıyor ve kimyada yer aldığı görünmüyor. Evrimsel ağaçlar kurup dizi desenlerini analiz ederek ekip, TraH’nin hidrojen bağı ağında yer alan bazı kapak kalıntılarının güçlü şekilde korunduğunu, oysa diğer pozisyonların farklı substrat tercihlerine paralel olarak değiştiğini buldu. Bu, evrimin bu döngülerin hem sertliğini hem de kimyasını yeni molekülleri tanımak ve reaksiyonları belirli sonuçlara yönlendirmek için ayarladığını gösteriyor.
Gelecek kimyası için bunun anlamı
Bir uzman olmayan için merkezi mesaj şudur: Bir enzimin yüzeyindeki küçük esnek bir döngü, içinde protonların ve su moleküllerinin nereden geçeceğini kontrol edebilir ve bu kontrol bir molekülün yalnızca bir hidrojen kaybedip kaybetmeyeceğini ya da aynı zamanda karbondioksit kaybedip kaybetmeyeceğini belirleyebilir. TraH’de kapağın görevi sadece aktif bölgeyi kapatmak değil, amino asitler ve hapsedilmiş sulardan oluşan küçük bir proton‑transfer makinesini bir araya getirmektir. Bu döngü aracılı strateji, ayrılan gruba bitişik sabit bir bazik kalıntı kullanan birçok ilişkili enzimin yönteminden farklıdır. Bu alternatif tasarımı ortaya koyarak çalışma, doğanın çok yönlü katalizörler inşa etme biçimine dair anlayışımızı genişletiyor ve hareketli parçaları yeniden kablolayarak yeni reaksiyonlar ve yeni biyoaktif moleküller üretilebilecek enzimlerin tasarımına dair bir şablon sunuyor.
Atıf: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
Anahtar kelimeler: enzim mekanizmaları, heme dışı demir enzimleri, proton transferi, fungal ikincil metabolizma, enzim evrimi