Clear Sky Science · fr
Transfert de protons médié par une boucle de couvercle révélé dans la décarboxylase TraH dépendante du Fe/αKG
Pourquoi une petite boucle mobile a de l’importance
À l’intérieur des microbes, des protéines spécialisées construisent et remodèlent silencieusement des molécules complexes, y compris des candidats antibiotiques. Cette étude s’intéresse à l’une de ces protéines, nommée TraH, issue d’un champignon courant responsable de la détérioration des aliments. Les chercheurs montrent qu’un petit « couvercle » flexible dans TraH agit comme une porte mobile contrôlant la manière dont l’enzyme élimine un fragment d’une molécule et, dans certains cas, contribue à déterminer quel type de transformation chimique se produit. Comprendre cette pièce mobile approfondit non seulement notre vision du fonctionnement des catalyseurs naturels, mais pourrait aussi aider les scientifiques à concevoir de nouvelles enzymes pour fabriquer des médicaments et d’autres composés de valeur.
Un assistant fongique dans la synthèse moléculaire
TraH appartient à une vaste famille d’enzymes qui utilisent le fer et une molécule auxiliaire, l’α‑cétoglutarate, pour réaliser de puissantes réactions d’oxydation. Ces enzymes jouent un rôle central dans la chimie microbienne, où elles contribuent à la production de « métabolites secondaires » tels que pigments, toxines et molécules à activité pharmaceutique. Chez le champignon Penicillium crustosum, TraH participe à la biosynthèse de l’acide terrestrique, un composé présentant des propriétés antibactériennes et antivirales prometteuses. La fonction principale de TraH est de cliver un groupe carboxyle sous forme de dioxyde de carbone à partir d’un précurseur appelé acide crustosique, tout en introduisant simultanément une double liaison dans la molécule. Fait intriguant, TraH peut aussi agir sur une version étroitement liée du même composé portant un méthyl‑ester : dans ce cas, il se contente d’introduire la double liaison sans éliminer le dioxyde de carbone.
Un couvercle qui se referme et reconfigure le site actif
Grâce à la cristallographie aux rayons X, les auteurs ont capturé des clichés à haute résolution de TraH dans différents états : vide, lié au métal seul, et lié au métal avec soit l’acide crustosique soit son méthyl‑ester. Toutes les formes partagent un noyau rigide en forme d’hélice bêta à double couche, qui maintient l’atome de fer où la chimie se déroule. Enveloppant ce noyau se trouvent des segments supplémentaires aux extrémités de la protéine, dont une boucle à l’avant qui se comporte comme un couvercle. À l’état libre, ce couvercle est lâche et partiellement indétectable dans la structure cristalline, ce qui indique qu’il fluctue. Quand le vrai substrat carboxylate se lie, le couvercle bascule, devient ordonné et, avec des hélices voisines, scelle le site actif de sorte que la molécule s’installe profondément dans une poche fermée. Pour le substrat méthyl‑ester, en revanche, une grande partie du couvercle reste désordonnée et reculée, montrant que sa fermeture précise dépend de la nature de la molécule liée.
Une chaîne à base d’eau pour déplacer les protons
Une inspection plus fine de la structure à couvercle fermé avec l’acide crustosique a révélé un réseau complexe de liaisons hydrogène reliant le couvercle à une lysine conservée (K191) dans le cœur de l’enzyme et au groupe carboxyle du substrat. Des résidus clés du couvercle aident à positionner une ou deux molécules d’eau entre K191 et l’extrémité réactive du substrat. Pour tester l’importance de ce réseau, l’équipe a modifié des acides aminés individuels dans le couvercle et le cœur proche. Les mutations perturbant le réseau, en particulier aux positions Q99, D112, K114, K191 et Y214, ont fortement réduit ou supprimé la décarboxylation, tandis que des modifications de résidus voisins hors du réseau avaient peu d’effet. En revanche, la plupart de ces mutations perturbatrices ont à peine altéré la capacité de l’enzyme à réaliser la désaturation sur le substrat méthyl‑ester, ce qui suggère que le réseau médié par l’eau est spécifiquement crucial pour la perte de dioxyde de carbone.
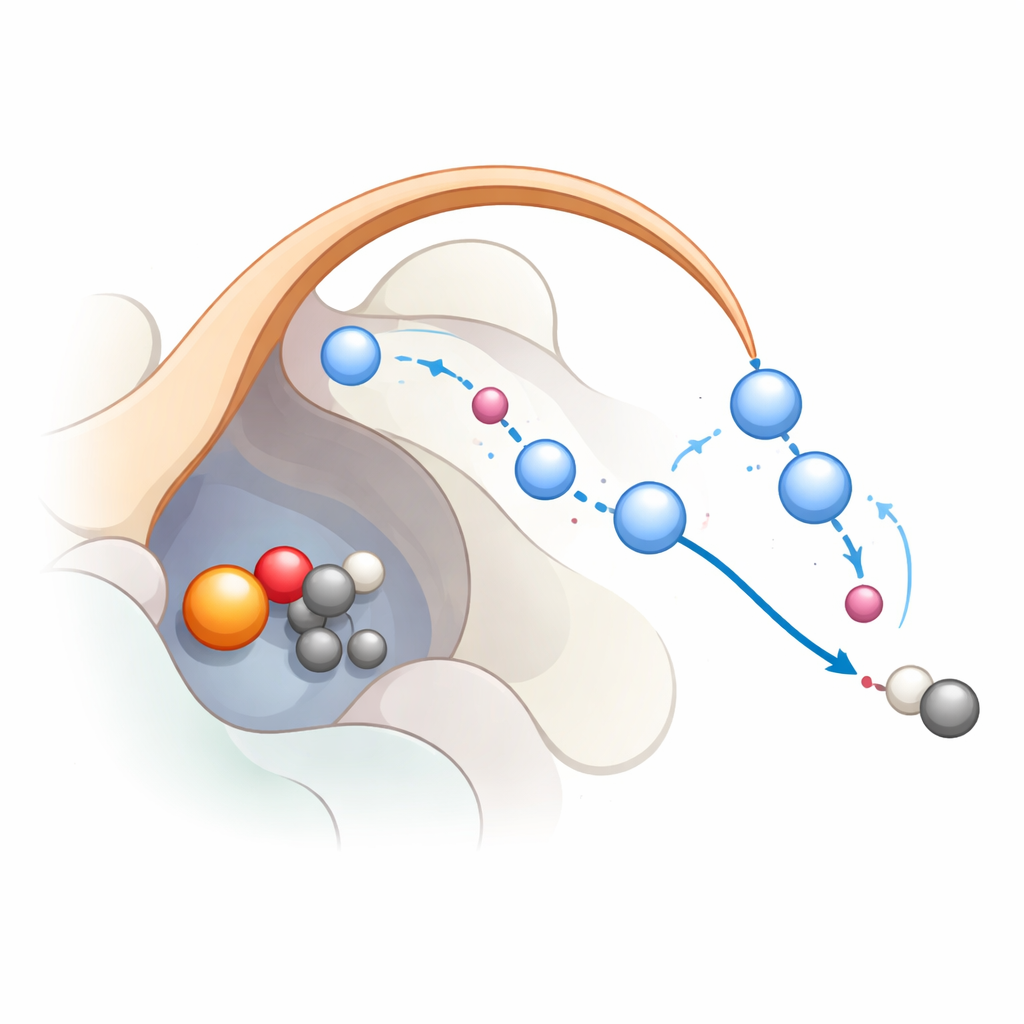
Suivre la réaction étape par étape
Pour comprendre comment ce réseau fonctionne réellement pendant la réaction, les chercheurs ont combiné dynamique moléculaire classique et simulations plus avancées de mécanique quantique. Ils sont partis d’un état où le fer a déjà formé une espèce fer‑oxo hautement réactive, un intermédiaire courant dans cette famille d’enzymes. Les calculs soutiennent une voie en trois étapes : d’abord, le fer‑oxo arrache un atome d’hydrogène au substrat, créant un radical ; ensuite, un électron retourne vers le fer, aidant le substrat à perdre le dioxyde de carbone ; enfin, le groupe hydroxyle lié au fer est reprotoné pour que le fer retrouve son état de repos. Les simulations montrent que K191 et la chaîne de molécules d’eau stabilisée par la boucle‑couvercle forment une relayeur de protons qui transporte efficacement les protons durant les dernières étapes. Lorsque ce relais est rompu, la réaction devient énergétiquement défavorable, en accord avec les données de mutation.
Une boucle adaptable qui oriente l’évolution des enzymes
Au‑delà de TraH lui‑même, les auteurs ont comparé des enzymes apparentées qui partagent le même noyau de liaison au fer mais accomplissent des tâches chimiques différentes. Bon nombre de ces enzymes possèdent aussi des boucles de type couvercle, mais leurs longueurs, séquences et mobilités varient largement. Chez certaines, la boucle se referme fermement sur les substrats et forme des liaisons hydrogène clés ; chez d’autres, elle reste ouverte et ne semble pas participer à la chimie. En construisant des arbres évolutifs et en analysant les motifs de séquence, l’équipe a trouvé que certains résidus de la boucle impliqués dans le réseau de liaisons hydrogène de TraH sont fortement conservés, tandis que d’autres positions varient d’une manière corrélée aux préférences de substrat. Cela suggère que l’évolution règle à la fois la rigidité et la chimie de ces boucles pour reconnaître de nouvelles molécules et orienter les réactions vers des issues particulières.
Ce que cela signifie pour la chimie future
Pour un non‑spécialiste, le message central est qu’une petite boucle flexible à la surface d’une enzyme peut contrôler où les protons et les molécules d’eau se déplacent à l’intérieur, et que ce contrôle peut déterminer si une molécule perd simplement un hydrogène ou perd aussi du dioxyde de carbone. Dans TraH, la fonction du couvercle n’est pas seulement de refermer le site actif mais d’assembler une minuscule machine de transfert de protons à partir d’acides aminés et d’eaux piégées. Cette stratégie médiée par une boucle diffère de celle de nombreuses enzymes apparentées, qui utilisent un résidu basique fixe placé juste à côté du groupe partant. En révélant ce design alternatif, le travail élargit notre compréhension de la manière dont la nature construit des catalyseurs polyvalents et offre un plan pour l’ingénierie d’enzymes dont les parties mobiles peuvent être reconfigurées pour réaliser de nouvelles réactions et permettre la fabrication de nouvelles molécules bioactives.
Citation: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
Mots-clés: mécanismes enzymatiques, enzymes non‑hémées à fer, transfert de protons, métabolisme secondaire fongique, évolution des enzymes