Clear Sky Science · de
Schleifenvermittelte Protonenübertragung im Fe/αKG‑abhängigen Decarboxylase TraH enthüllt
Warum eine winzige bewegliche Schleife wichtig ist
In Mikroben bauen spezialisierte Proteine leise komplexe Moleküle auf und verändern sie — darunter auch potenzielle Antibiotika. Diese Studie richtet den Blick auf ein solches Protein, TraH, aus einem häufigen lebensmittelverderbenden Pilz. Die Forschenden zeigen, dass eine kleine flexible „Klappe“ in TraH wie ein bewegliches Tor wirkt, das steuert, wie das Enzym einen Teil eines Moleküls entfernt und in manchen Fällen sogar bestimmt, welche chemische Veränderung insgesamt stattfindet. Das Verständnis dieses beweglichen Teils vertieft nicht nur unser Bild davon, wie natürliche Katalysatoren arbeiten, sondern könnte auch dabei helfen, neue Enzyme für die Herstellung von Medikamenten und anderen wertvollen Verbindungen zu entwerfen.
Ein pilzlicher Helfer bei der Molekülherstellung
TraH gehört zu einer großen Enzymfamilie, die Eisen und einen Helferstoff namens α‑Ketoglutarat nutzt, um starke Oxidationsreaktionen durchzuführen. Diese Enzyme sind zentrale Akteure der mikrobiellen Chemie und helfen beim Aufbau von Sekundärmetaboliten wie Pigmenten, Toxinen und wirkstoffähnlichen Molekülen. Im Pilz Penicillium crustosum trägt TraH zur Produktion von terrestrischer Säure bei, einer Verbindung mit vielversprechenden antibakteriellen und antiviralen Eigenschaften. Die Hauptaufgabe von TraH besteht darin, eine Kohlendioxidgruppe von einem Vorläufer, der crustosischen Säure, abzuschneiden und gleichzeitig eine Doppelbindung in das Molekül einzuführen. Interessanterweise kann TraH auch an einer eng verwandten Methylester‑Variante desselben Verbindungen arbeiten, wobei in diesem Fall nur eine Doppelbindung eingeführt wird, ohne Kohlendioxid zu entfernen.
Eine schließende Klappe, die das aktive Zentrum umformt
Mithilfe von Röntgenkristallographie hielten die Autoren hochauflösende Schnappschüsse von TraH in verschiedenen Zuständen fest: unbesetzt, nur mit Metall gebunden sowie mit Metall und entweder crustosischer Säure oder ihrem Methylester. Alle Formen teilen einen starren Kern in Form einer doppellagigen Beta‑Helix, der das Eisenatom an der Reaktionsstelle trägt. Um diesen Kern sind zusätzliche Segmente an den Proteinenden gewickelt, darunter eine Schleife vorn, die sich wie eine Klappe verhält. Im ungebundenen Zustand ist diese Klappe flexibel und im Kristall teilweise unsichtbar, was darauf hindeutet, dass sie umherwandert. Bindet das echte Carboxylat‑Substrat, schwingt die Klappe herunter, wird gut geordnet und verschließt zusammen mit benachbarten Helices das aktive Zentrum, sodass das Molekül tief in einer geschlossenen Tasche liegt. Beim Methylester‑Substrat bleibt hingegen ein großer Teil der Klappe ungeordnet und zurückgezogen, was zeigt, dass ihr genaues Schließen von der Natur des gebundenen Moleküls abhängt.
Ein wasserbasierter Staffelmechanismus zum Verschieben von Protonen
Eine genauere Betrachtung der geschlossenen‑Klappe‑Struktur mit crustosischer Säure zeigte ein komplexes Netzwerk von Wasserstoffbrücken, das die Klappe mit einem konservierten Lysin (K191) im Enzymkern und mit der Carboxylgruppe des Substrats verbindet. Schlüsselreste der Klappe positionieren ein oder zwei Wassermoleküle zwischen K191 und dem reaktiven Ende des Substrats. Um die Bedeutung dieses Netzwerks zu prüfen, veränderte das Team einzelne Aminosäuren in der Klappe und im nahen Kern. Mutationen, die das Netzwerk störten — besonders an den Positionen Q99, D112, K114, K191 und Y214 — verminderten oder eliminierten die Decarboxylierungsreaktion deutlich, während Veränderungen in benachbarten, nicht‑netzwerkbildenden Resten wenig Einfluss hatten. Im Gegensatz dazu beeinträchtigten die meisten dieser störenden Mutationen kaum die Fähigkeit des Enzyms, die Desaturierung am Methylester‑Substrat durchzuführen, was darauf hindeutet, dass das wasservermittelte Netzwerk speziell für den Kohlendioxidverlust entscheidend ist.
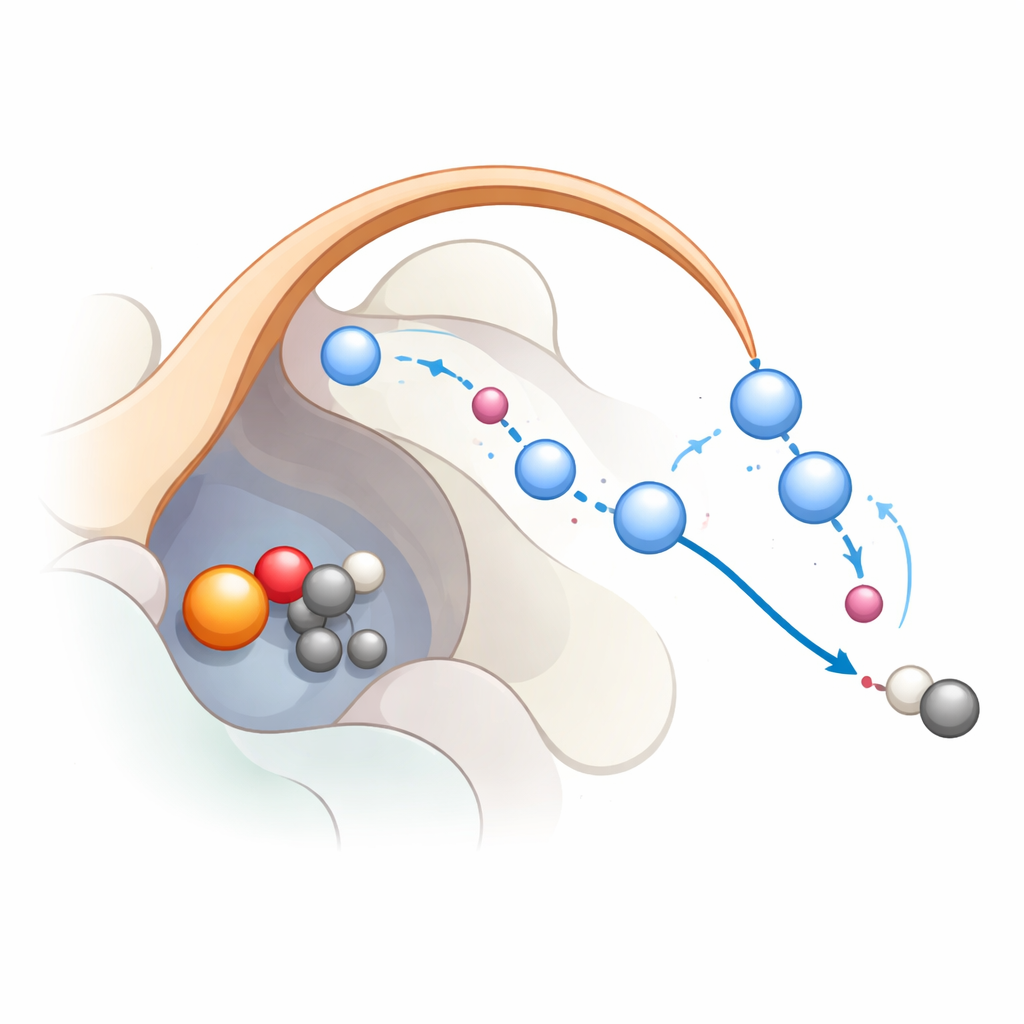
Die Reaktion Schritt für Schritt verfolgen
Um zu sehen, wie dieses Netzwerk während der Reaktion tatsächlich funktioniert, kombinierten die Forschenden klassische Molekulardynamik mit fortgeschritteneren quantenmechanischen Simulationen. Sie begannen von einem Zustand, in dem das Eisen bereits eine hochreaktive Eisen‑oxo‑Spezies gebildet hatte, ein häufiges Zwischenprodukt in dieser Enzymfamilie. Die Berechnungen stützen einen dreistufigen Weg: Zuerst zieht das Eisen‑oxo ein Wasserstoffatom vom Substrat ab und erzeugt ein Radikal; zweitens verschiebt sich ein Elektron zurück zum Eisen und unterstützt so das Abspalten von Kohlendioxid; drittens wird die am Eisen gebundene Hydroxylgruppe reprotoniert, sodass das Eisen in seinen Ruhezustand zurückkehrt. Die Simulationen zeigen, dass K191 und die durch die Klappenschleife stabilisierte Kette von Wassermolekülen einen Protonenrelay bilden, der Protonen in den letzten Schritten effizient shuttlelt. Wird dieses Relay unterbrochen, wird die Reaktion energetisch ungünstig — ein Befund, der gut mit den Mutationsdaten übereinstimmt.
Eine anpassungsfähige Schleife, die die Enzymentwicklung lenkt
Über TraH hinaus verglichen die Autoren verwandte Enzyme, die denselben eisenbindenden Kern teilen, aber unterschiedliche chemische Aufgaben übernehmen. Viele dieser Enzyme besitzen ebenfalls klappenartige Schleifen, deren Längen, Sequenzen und Bewegungsgrade jedoch stark variieren. Bei einigen schließt die Schleife fest über den Substraten und bildet wichtige Wasserstoffbrücken; bei anderen bleibt sie offen und scheint nicht an der Chemie beteiligt zu sein. Durch den Aufbau von Stammbaumanalysen und die Untersuchung von Sequenzmustern fanden die Forschenden, dass bestimmte in TraH am Wasserstoffbrückennetz beteiligte Klappenreste stark konserviert sind, während andere Positionen so variieren, dass dies mit unterschiedlichen Substratpräferenzen korreliert. Das deutet darauf hin, dass die Evolution sowohl die Starrheit als auch die chemische Ausstattung dieser Schleifen abstimmt, um neue Moleküle zu erkennen und Reaktionen in bestimmte Richtungen zu lenken.
Was das für künftige Chemie bedeutet
Für Nicht‑Spezialisten ist die zentrale Botschaft, dass eine kleine flexible Schleife an der Oberfläche eines Enzyms kontrollieren kann, wo Protonen und Wassermoleküle im Inneren wandern, und dass diese Kontrolle darüber entscheiden kann, ob ein Molekül nur ein Wasserstoffatom verliert oder zusätzlich Kohlendioxid. Bei TraH besteht die Aufgabe der Klappe nicht nur darin, das aktive Zentrum zu schließen, sondern eine winzige Protonenübertragungsmaschine aus Aminosäuren und eingeschlossenen Wassermolekülen zusammenzusetzen. Diese schleifenvermittelte Strategie unterscheidet sich von vielen verwandten Enzymen, die eine feststehende basische Aminosäure direkt neben der abgehenden Gruppe verwenden. Indem diese alternative Entwurfsweise aufgezeigt wird, erweitert die Arbeit unser Verständnis dafür, wie die Natur vielseitige Katalysatoren baut, und liefert eine Blaupause dafür, Enzyme so zu konstruieren, dass sich bewegliche Teile umverdrahten lassen, um neue Reaktionen und neue bioaktive Moleküle möglich zu machen.
Zitation: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
Schlüsselwörter: Enzymmechanismen, nicht‑heme Eisen‑Enzyme, Protonentransfer, pilzlicher Sekundärstoffwechsel, Enzymentwicklung