Clear Sky Science · ja
Fe/αKG依存性脱炭酸酵素TraHにおける蓋ループ媒介のプロトン移動の解明
なぜ小さな可動ループが重要なのか
微生物の内部では、特殊化したタンパク質が静かに複雑な分子を合成・再構築しており、その中には抗生物質候補も含まれます。本研究は、一般的な食品腐敗性真菌由来のタンパク質TraHに焦点を当てています。研究者たちは、TraHの小さな柔軟な「蓋」が可動ゲートのように働き、酵素が分子から部分を取り除く過程を制御し、場合によってはどのような化学変化が起こるかを決めることさえあることを明らかにしました。この可動部位の理解は、自然の触媒の働き方を深めるだけでなく、医薬品や他の有用化合物を作るための新しい酵素設計にも役立つ可能性があります。
分子合成を助ける真菌の酵素
TraHは鉄と補助分子であるα‑ケトグルタル酸を利用して強力な酸化反応を行う大きな酵素ファミリーに属します。これらの酵素は色素、毒素、医薬様分子などの「二次代謝産物」を構築する微生物化学の中心的な役割を担います。真菌Penicillium crustosumでは、TraHは抗菌・抗ウイルス性が期待される化合物であるterrestric acidの生合成に関与します。TraHの主な役割は、前駆体であるcrustosic acidから二酸化炭素を切り離す一方で、分子に二重結合を導入することです。興味深いことに、TraHは同じ化合物の近縁体であるメチルエステル型にも作用しますが、その場合は二酸化炭素を取り除かずに単に脱水素(脱飽和)を引き起こします。
活性部位を再構成する閉じる蓋
X線結晶構造解析により、著者らはTraHの高分解能スナップショットを複数の状態で捉えました:未結合、金属のみ結合、金属とcrustosic acidまたはそのメチルエステルのどちらかが結合した状態です。すべての形は二重層のβヘリックスのような剛直なコアを共有し、化学反応が起こる鉄原子を保持しています。このコアの周囲には端部に追加の領域が巻き付いており、前方に近いループが蓋のように振る舞います。未結合状態ではこの蓋は柔らかく結晶構造で部分的に見えないことがあり、自由に動いていることを示しています。本来のカルボキシレート基をもつ基質が結合すると、蓋は下に振り下ろされ、秩序だった状態になり、近くのヘリックスと共に活性部位を密閉して分子が閉じたポケットの深部に納まります。一方でメチルエステル基をもつ基質では、蓋の大部分が無秩序のまま引き戻され、蓋の正確な閉鎖は結合した分子の性質に依存することが示されました。
プロトンを運ぶ水分子の中継
crustosic acid結合時の閉じた蓋の構造を詳しく見ると、蓋が酵素コアの保存されたリジン(K191)および基質のカルボキシル基に連なる精緻な水素結合ネットワークが観察されました。蓋の重要な残基は、K191と反応する基質末端の間に一つまたは二つの水分子を配置するのを助けます。このネットワークの重要性を検証するため、研究チームは蓋や近接するコアの個々のアミノ酸を改変しました。Q99、D112、K114、K191、Y214の位置でネットワークを乱す変異は、脱炭酸反応を著しく低下させるか消失させましたが、隣接するネットワーク外の残基の変化はほとんど影響しませんでした。対照的に、これらの破壊的変異の多くはメチルエステル基に対する脱飽和作用にはほとんど影響を与えず、水を介したネットワークが特に二酸化炭素の喪失にとって重要であることを示唆します。
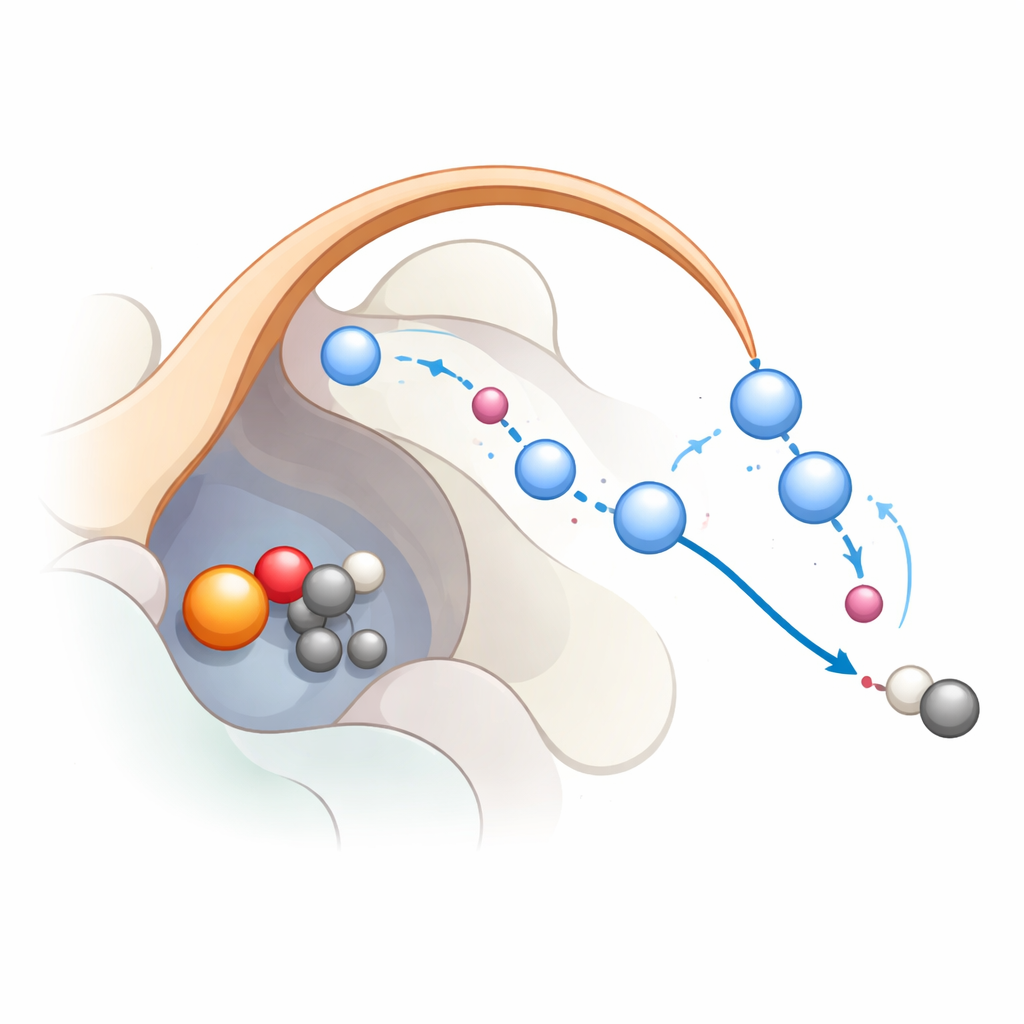
反応を段階的に追う
このネットワークが反応中に実際にどのように機能するかを確かめるため、研究者たちは古典的分子動力学とより進んだ量子力学的シミュレーションを組み合わせました。彼らは鉄がすでに高反応性の鉄オキソ種を形成している状態から計算を開始しました。計算は三段階の経路を支持します:まず、鉄オキソが基質から水素原子を引き抜きラジカルを作る;次に、電子が鉄に戻り基質が二酸化炭素を放出するのを助ける;最後に、鉄に結合したヒドロキシル基が再プロトン化されて鉄が休止状態に戻る。シミュレーションは、K191と蓋ループによって安定化された水分子の連鎖がプロトン中継を形成し、後半の段階で効率的にプロトンを運ぶことを示しました。この中継が壊れると反応はエネルギー的に不利になり、変異実験のデータとよく一致します。
酵素進化を導く適応的なループ
TraH自身にとどまらず、著者らは同じ鉄結合コアを共有しながら異なる化学反応を行う関連酵素と比較しました。これらの多くも蓋様のループを持ちますが、その長さ、配列、運動の度合いは大きく異なります。あるものではループが基質の上にしっかりと閉じて重要な水素結合を形成し、他では開いたままで化学に参加していないように見えます。系統樹を構築し配列パターンを解析することで、TraHの水素結合ネットワークに関与する特定の蓋残基は強く保存されている一方で、他の位置は基質嗜好の違いに沿って変化していることがわかりました。これは進化がこれらのループの剛性と化学的性質の両方を調整して、新しい分子を認識し特定の反応へ偏らせていることを示唆します。
今後の化学にとっての意味
非専門家にとっての中心的なメッセージは、酵素表面の小さな柔軟なループが内部でプロトンや水分子がどこを通るかを制御でき、その制御が分子が単に水素を失うか、あるいは二酸化炭素も失うかを決定しうる、ということです。TraHでは、蓋の役割は単に活性部位を閉じることにとどまらず、アミノ酸と閉じ込められた水からなる小さなプロトン転移装置を組み立てることにあります。このループ媒介戦略は、出て行く基に隣接して固定された塩基性残基を用いる多くの関連酵素の戦略とは異なります。この代替設計を明らかにすることで、自然がいかに多用途な触媒を構築するかについての理解が広がり、可動部位を再配線して新しい反応や新しい生理活性分子を作る酵素工学の設計図を提供します。
引用: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
キーワード: 酵素機構, 非ヘム鉄酵素, プロトン移動, 真菌の二次代謝, 酵素の進化