Clear Sky Science · he
העברה פרוטונית מוּתוּכֶת לולאת מכסה נחשפת בדקארבוקסילאז TraH התלוי ב‑Fe/αKG
מדוע לולאה קטנטנה זזה חשובה
בתוך מיקרואורגניזמים, חלבונים מיוחדים בונים ושונאים בשקט מולקולות מורכבות, כולל כאלו שעשויות לשמש כתרופות אנטיביוטיות. המחקר הזה מתמקד בחלבון כזה, הנקרא TraH, ממין פטרייה נפוץ שמקלקל מזון. החוקרים מגלים שלולאה גמישה קטנה — מעין "מכסה" — ב‑TraH פועלת כשער נייד שמווסת כיצד האנזים מסיר חלק ממולקולה ובמקרים מסוימים גם קובע איזו שינוי כימי יתרחש בסופו של דבר. הבנת החלק הנע הזה לא רק מעמיקה את תמונתנו על אופן הפעולה של זרזי טבע, אלא עשויה גם לסייע למדענים לעצב אנזימים חדשים לייצור תרופות וחומרים יקרי ערך אחרים.
עוזרת פטרייתית ביצירת מולקולות
TraH שייך למשפחה גדולה של אנזימים המשתמשים בברזל ובמולקולת סיוע שנקראת α‑קטוגלוטרט כדי לבצע ריאקציות חמצון עזות. אנזימים אלה הם שחקנים מרכזיים בכימיה המיקרוביאלית, שבה הם תורמים לבניין של "מטבוליטים משניים" כגון פיגמנטים, רעלנים ומולקולות דמויות‑תרופות. בפטריית Penicillium crustosum, TraH מסייע בייצור חומצת terrestric, תרכובת עם תכונות אנטיבקטריאליות ואנטיוויראליות מבטיחות. תפקידו העיקרי של TraH הוא לחתוך קבוצת פחמן‑דו‑חמצני מקדימה הנקראת crustosic acid, ובעת ובעונה אחת להחדיר קשר כפול למולקולה. באופן מרתק, TraH יכול לפעול גם על גרסה קשורה של המולקולה שבה נמצא מתיל‑אסטר, אבל במקרה הזה הוא פשוט יוצר את הקשר הכפול מבלי להסיר את הפחמן‑דו‑חמצני.
מכסה שנועל ומשנה את האתר הפעיל
באמצעות קריסטלוגרפיית קרני X, המחברים תפסו תמונות ברזולוציה גבוהה של TraH במצבים שונים: ריק, קשור למתכת בלבד, וקשור למתכת בתוספת או לחומצת crustosic או לגרסת המתיל‑אסטר שלה. בכל הצורות יש ליבת חלבון קשיחה בצורת סליל‑בטא כפול‑שכבה, שמחזיקה את אטום הברזל שבו מתרחשת הכימיה. סביב ליבה זו עטופים מקטעים נוספים בקצות החלבון, כולל לולאה מקדימה המתנהגת כמכסה. במצב בלתי קשור המכסה רפוי וחלקו בלתי נראה במבנה הגבישי, מה שמעיד על נדידה. כאשר הסובסטרט הקרבוקסילאטי האמיתי נקשר, המכסה ננעל כלפי מטה, מסודר היטב, וביחד עם ההליקסים הסמוכים סוגר את האתר הפעיל כך שהמולקולה יושבת עמוק בתוך כיס סגור. בעניינה של תת־יחידת המתיל‑אסטר, לעומת זאת, רוב המכסה נשאר בלתי מסודר ונמשך לאחור, מה שמראה שנסגירה מדויקת תלויה בטיב המולקולה הקשורה.
שרשרת מבוססת מים להעברת פרוטונים
בדיקה צמודה של המבנה עם המכסה הסגור ועם crustosic acid חשפה רשת מסועפת של קשרי מימן שמקשרים את המכסה לליזין משמר (K191) בליבת האנזים ולקבוצת הקרבוקסיל של הסובסטרט. חומצות אמינו מפתח במכסה מסייעות למקם מולקולת מים אחת או שתי מולקולות בין K191 לבין קצה המגיב של הסובסטרט. כדי לבדוק עד כמה רשת זו חשובה, הצוות החליף חומצות אמינו בודדות במכסה ובליבה הסמוכה. מוטציות שהפריעו לרשת, במיוחד במיקומים Q99, D112, K114, K191 ו‑Y214, הקטינו באופן חד או ביטלו את תגובת הדקארבוקסילציה, בעוד ששינויים באמינו‑חומצות סמוכות שאינן חלק מהרשת השפיעו מעט בלבד. לעומת זאת, רוב המוטציות המשבשות הללו כמעט ולא השפיעו על יכולת האנזים לבצע דיסאטרציה על תת‑היחידה המתיל‑אסטרית, מה שמרמז שרשת התיווך המימית חשובה במיוחד לאובדן פחמן‑דו‑חמצני.
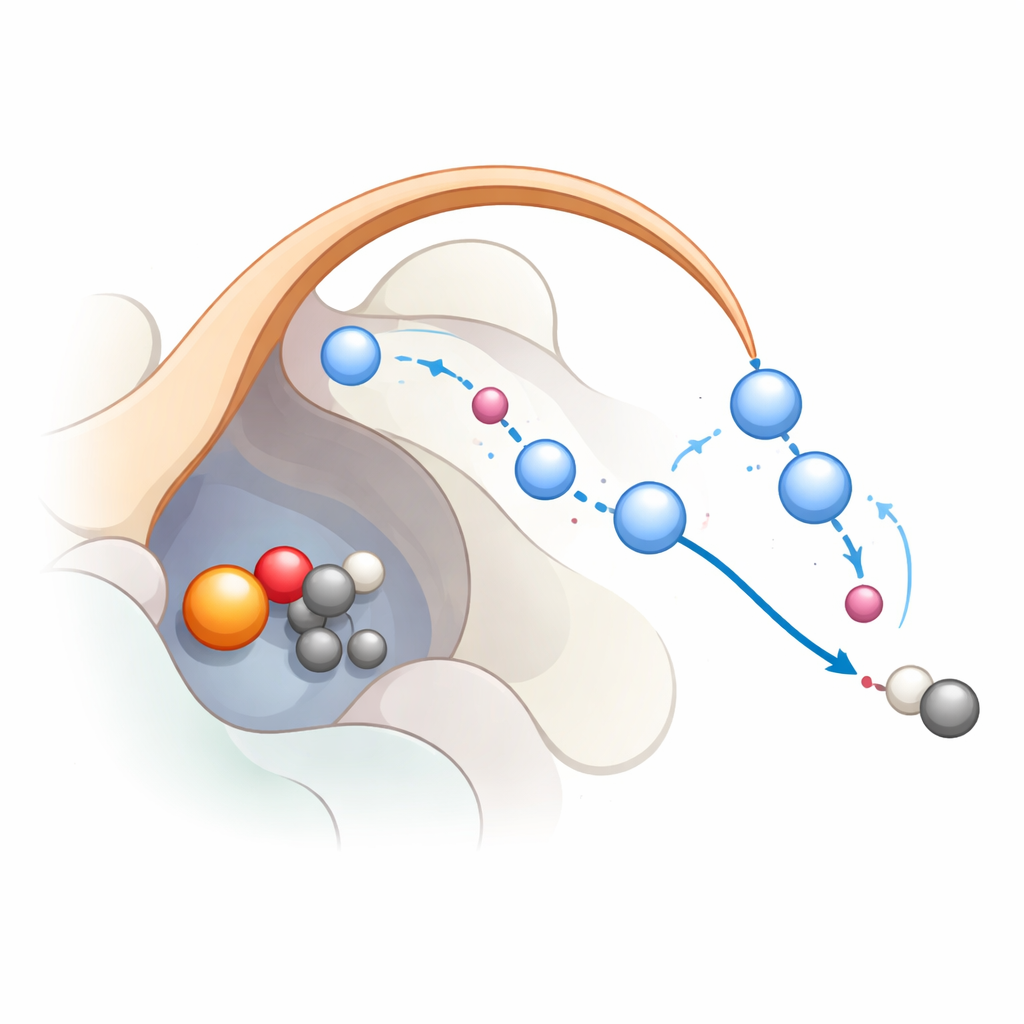
מעקב אחר שלבי התגובה שלב‑אחר‑שלב
כדי לראות כיצד הרשת עובדת בפועל במהלך התגובה, החוקרים שילבו דינמיקת מולקולות קלאסית עם סימולציות מתקדמות קוואנטומכניות. הם התחילו ממצב שבו הברזל כבר יצר מין ברזל‑אוקסו ריאקטיבי מאוד, בן‑ביניים שכיח במשפחה זו של אנזימים. החישובים תומכים במסלול בן שלושה שלבים: ראשית, הברזל‑אוקסו מושך אטום מימן מהסובסטרט ויוצר רדיקל; שנית, אלקטרון עובר חזרה לברזל ועוזר לסובסטרט להיפטר מפחמן‑דו‑חמצני; שלישית, קבוצת ההידרוקסיל הקשורה לברזל מוּוחזרת בפרוטון כך שהברזל חוזר למצב המנוחה שלו. הסימולציות מראות כי K191 והשרשרת של מולקולות המים היציבות על‑ידי לולאת המכסה מהווים מסלול העברת פרוטונים המוביל פרוטונים ביעילות בשלבים האחרונים. כאשר מסלול זה נשבר, התגובה הופכת ללא מועדפת מבחינה אנרגטית, התאמה מסודרת לנתוני המוטציות.
לולאה מסתגלת שמנחה את אבולוציית האנזים
מעבר ל‑TraH עצמו, המחברים השוו אנזימים קרובים החולקים את ליבת קשירת‑הברזל אך מטפלים במשימות כימיות שונות. רבים מהאנזימים הללו נושאים גם לולאות דמויות‑מכסה, אך אורכן, הרצף שלהן ומידת התנועה משתנים במידה ניכרת. בחלק מהן הלולאה נסגרת היטב על גבי הסובסטרטים ויוצרת קשרי מימן מרכזיים; באחרות היא נשארת פתוחה ונראית שאינה משתתפת בכימיה. באמצעות בניית עצי אבולוציה וניתוח תבניות רצף, הצוות מצא כי שרידי מכסה מסוימים המעורבים ברשת קשרי המימן של TraH שימורים בחוזקה, בעוד שמיקומים אחרים משתנים באופן שתואם להעדפות סובסטרט שונות. תוצאה זו מרמזת שאבולוציה מווסתת הן את הקשיחות והן את הכימיה של לולאות אלה כדי לזהות מולקולות חדשות ולהטות תגובות לעבר תוצאות ספציפיות.
מה המשמעות של זה עבור הכימיה העתידית
ללא‑מומחה, המסר המרכזי הוא כי לולאה גמישה קטנה על פני השטח של אנזים יכולה לשלוט באן־כיצד פרוטונים ומולקולות מים נעים בתוכו, ושבשליטה זו יכול להיות ההבדל בין כך שמולקולה תאבד פשוט מימן לבין כך שהיא תאבד גם פחמן‑דו‑חמצני. ב‑TraH, תפקיד המכסה אינו רק לסגור את האתר הפעיל אלא להרכיב מנגנון קטן להעברת פרוטונים מחומצות אמינו וממים כלואים. אסטרטגיית התיווך על‑ידי לולאה זו שונה מזו של רבים מהאנזימים הקרובים, שמשתמשים בשייר בסיסי קבוע המונח ממש לצד הקבוצה העוזבת. בעזרת גילוי העיצוב האלטרנטיבי הזה, העבודה מרחיבה את הבנתנו כיצד הטבע בונה זרזים רב‑תכליתיים ומציעה מתווה למהנדסים לעצב אנזימים שבהם חלקים נעים יכולים להיות מתוכנתים מחדש כדי לאפשר תגובות חדשות ומולקולות ביואקטיביות חדשות.
ציטוט: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
מילות מפתח: מנגנוני אנזימים, אנזימים ללא המין‑הם ברזל, העברת פרוטון, מטבוליזם משני פטרייתי, אבולוציית אנזימים