Clear Sky Science · ru
Перенос протона, опосредованный закрывающей петлей, выявлен в Fe/αKG‑зависимой декарбоксилазе TraH
Почему важна крошечная подвижная петля
Внутри микробов специализированные белки тихо собирают и перестраивают сложные молекулы, включая потенциальные антибиотики. В этом исследовании фокус направлен на один такой белок — TraH из обычного плесневого гриба. Авторы показывают, что небольшая гибкая «крышка» в TraH действует как подвижный затвор, контролирующий, как фермент отсекает часть молекулы и в некоторых случаях определяющий, какой именно химический переход произойдёт. Понимание этой движущейся части не только углубляет представление о работе природных катализаторов, но и может помочь учёным проектировать новые ферменты для синтеза лекарств и других ценных соединений.
Фунгальный помощник в синтезе молекул
TraH принадлежит к большой семье ферментов, которые используют железо и вспомогательную молекулу α‑кетоглутарат для проведения мощных окислительных реакций. Эти ферменты — ключевые участники микробной химии, где они помогают собирать «вторичные метаболиты», такие как пигменты, токсины и молекулы с лекарственными свойствами. В грибe Penicillium crustosum TraH участвует в биосинтезе терестрицовой кислоты — соединения с перспективной антибактериальной и антивирусной активностью. Главная задача TraH — отщепить карбоксильную группу в виде углекислого газа от прекурсора, называемого crustosic acid, одновременно вводя двойную связь в молекулу. Любопытно, что TraH также действует на сходную метил‑эфирную версию этого соединения, но в этом случае он лишь вводит двойную связь, не удаляя CO2.
Закрывающаяся крышка, перестраивающая активный центр
С помощью рентгеновской кристаллографии авторы получили снимки TraH в высоком разрешении в разных состояниях: пустого, связанного только с металлом и связанного с металлом плюс либо crustosic acid, либо его метил‑эфиром. Все формы имеют жесткое ядро в форме двухслойной бета‑спирали, которое удерживает атом железа, где протекает химия. Вокруг этого ядра расположены дополнительные сегменты на концах белка, включая петлю спереди, которая ведёт себя как крышка. В несвязанном состоянии эта крышка подвижна и частично не видна в кристаллической структуре, что говорит о её флуктуациях. При связывании истинного карбоксилатного субстрата крышка опускается, упорядочивается и вместе с соседними спиралями герметизирует активный центр, так что молекула оказывается глубоко внутри закрытого кармана. Для метил‑эфирного субстрата, однако, большая часть крышки остаётся неупорядоченной и оттянутой назад, что показывает: её плотное закрытие зависит от природы связанного лиганда.
Релей на основе воды для перемещения протонов
Более тщательное рассмотрение структуры с закрытой крышкой и crustosic acid выявило сложную сеть водородных связей, соединяющую крышку с консервативным лизином (K191) в ядре фермента и с карбоксильной группой субстрата. Ключевые остатки крышки позиционируют одну или две молекулы воды между K191 и реакционноспособным концом субстрата. Чтобы проверить важность этой сети, команда заменила отдельные аминокислоты в крышке и соседнем ядре. Мутации, разрушающие сеть, особенно в позициях Q99, D112, K114, K191 и Y214, резко снижали или полностью прекращали реакцию декарбоксилирования, тогда как изменения в соседних, не вовлечённых в сеть остатках почти не влияли. Напротив, большинство этих разрушительных мутаций практически не сказывались на способности фермента проводить десатурацию метил‑эфирного субстрата, что указывает на то, что водная сеть с реле важна именно для потери углекислого газа.
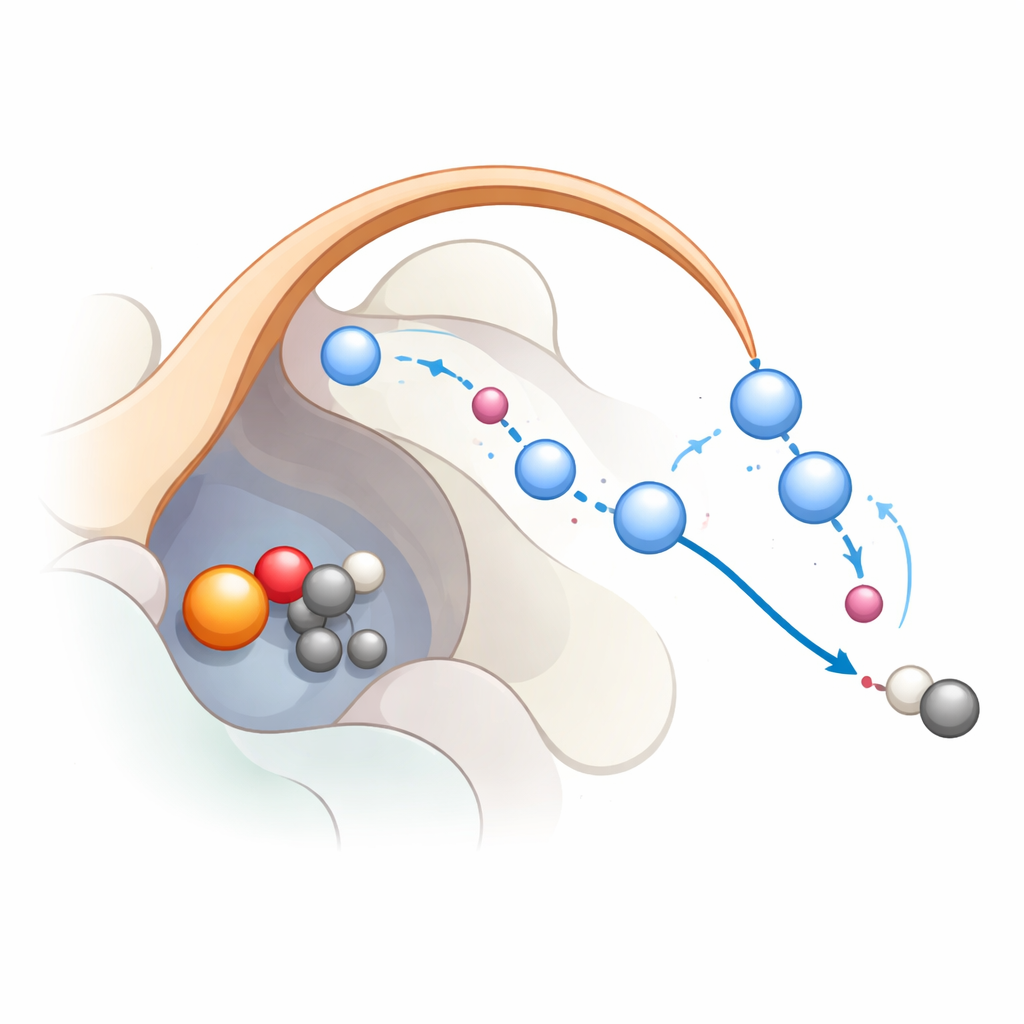
Проследить реакцию шаг за шагом
Чтобы понять, как эта сеть работает в ходе реакции, исследователи сочетали классическую молекулярную динамику с более продвинутыми квантово‑механическими моделями. Они начали из состояния, где железо уже образовало высокореактивный оксо‑вид (железо‑оксо), общий интермедиат для этой семейства ферментов. Вычисления поддерживают трёхшаговый механизм: сначала железо‑оксо отрывает атом водорода от субстрата, создавая радикал; затем электрон возвращается к железу, способствуя отщеплению карбоксильной группы в виде CO2; наконец, гидроксильная группа, связанная с железом, повторно протонируется, и железо возвращается в своё исходное состояние. Симуляции показывают, что K191 и цепочка молекул воды, стабилизируемых крышкой‑петлёй, формируют протонное реле, эффективно перенаправляющее протоны на последних этапах. Когда это реле разрушается, реакция становится энергетически неблагоприятной, что хорошо согласуется с данными мутационного анализа.
Адаптируемая петля, направляющая эволюцию ферментов
За пределами самого TraH авторы сравнили родственные ферменты, которые сохраняют одно и то же железосвязывающее ядро, но выполняют разные химические функции. Многие из этих ферментов тоже имеют петлеобразные крышки, однако их длины, последовательности и подвижность сильно различаются. В одних петля плотно закрывается над субстратом и образует ключевые водородные связи; в других она остаётся открытой и, по‑всему, не участвует в химии. Построив эволюционные деревья и проанализировав паттерны последовательностей, команда обнаружила, что некоторые остатки крышки, вовлечённые в водородную сеть TraH, сильно консервативны, тогда как другие позиции варьируют в соответствии с предпочтениями разных субстратов. Это указывает на то, что эволюция настраивает и жёсткость, и химические свойства этих петель для распознавания новых молекул и смещения реакций в требуемую сторону.
Что это значит для будущей химии
Для неспециалиста ключевое сообщение таково: небольшая гибкая петля на поверхности фермента может контролировать, куда перемещаются протоны и молекулы воды внутри, и этот контроль может определять, потеряет ли молекула только водород или также углекислый газ. В TraH задача крышки — не просто закрыть активный центр, но и собрать крошечный протон‑передающий механизм из аминокислот и захваченных молекул воды. Эта стратегия, опосредованная петлёй, отличается от подхода многих родственных ферментов, которые используют фиксированный основной остаток прямо рядом с уходящей группой. Описав этот альтернативный дизайн, работа расширяет наше понимание того, как природа строит универсальные катализаторы, и предлагает план для инженерии ферментов, чьи подвижные части можно перенастроить для создания новых реакций и новых биоактивных молекул.
Цитирование: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
Ключевые слова: механизмы ферментов, негемовые железосодержащие ферменты, перенос протона, фунгальный вторичный метаболизм, эволюция ферментов