Clear Sky Science · sv
Locketslingsförmedlad protonöverföring avslöjad i den Fe/αKG‑beroende dekarboxylasen TraH
Varför en liten rörlig loop spelar roll
Inuti mikrober bygger och omformar specialiserade proteiner tyst komplexa molekyler, inklusive potentiella antibiotika. Denna studie zoomar in på ett sådant protein, kallat TraH, från en vanlig livsmedelsfördärvande svamp. Forskarna visar att en liten flexibel ”lock” i TraH fungerar som en rörlig port som styr hur enzymet avlägsnar en del av en molekyl och, i vissa fall, hjälper avgöra vilken typ av kemisk förändring som äger rum. Att förstå denna rörliga del fördjupar inte bara vår bild av hur naturens katalysatorer fungerar, utan kan också hjälpa forskare att designa nya enzymer för framställning av läkemedel och andra värdefulla föreningar.
En svampassistent i molekylbyggande
TraH tillhör en stor familj av enzymer som använder järn och ett hjälpmolekyl kallad α‑ketoglutarat för att utföra kraftfulla oxidationsreaktioner. Dessa enzymer är centrala aktörer i mikrobiell kemi, där de hjälper till att bygga ”sekundära metaboliter” som pigment, toxiner och läkemedelsliknande molekyler. I svampen Penicillium crustosum hjälper TraH till att producera terrestric acid, en förening med lovande antibakteriella och antivirala egenskaper. TraH:s huvudsakliga uppgift är att klippa av en koldioxidgrupp från en prekursor kallad crustosic acid, samtidigt som den inför en dubbelbindning i molekylen. Intressant nog kan TraH också verka på en närbesläktad metylester‑version av samma förening, men i det fallet inför den endast en dubbelbindning utan att avlägsna koldioxid.
Ett sluttande lock som omformar det aktiva sätet
Med hjälp av röntgenkristallografi fångade författarna högupplösta ögonblicksbilder av TraH i olika tillstånd: tom, bundet till metall endast, och bundet till metall plus antingen crustosic acid eller dess metylester. Alla former delar en styv kärna formad som en dubbel‑lagrad beta‑helix, som håller järnatomen där kemin sker. Omslutna runt denna kärna finns extra segment vid proteinets ändar, inklusive en loop nära fronten som beter sig som ett lock. I obundet tillstånd är detta lock slappt och delvis osynligt i kristallstrukturen, vilket tyder på att det vandrar. När det verkliga karboxylatsubstratet binder svänger locket ner, blir välordnat och förseglar tillsammans med närliggande helixar det aktiva sätet så att molekylen sitter djupt inne i en sluten ficka. För metylestern däremot förblir mycket av locket oordnat och tillbakadraget, vilket visar att dess precisa stängning beror på vilken typ av molekyl som är bunden.
En vattenbaserad relä för att flytta protoner
Nogrann undersökning av den slutna‑lock‑strukturen med crustosic acid avslöjade ett intrikat nätverk av vätebindningar som länkar locket till en konserverad lysin (K191) i enzymets kärna och till substratets karboxylgrupp. Viktiga rester i locket hjälper till att positionera en eller två vattenmolekyler mellan K191 och substratets reagerande ände. För att testa hur viktigt detta nätverk är förändrade teamet enskilda aminosyror i locket och i den närliggande kärnan. Mutationer som störde nätverket, särskilt vid positionerna Q99, D112, K114, K191 och Y214, minskade kraftigt eller avskaffade dekarboxyleringsreaktionen, medan förändringar i närliggande, icke‑nätverksresiduer hade liten effekt. Däremot påverkade de flesta av dessa störande mutationer knappt enzymets förmåga att utföra desaturering på metylester‑substratet, vilket tyder på att det vattenmedierade nätverket är avgörande specifikt för förlust av koldioxid.
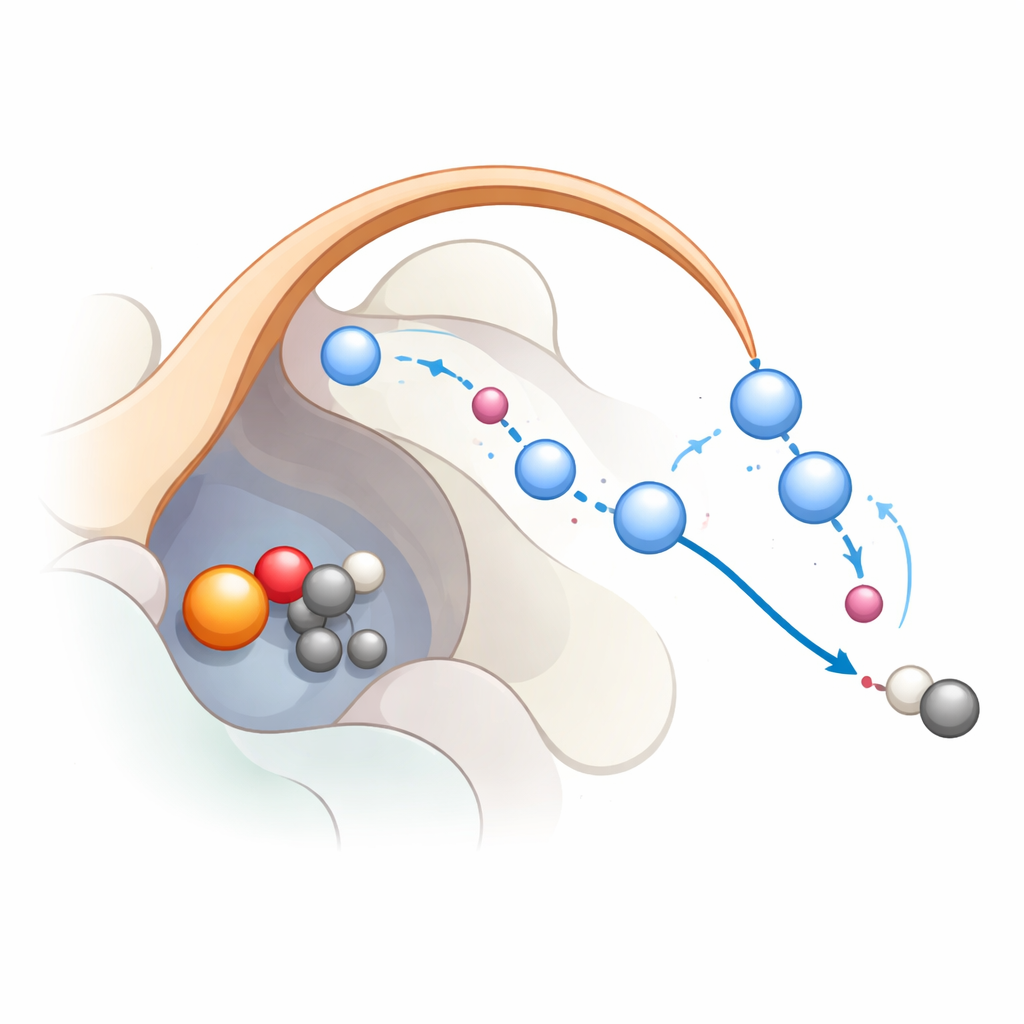
Följa reaktionen steg för steg
För att se hur detta nätverk faktiskt fungerar under reaktionen kombinerade forskarna klassisk molekylär dynamik med mer avancerade kvantmekaniska simuleringar. De startade från ett tillstånd där järnet redan bildat en högreaktiv järn‑oxo‑art, ett vanligt mellanprodukt i denna enzymfamilj. Beräkningarna stöder en trestegs‑väg: först drar järn‑oxo ut en väteatom från substratet och bildar en radical; andra steget är att en elektron förskjuts tillbaka till järnet, vilket hjälper substratet att göra sig av med koldioxid; tredje steget är att den järnbundna hydroxylgruppen reprotoneras så att järnet återvänder till sitt vilotillstånd. Simulationerna visar att K191 och kedjan av vattenmolekyler stabiliserade av lockloopen bildar ett protonrelä som effektivt förflyttar protoner under de sista stegen. När detta relä bryts blir reaktionen energimässigt ogynnsam, vilket passar väl med mutationsdata.
En anpassningsbar loop som styr enzymutveckling
Bortom TraH jämförde författarna närliggande enzymer som delar samma järnbindande kärna men hanterar olika kemiska uppgifter. Många av dessa enzymer har också lock‑liknande loopar, men deras längder, sekvenser och rörlighetsgrad varierar stort. I vissa stänger loopen ordentligt över substraten och bildar viktiga vätebindningar; i andra förblir den öppen och verkar inte delta i kemin. Genom att bygga evolutionära träd och analysera sekvensmönster fann teamet att vissa lockresiduer som är involverade i TraH:s vätebindningsnätverk är starkt konserverade, medan andra positioner varierar på ett sätt som följer olika substratpreferenser. Detta tyder på att evolutionen ställer in både stelheten och kemin hos dessa loopar för att känna igen nya molekyler och för att styra reaktionerna mot särskilda utfall.
Vad detta betyder för framtidens kemi
För en icke‑specialist är huvudbudskapet att en liten flexibel loop på ytan av ett enzym kan kontrollera var protoner och vattenmolekyler färdas inuti, och att denna kontroll kan avgöra om en molekyl bara förlorar en väteatom eller också förlorar koldioxid. I TraH är locket inte bara till för att stänga det aktiva sätet utan för att montera en liten protonöverföringsmaskin bestående av aminosyror och instängda vattenmolekyler. Denna loopförmedlade strategi skiljer sig från många närbesläktade enzymer, som använder en fast basisk rest placerad precis intill den avgående gruppen. Genom att avslöja denna alternativa design breddar arbetet vår förståelse för hur naturen bygger mångsidiga katalysatorer och erbjuder en ritning för hur man kan konstruera enzymer vars rörliga delar kan omkopplas för att möjliggöra nya reaktioner och nya bioaktiva molekyler.
Citering: Zheng, X., Ge, R., Guo, Z. et al. Lid loop-mediated proton transfer revealed in the Fe/αKG-dependent decarboxylase TraH. Commun Chem 9, 159 (2026). https://doi.org/10.1038/s42004-026-01986-9
Nyckelord: enzymmekanismer, icke‑hem‑järn‑enzymer, protonöverföring, fungal sekundärmetabolism, enzymutveckling