Clear Sky Science · zh
同时靶向拓扑异构酶 I 和 DNA G-四链体可增强结直肠癌的衰老反应和化疗敏感性
这一新癌症策略为何重要
许多结直肠癌患者最终对常规化疗失去反应,使肿瘤在积极治疗下仍能继续生长。该研究描述了一种新的候选药物,称为 ZBH-01,旨在同时从两个关键方向攻击癌细胞:它既能损伤 DNA,又能关闭维持癌细胞“不朽性”的重要发动机。通过将这两种作用合并到单一、更易溶解的分子中,这项工作为使顽固、耐药的肿瘤再次变得脆弱提供了一种潜在路径。
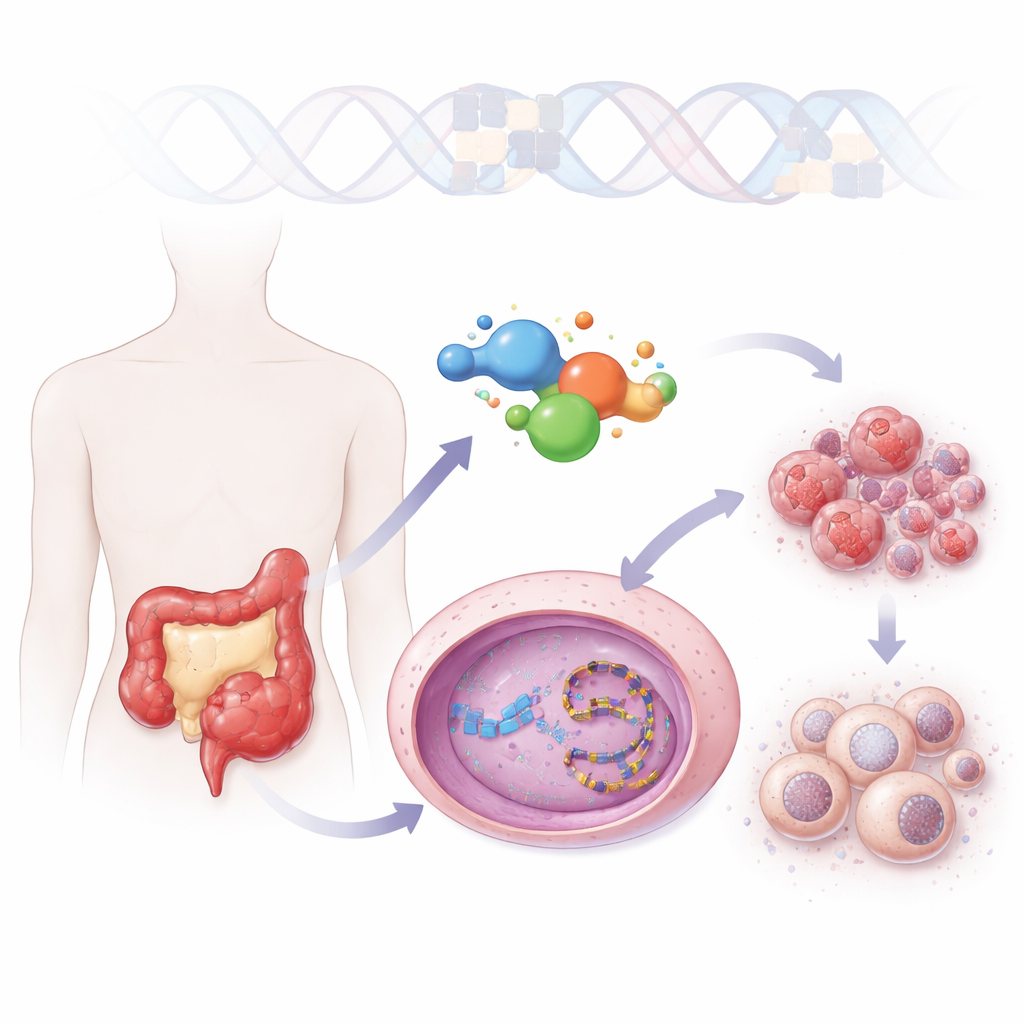
对一种老牌抗癌药的新诠释
医生已经使用一种名为伊立替康(irinotecan)的药物治疗结直肠癌,但它必须在体内转化为一种活性形式,该形式溶解性差且易被迅速失活。ZBH-01 基于相同的核心化学骨架构建,但经过工程改造以避免这些缺点。它在水中的溶解性大大改善,并且可直接发挥作用,无需代谢活化。在多种癌细胞系的测试中,ZBH-01 的效力可与现有最佳伊立替康代谢物相媲美,并且明显强于伊立替康本身,即使在更低剂量下也是如此。结构模拟显示,ZBH-01 夹持同一处理 DNA 的酶——拓扑异构酶 I,但形成了额外的接触点,使该酶被稳定地“卡”在 DNA 上,从而增加了癌细胞基因物质所承受的应激。
打击癌细胞保持“年轻”的所在
癌细胞常通过过度激活端粒酶来保持无限分裂的能力,端粒酶可保护染色体末端。研究人员将注意力集中在控制端粒酶主要成分 hTERT 的 DNA “开关”上。该区域可折叠成不寻常的四链结构,称为 G-四链体,这类结构往往减缓或阻断基因活性。通过高分辨率核磁共振和其他生物物理方法,团队发现 ZBH-01 能整齐地堆叠在 hTERT G-四链体的一端,从而稳定了这种折叠结构,并使得像 MYC 和 SP1 这样强有力的促生长蛋白更难结合并启动 hTERT 基因的表达。
迫使受损细胞进入永久“退休”
当结直肠癌细胞暴露于 ZBH-01 时,其基因表达谱显著向与 DNA 损伤、衰老和细胞周期停滞相关的通路转变。与对照化合物相比,该药增加了断裂 DNA 的标志并更强烈地缩短了端粒——染色体的保护帽。同时,它显著降低了 hTERT 及数个通常推动细胞持续分裂的基因的水平。结果,许多被处理的细胞进入了细胞衰老状态:一种仍然存活但永久退出分裂周期的状态。这些衰老细胞累积了“停摆”细胞核的化学和结构特征,并且随时间形成的克隆明显减少。
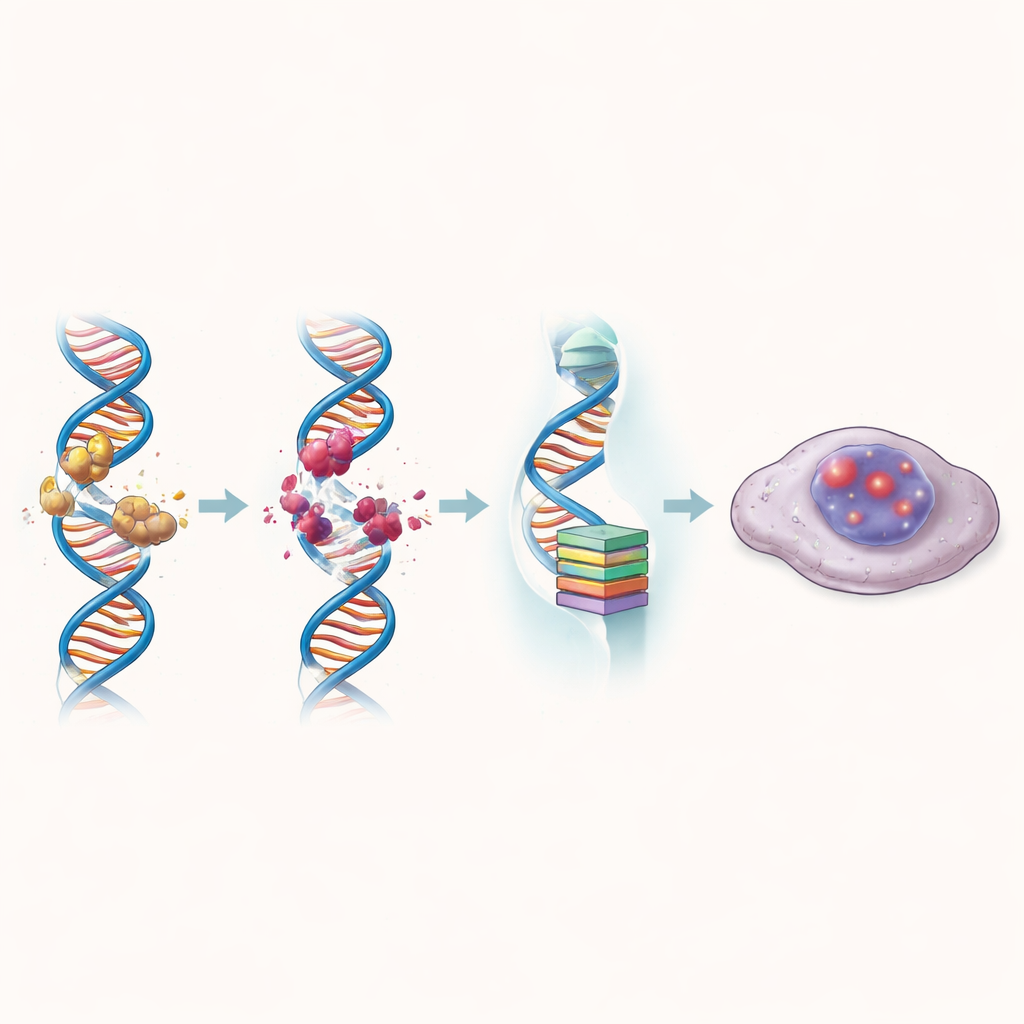
克服对常见化疗的耐药性
任何新结直肠癌治疗的关键考验是它在常规药物失效时是否仍能发挥作用。作者研究了对顺铂或氟尿嘧啶(5-fluorouracil)产生耐药的细胞,这两种药物被广泛使用。在这两种耐药模型中,ZBH-01 的效果远优于伊立替康及其活性代谢物,可将抑制生长所需的剂量降低数十倍。在与顺铂或氟尿嘧啶按精心选择的浓度联合使用时,ZBH-01 表现出协同效应:组合用药比任一单药更有效地杀死耐药细胞。这种双重作用分子还降低了若干帮助细胞泵出药物或修复化疗诱导损伤的基因活性,暗示它可能同时削弱多种耐药手段。
这对未来治疗可能意味着什么
通过在单一、性质良好的分子中将 DNA 损伤与端粒酶抑制结合,ZBH-01 为下一代癌症药物提供了蓝图,这类药物可从多个角度打击肿瘤生存机制。在实验室模型中,这一策略不仅减缓了细胞生长,还将癌细胞推向不可逆的衰老并恢复了对其他化疗药物的敏感性。尽管仍需大量工作——包括安全性研究以及动物和人体试验——但该研究表明,经过周到设计的双靶向药物或能帮助战胜使结直肠癌难治的适应性特征。
引用: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
关键词: 结直肠癌, 化疗耐药, 端粒酶, DNA 损伤, 靶向治疗