Clear Sky Science · es
Dobles dianas sobre la topoisomerasa I y los G-cuádruplex de ADN aumenta la senescencia y la quimiosensibilidad en el cáncer colorrectal
Por qué importa esta nueva estrategia contra el cáncer
Muchas personas con cáncer colorrectal acaban dejando de responder a la quimioterapia estándar, lo que permite que los tumores crezcan a pesar de tratamientos agresivos. Este estudio describe un nuevo candidato farmacológico, llamado ZBH-01, diseñado para atacar las células cancerosas en dos frentes críticos a la vez: daña su ADN y además apaga un motor clave de su inmortalidad. Al combinar estas acciones en una sola molécula más soluble, el trabajo ofrece una vía potencial para volver vulnerables a tumores resistentes a los fármacos.
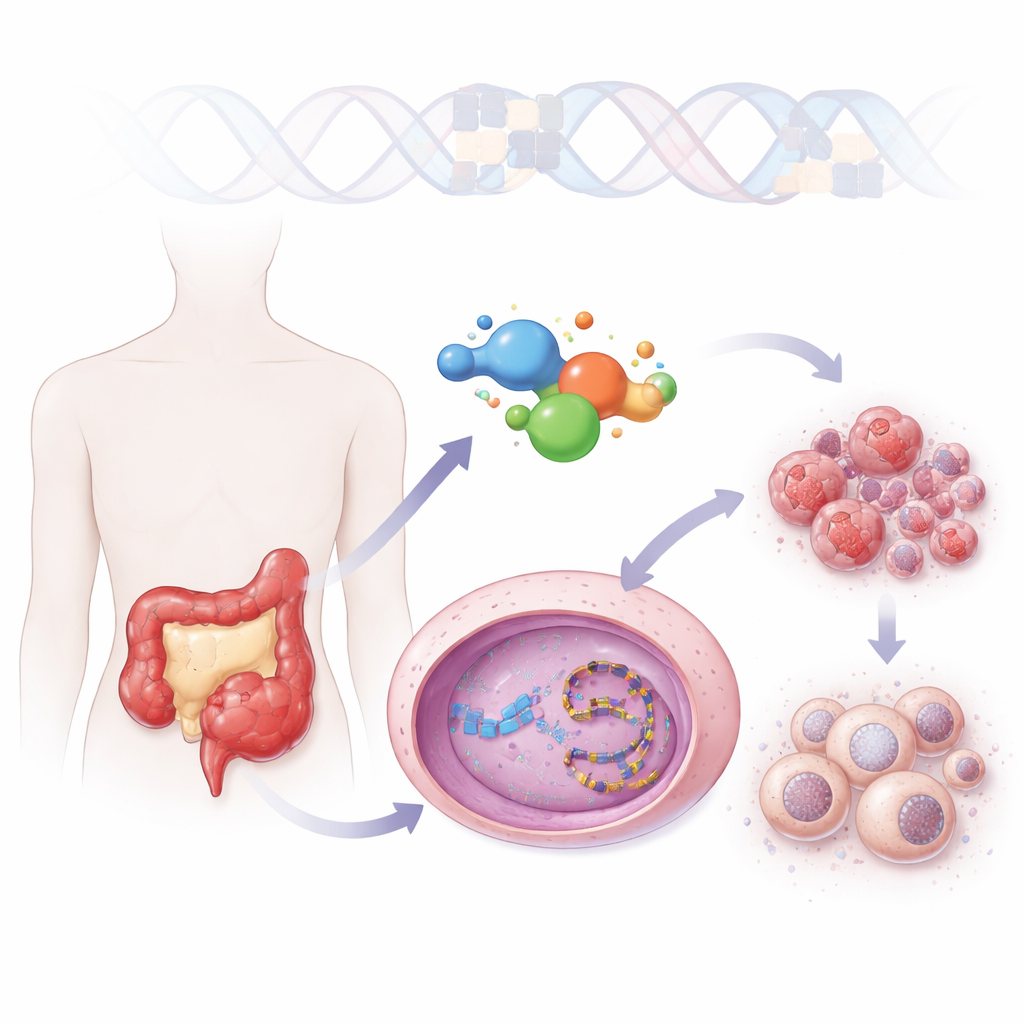
Una nueva mirada a una familia antigua de fármacos oncológicos
Los médicos ya emplean un fármaco llamado irinotecán para el cáncer colorrectal, pero debe convertirse dentro del organismo en una forma activa que es poco soluble y se inactiva con rapidez. ZBH-01 se basa en el mismo andamiaje químico central, pero se ha diseñado para evitar estos inconvenientes. Se disuelve mucho mejor en agua y actúa de forma directa sin necesitar activación metabólica. En pruebas en múltiples líneas celulares tumorales, ZBH-01 fue tan potente como el mejor metabolito activo del irinotecán y claramente más fuerte que el propio irinotecán, incluso a dosis menores. Modelos estructurales mostraron que ZBH-01 se sujeta a la misma enzima procesadora del ADN, la topoisomerasa I, pero establece contactos adicionales que estabilizan la enzima atrapada sobre el ADN, aumentando el estrés sobre el material genético de la célula cancerosa.
Atacar al cáncer donde mantiene su juventud
Las células cancerosas frecuentemente mantienen su capacidad de dividirse indefinidamente mediante la sobreactivación de la telomerasa, una enzima que protege los extremos de los cromosomas. Los investigadores se centraron en el “interruptor” de ADN que controla el componente principal de la telomerasa, hTERT. Esta región puede plegarse en formas inusuales de cuatro hebras conocidas como G-cuádruplexes, que tienden a ralentizar o bloquear la actividad génica. Usando NMR de alta resolución y otros métodos biofísicos, el equipo descubrió que ZBH-01 se apila ordenadamente en un extremo del G-cuádruplex de hTERT. Al hacerlo, estabiliza esta estructura plegada y dificulta que proteínas potentes impulsoras del crecimiento, como MYC y SP1, se unan y activen el gen hTERT.
Forzar a las células dañadas a una jubilación permanente
Cuando las células de cáncer colorrectal se expusieron a ZBH-01, sus patrones de expresión génica cambiaron drásticamente hacia vías vinculadas con el daño en el ADN, el envejecimiento y la detención del ciclo celular. El fármaco aumentó los marcadores de rotura del ADN y acortó los telómeros, las tapas protectoras de los cromosomas, con más intensidad que los compuestos de comparación. Al mismo tiempo, redujo de forma pronunciada los niveles de hTERT y de varios otros genes que normalmente empujan a las células a seguir dividiéndose. Como resultado, muchas células tratadas entraron en senescencia celular: un estado en el que permanecen vivas pero excluidas de forma permanente del ciclo de división. Estas células senescentes acumularon señas químicas y estructurales de núcleos “apagados” y formaron muchas menos colonias con el tiempo.
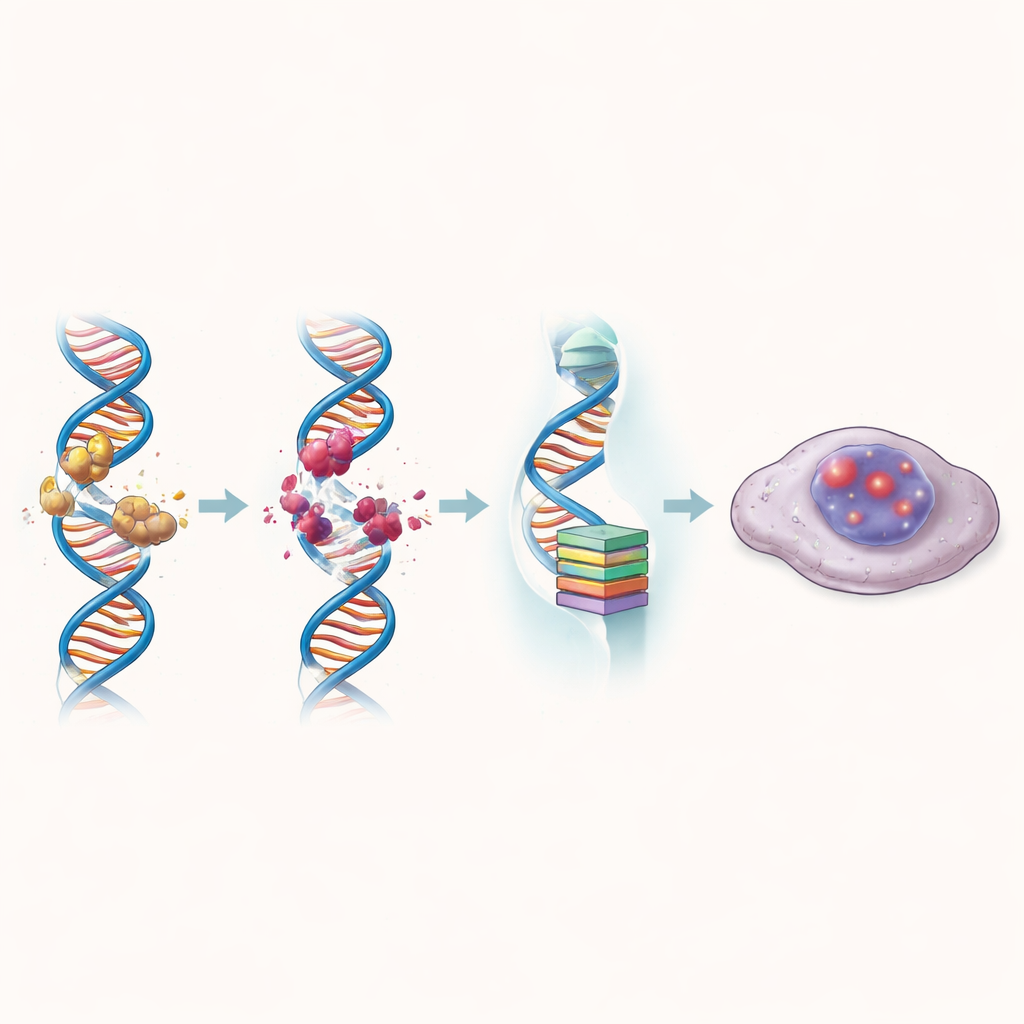
Superar la resistencia a quimioterapias comunes
Una prueba clave para cualquier nueva terapia del cáncer colorrectal es si puede ayudar cuando los fármacos estándar fallan. Los autores examinaron células que se habían vuelto resistentes al cisplatino o a 5-fluorouracilo, dos agentes ampliamente usados. En ambos modelos resistentes, ZBH-01 fue mucho más eficaz que el irinotecán o su metabolito activo, reduciendo la dosis necesaria para frenar el crecimiento hasta por decenas de veces. Cuando se combinó con cisplatino o 5-fluorouracilo en concentraciones cuidadosamente elegidas, ZBH-01 actuó de forma sinérgica: juntos, los fármacos mataron las células resistentes con mayor eficiencia que cualquiera de ellos por separado. La molécula de doble acción también redujo la actividad de varios genes que ayudan a las células a expulsar fármacos o a reparar el daño inducido por quimioterapia, lo que sugiere que puede atenuar varias estrategias de resistencia a la vez.
Qué podría significar esto para tratamientos futuros
Al unir el daño al ADN y la supresión de la telomerasa en una sola molécula bien comportada, ZBH-01 ofrece un modelo para fármacos oncológicos de próxima generación que ataquen la supervivencia tumoral desde más de un ángulo. En modelos de laboratorio, esta estrategia no solo ralentizó el crecimiento celular sino que empujó a las células cancerosas hacia una senescencia irreversible y restauró la sensibilidad a otras quimioterapias. Aunque queda mucho trabajo por delante —incluyendo estudios de seguridad y ensayos en animales y humanos— la investigación sugiere que fármacos de doble diana diseñados con criterio podrían ayudar a burlar la adaptabilidad que hace que el cáncer colorrectal sea tan difícil de tratar.
Cita: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
Palabras clave: cáncer colorrectal, quimiorresistencia, telomerasa, daño en el ADN, terapia dirigida