Clear Sky Science · pl
Podwójne ukierunkowanie na topoizomerazę I i DNA G-czwórki zwiększa senescencję i chemoskuteczność w raku jelita grubego
Dlaczego ta nowa strategia onkologiczna ma znaczenie
Wiele osób z rakiem jelita grubego ostatecznie przestaje reagować na standardową chemioterapię, co pozwala guzom rosnąć pomimo agresywnego leczenia. W tym badaniu opisano nowego kandydata na lek, nazwanego ZBH-01, zaprojektowanego tak, by jednocześnie atakować komórki nowotworowe na dwóch kluczowych frontach: uszkadzać ich DNA i jednocześnie wyłączać istotny mechanizm ich „nieśmiertelności”. Poprzez połączenie tych działań w pojedynczej, bardziej rozpuszczalnej cząsteczce, praca ta oferuje potencjalny sposób na uczynienie opornych na leki guzów znów wrażliwymi.
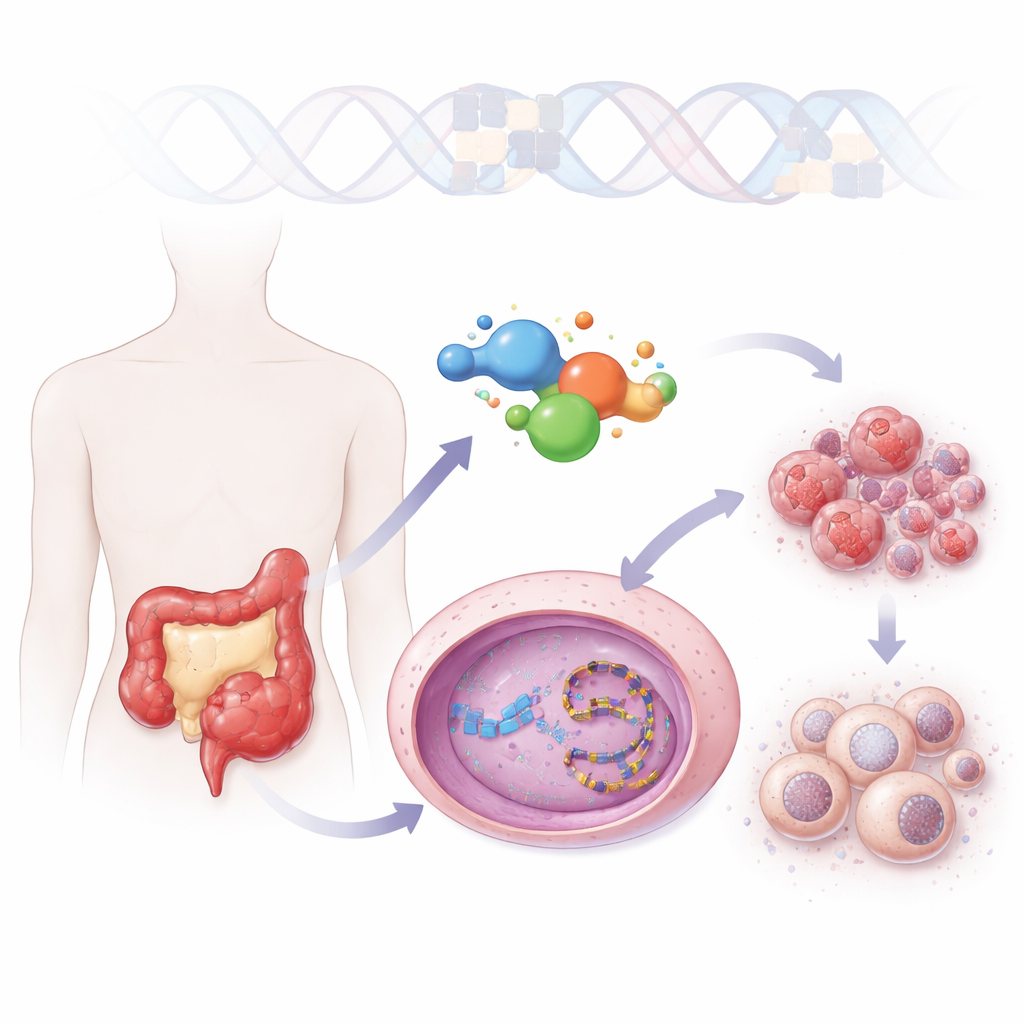
Nowe spojrzenie na starą rodzinę leków przeciwnowotworowych
Lek irinotekan jest już stosowany w raku jelita grubego, ale musi być przekształcony w organizmie do aktywnej postaci, która ma słabą rozpuszczalność i szybko ulega inaktywacji. ZBH-01 oparty jest na tej samej podstawowej szkielecie chemicznym, lecz został zaprojektowany tak, by uniknąć tych wad. Rozpuszcza się znacznie lepiej w wodzie i działa bezpośrednio, bez konieczności aktywacji metabolicznej. W testach na wielu liniach komórkowych nowotworowych ZBH-01 był tak samo silny jak najlepszy znany metabolit irinotekanu i wyraźnie silniejszy niż sam irinotekan, nawet przy niższych dawkach. Modelowanie strukturalne wykazało, że ZBH-01 przytrzymuje tę samą enzymatyczną maszynerię przetwarzającą DNA, topoizomerazę I, ale tworzy dodatkowe kontakty, które stabilizują enzym uwięziony na DNA, zwiększając stres na materiale genetycznym komórki nowotworowej.
Uderzenie tam, gdzie nowotwór zachowuje młodość
Komórki nowotworowe często utrzymują zdolność nieograniczonego dzielenia się przez nadaktywację telomerazy, enzymu chroniącego końce chromosomów. Badacze skupili się na „przełączniku” DNA kontrolującym główny składnik telomerazy, hTERT. Ten obszar może składać się w nietypowe, czteroniciowe struktury znane jako G-czwórki, które mają tendencję do spowalniania lub blokowania aktywności genów. Przy użyciu wysokorozdzielczej spektroskopii NMR i innych metod biofizycznych zespół wykazał, że ZBH-01 układa się piętrowo na jednym końcu G-czwórki hTERT. Stabilizując tę złożoną strukturę, utrudnia wiązanie się potężnych białek napędzających wzrost, takich jak MYC i SP1, i włączanie genu hTERT.
Wpychanie uszkodzonych komórek w trwałą emeryturę
Po ekspozycji komórek raka jelita grubego na ZBH-01 ich wzorce aktywności genów przesunęły się radykalnie w stronę szlaków związanych z uszkodzeniami DNA, starzeniem i zatrzymaniem cyklu komórkowego. Lek zwiększał markery złamanej nici DNA i skrócenie telomerów — ochronnych czapek na chromosomach — silniej niż związki porównawcze. Jednocześnie wyraźnie obniżył poziomy hTERT i kilku innych genów, które zazwyczaj popychają komórki do dalszego dzielenia się. W rezultacie wiele leczonych komórek weszło w senescencję komórkową: stan, w którym komórki pozostają żywe, ale trwale wyłączone z cyklu podziałowego. Te senescentne komórki akumulowały chemiczne i strukturalne cechy „wyłączonych” jąder i z biegiem czasu tworzyły znacznie mniej kolonii.
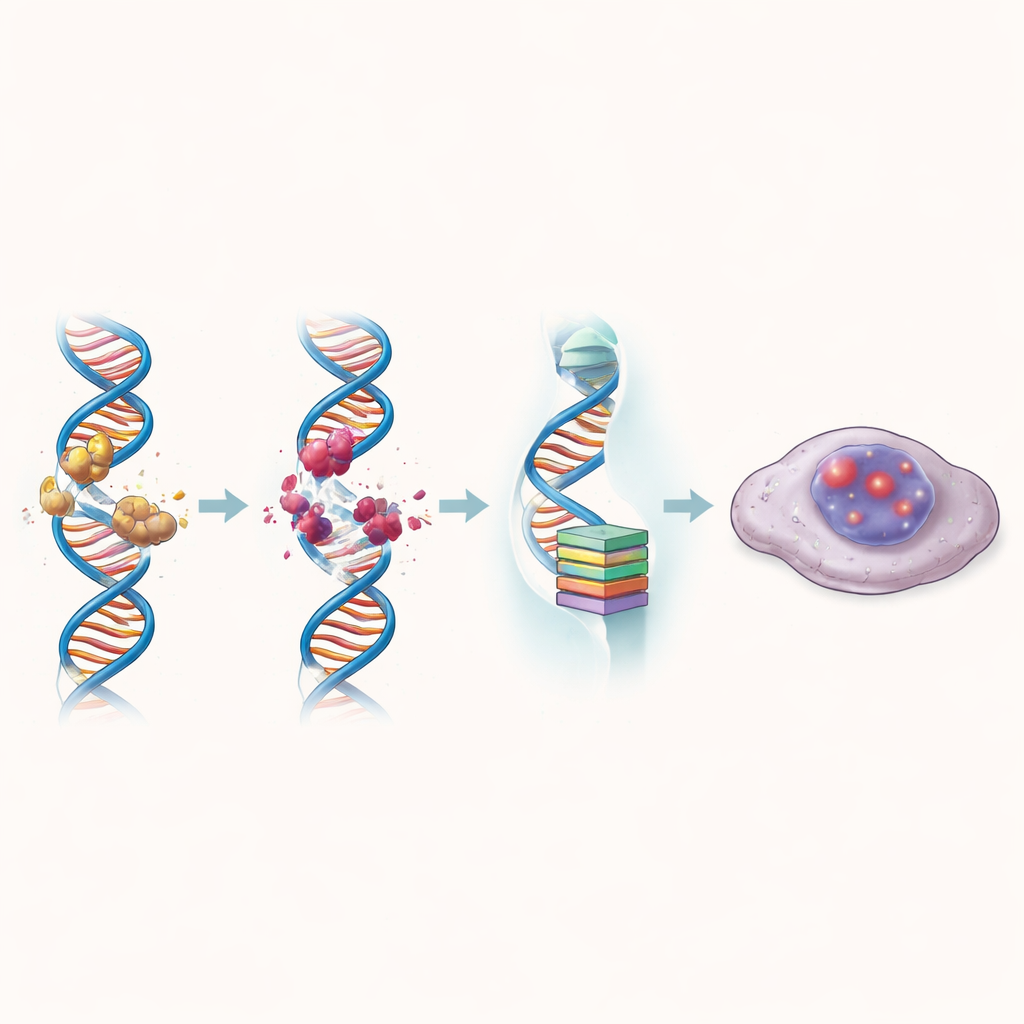
Przezwyciężanie oporności na powszechną chemioterapię
Kluczowym testem dla każdej nowej terapii raka jelita grubego jest to, czy pomaga, gdy standardowe leki zawodzą. Autorzy zbadali komórki, które stały się oporne na cisplatynę lub 5-fluorouracyl, dwa szeroko stosowane środki. W obu modelach oporności ZBH-01 okazał się znacznie skuteczniejszy niż irinotekan lub jego aktywny metabolit, zmniejszając dawkę potrzebną do zahamowania wzrostu nawet wielkakrotnie. W połączeniu z cisplatyną lub 5-fluorouracylem w starannie dobranych stężeniach ZBH-01 działał synergicznie: razem leki zabijały oporne komórki skuteczniej niż każdy z nich osobno. Cząsteczka o podwójnym działaniu obniżała także aktywność kilku genów, które pomagają komórkom wypompowywać leki lub naprawiać uszkodzenia wywołane chemioterapią, co sugeruje, że może osłabiać kilka mechanizmów oporności jednocześnie.
Co to może znaczyć dla przyszłych terapii
Łącząc uszkodzenia DNA i hamowanie telomerazy w pojedynczej, dobrze zachowującej się cząsteczce, ZBH-01 pokazuje wzorzec działania dla leków nowej generacji, które atakują przetrwanie guza z więcej niż jednego kąta. W modelach laboratoryjnych ta strategia nie tylko spowalniała wzrost komórek, lecz także popychała komórki nowotworowe w nieodwracalną senescencję i przywracała wrażliwość na inne chemioterapie. Choć pozostało wiele pracy — w tym badania bezpieczeństwa oraz testy na zwierzętach i ludziach — badania sugerują, że przemyślanie zaprojektowane leki o podwójnym celu mogą pomóc przechytrzyć adaptacyjność, która sprawia, że rak jelita grubego jest tak trudny do leczenia.
Cytowanie: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
Słowa kluczowe: rak jelita grubego, oporność na chemioterapię, telomeraza, uszkodzenia DNA, terapia celowana