Clear Sky Science · pt
Duplo direcionamento da topoisomerase I e dos G-quadruplexos de DNA aumenta senescência e quimiossensibilidade no câncer colorretal
Por que essa nova estratégia contra o câncer importa
Muitas pessoas com câncer colorretal acabam parando de responder à quimioterapia padrão, permitindo que tumores cresçam apesar do tratamento agressivo. Este estudo descreve um novo candidato a fármaco, chamado ZBH-01, projetado para atacar células cancerosas em duas frentes críticas ao mesmo tempo: ele danifica o DNA e também desativa um motor chave de sua imortalidade. Ao combinar essas ações em uma única molécula mais solúvel, o trabalho oferece uma forma potencial de tornar tumores resistentes a medicamentos vulneráveis novamente.
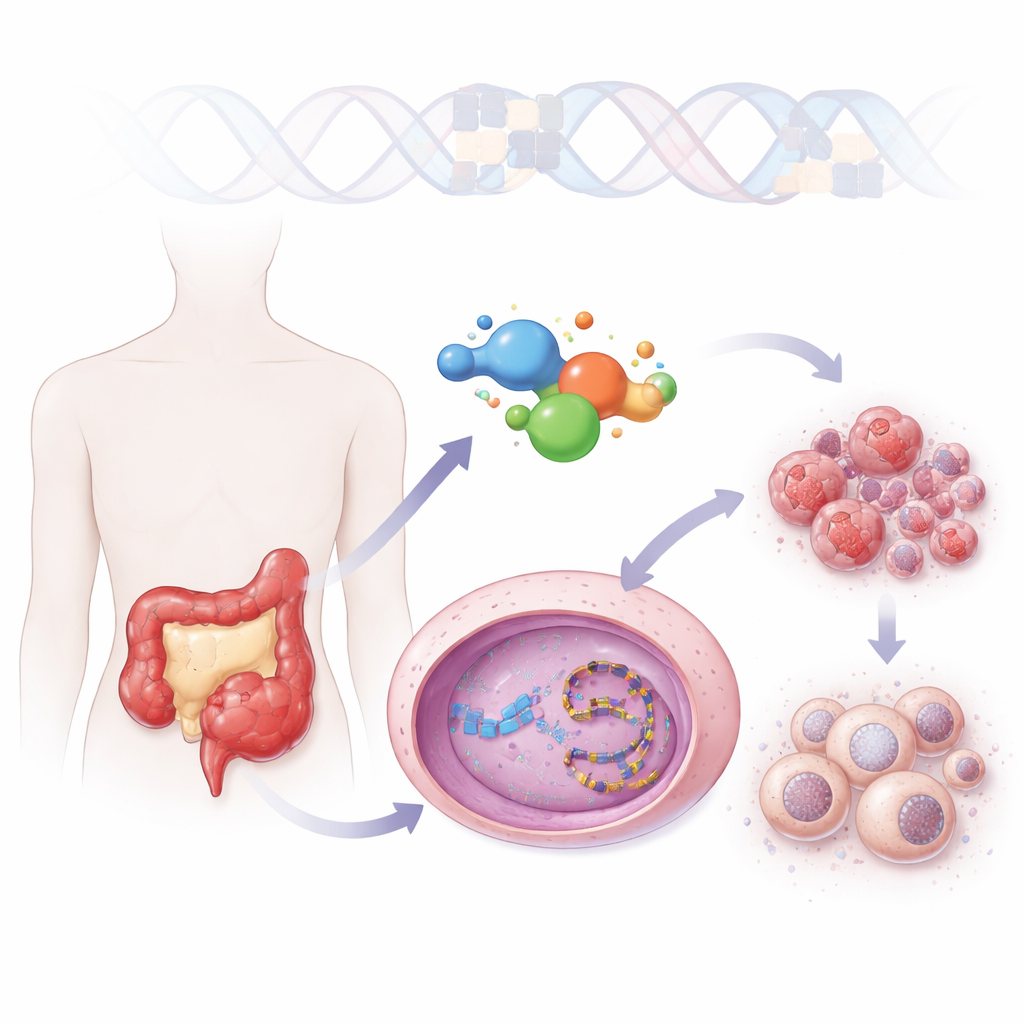
Uma nova abordagem para uma família antiga de medicamentos contra o câncer
Médicos já usam um fármaco chamado irinotecano para câncer colorretal, mas ele precisa ser convertido dentro do corpo em uma forma ativa que é pouco solúvel e rapidamente inativada. O ZBH-01 é construído sobre o mesmo esqueleto químico central, mas foi projetado para evitar essas limitações. Dissolve-se muito melhor em água e age diretamente sem precisar de ativação metabólica. Em testes em várias linhas celulares cancerígenas, o ZBH-01 foi tão potente quanto o melhor metabólito ativo do irinotecano e claramente mais forte que o próprio irinotecano, mesmo em doses menores. Modelagem estrutural mostrou que o ZBH-01 se prende à mesma enzima que processa o DNA, a topoisomerase I, mas forma contatos extras que estabilizam a enzima presa ao DNA, aumentando o estresse sobre o material genético da célula cancerosa.
Atingindo o câncer onde ele mantém sua juventude
Células cancerosas frequentemente mantêm sua capacidade de dividir-se indefinidamente ao superativar a telomerase, uma enzima que protege as extremidades dos cromossomos. Os pesquisadores concentraram-se no “interruptor” de DNA que controla o componente principal da telomerase, hTERT. Essa região pode se dobrar em formas incomuns de quatro fitas conhecidas como G-quadruplexos, que tendem a retardar ou bloquear a atividade gênica. Usando RMN de alta resolução e outros métodos biofísicos, a equipe descobriu que o ZBH-01 se empilha ordenadamente em uma das extremidades do G-quadruplexo do hTERT. Ao fazer isso, ele estabiliza essa estrutura dobrada e dificulta a ligação de proteínas potentes que impulsionam o crescimento, como MYC e SP1, impedindo que ativem o gene hTERT.
Forçando células danificadas a aposentadoria permanente
Quando células de câncer colorretal foram expostas ao ZBH-01, seus padrões de atividade gênica mudaram dramaticamente para vias associadas a danos no DNA, envelhecimento e parada do ciclo celular. O fármaco aumentou marcadores de DNA quebrado e encurtou telômeros, as tampas protetoras dos cromossomos, mais fortemente do que compostos de comparação. Ao mesmo tempo, reduziu fortemente os níveis de hTERT e de vários outros genes que normalmente empurram as células a continuar se dividindo. Como resultado, muitas células tratadas entraram em senescência celular: um estado em que permanecem vivas, mas permanentemente excluídas do ciclo de divisão. Essas células senescentes acumularam marcas químicas e estruturais de núcleos “desligados” e formaram muito menos colônias ao longo do tempo.
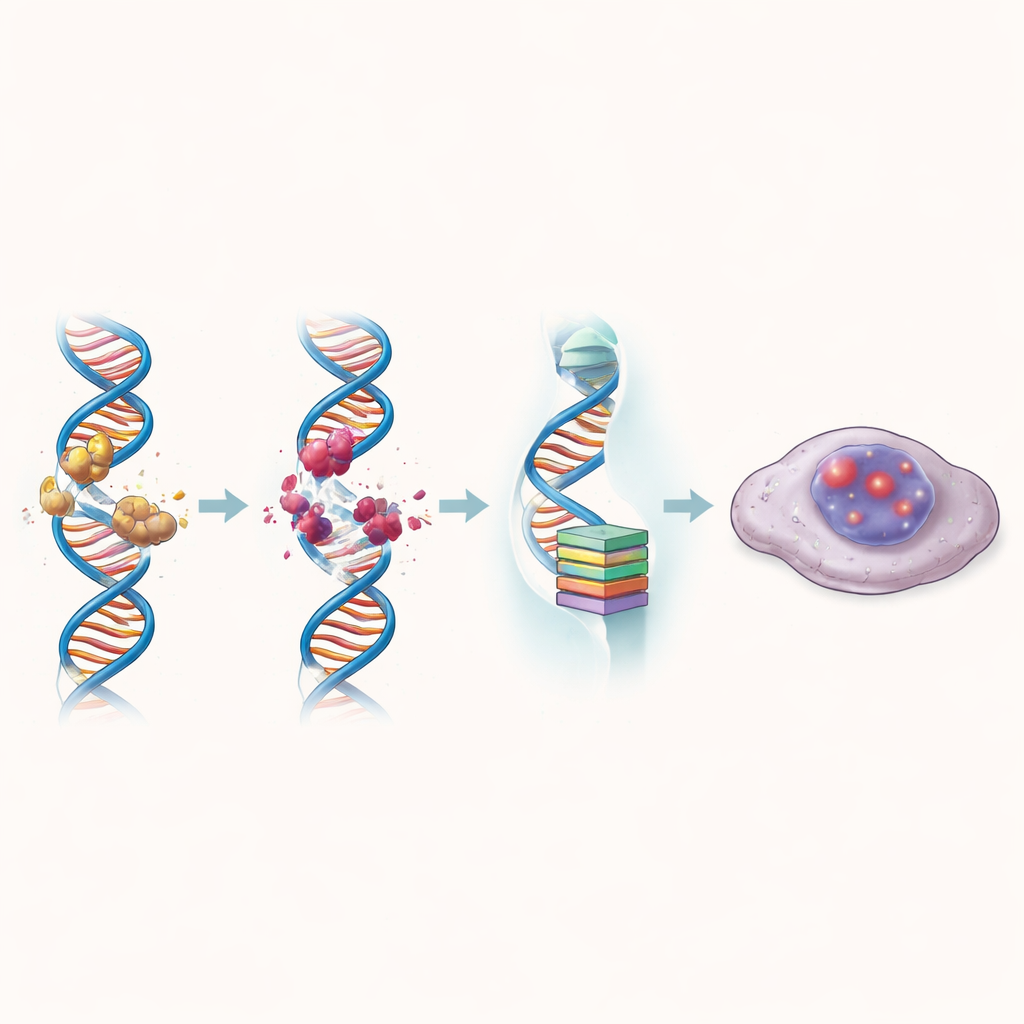
Superando a resistência à quimioterapia comum
Um teste chave para qualquer nova terapia contra o câncer colorretal é se ela pode ajudar quando os medicamentos padrão falham. Os autores examinaram células que se tornaram resistentes à cisplatina ou à 5-fluorouracila, dois agentes amplamente usados. Em ambos os modelos resistentes, o ZBH-01 foi muito mais eficaz do que o irinotecano ou seu metabólito ativo, reduzindo a dose necessária para inibir o crescimento em dezenas de vezes. Quando combinado com cisplatina ou 5-fluorouracila em concentrações cuidadosamente escolhidas, o ZBH-01 atuou sinergicamente: juntos, os fármacos mataram células resistentes de forma mais eficiente do que qualquer um isoladamente. A molécula de ação dupla também reduziu a atividade de vários genes que ajudam as células a bombear fora os fármacos ou reparar danos induzidos pela quimioterapia, sugerindo que pode atenuar múltiplos mecanismos de resistência ao mesmo tempo.
O que isso pode significar para tratamentos futuros
Ao unir dano ao DNA e supressão da telomerase em uma única molécula bem comportada, o ZBH-01 oferece um roteiro para fármacos anticâncer de próxima geração que atacam a sobrevivência tumoral por mais de um ângulo. Em modelos laboratoriais, essa estratégia não apenas desacelerou o crescimento celular, mas empurrou células cancerosas para uma senescência irreversível e restaurou a sensibilidade a outras quimioterapias. Embora ainda reste muito trabalho — incluindo estudos de segurança e testes em animais e humanos — a pesquisa sugere que fármacos de dupla ação, projetados com critério, poderiam ajudar a contornar a adaptabilidade que torna o câncer colorretal tão difícil de tratar.
Citação: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
Palavras-chave: câncer colorretal, quimiorresistência, telomerase, danos ao DNA, terapia alvo dirigida