Clear Sky Science · it
Doppio bersaglio: topoisomerasi I e quadruplex del DNA aumentano senescenza e chemosensibilità nel carcinoma colorettale
Perché questa nuova strategia oncologica è importante
Molte persone con carcinoma colorettale finiscono col non rispondere più alla chemioterapia standard, permettendo ai tumori di crescere nonostante trattamenti aggressivi. Questo studio descrive un nuovo candidato farmacologico, chiamato ZBH-01, progettato per attaccare le cellule tumorali su due fronti critici contemporaneamente: danneggia il loro DNA e al tempo stesso spegne un motore chiave della loro immortalità. Combinando queste azioni in una singola molecola più solubile, il lavoro propone un modo potenziale per rendere nuovamente vulnerabili i tumori ostinati e resistenti ai farmaci.
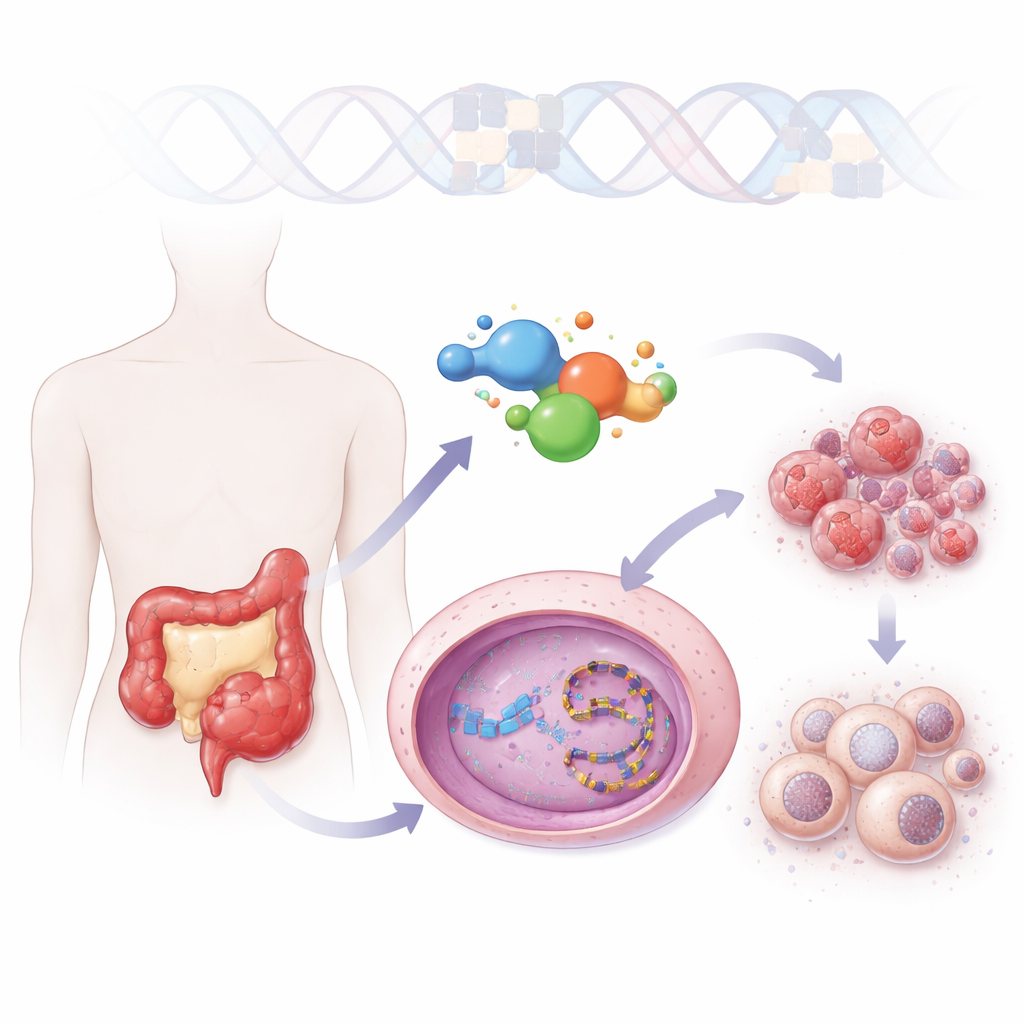
Una nuova lettura di una famiglia di farmaci nota
I medici usano già un farmaco chiamato irinotecan per il carcinoma colorettale, ma questo deve essere convertito all’interno dell’organismo in una forma attiva che ha scarsa solubilità e viene rapidamente inattivata. ZBH-01 è costruito sullo stesso nucleo chimico di base ma è ingegnerizzato per evitare questi limiti. Si dissolve molto meglio in acqua e agisce direttamente senza necessitare di attivazione metabolica. Nei test su più linee cellulari tumorali, ZBH-01 è risultato altrettanto potente quanto il miglior metabolita attivo dell’irinotecan e chiaramente più efficace dell’irinotecan stesso, anche a dosi inferiori. Modellizzazione strutturale ha mostrato che ZBH-01 si ancora allo stesso enzima che processa il DNA, la topoisomerasi I, ma stabilisce contatti aggiuntivi che mantengono l’enzima bloccato sul DNA, aumentando lo stress sul materiale genetico della cellula tumorale.
Colpire il luogo dove il tumore conserva la sua giovinezza
Le cellule tumorali spesso mantengono la capacità di dividersi indefinitamente sovraattivando la telomerasi, un enzima che protegge le estremità dei cromosomi. I ricercatori si sono concentrati sull’interruttore del DNA che controlla il componente principale della telomerasi, hTERT. Questa regione può ripiegarsi in forme a quattro filamenti insolite note come quadruplex G, che tendono a rallentare o bloccare l’attività genica. Utilizzando Risonanza magnetica nucleare ad alta risoluzione e altri metodi biofisici, il gruppo ha scoperto che ZBH-01 si sovrappone ordinatamente a un’estremità del quadruplex G di hTERT. Facendolo, stabilizza questa struttura ripiegata e rende più difficile l’accesso e il legame di potenti proteine che guidano la crescita, come MYC e SP1, impedendo l’attivazione del gene hTERT.
Forzare le cellule danneggiate in un ritiro permanente
Quando le cellule di carcinoma colorettale sono state esposte a ZBH-01, i loro profili di espressione genica sono cambiati drasticamente verso percorsi associati a danno al DNA, invecchiamento e arresto del ciclo cellulare. Il farmaco ha aumentato i marker di rottura del DNA e accorciato i telomeri, le cappette protettive sui cromosomi, più intensamente rispetto a composti di confronto. Allo stesso tempo, ha ridotto nettamente i livelli di hTERT e di diversi altri geni che normalmente spingono le cellule a continuare a dividersi. Di conseguenza, molte cellule trattate hanno assunto senescenza cellulare: uno stato in cui restano vive ma sono permanentemente escluse dal ciclo di divisione. Queste cellule senescenti hanno accumulato segni chimici e strutturali di nuclei «spenti» e hanno formato molte meno colonie nel tempo.
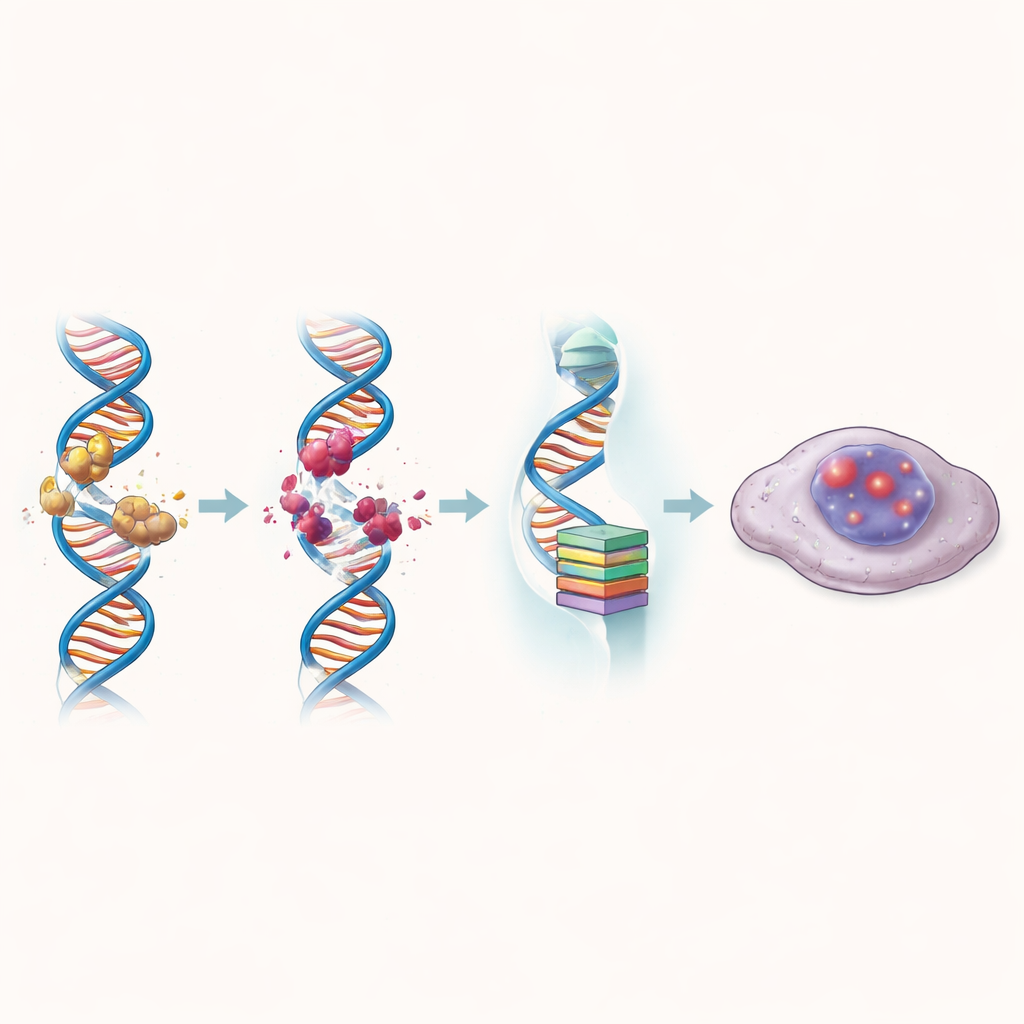
Superare la resistenza alla chemioterapia comune
Una prova cruciale per qualsiasi nuova terapia del carcinoma colorettale è se può aiutare quando i farmaci standard falliscono. Gli autori hanno esaminato cellule che erano diventate resistenti al cisplatino o al 5-fluorouracile, due agenti ampiamente usati. In entrambi i modelli resistenti, ZBH-01 è risultato molto più efficace dell’irinotecan o del suo metabolita attivo, riducendo la dose necessaria per frenare la crescita fino a decine di volte. In combinazione con cisplatino o 5-fluorouracile a concentrazioni scelte con cura, ZBH-01 ha agito in modo sinergico: insieme, i farmaci hanno ucciso le cellule resistenti più efficacemente di quanto potesse fare ciascuno da solo. La molecola a doppia azione ha anche ridotto l’attività di diversi geni che aiutano le cellule a espellere i farmaci o a riparare i danni indotti dalla chemioterapia, suggerendo che potrebbe attenuare più strategie di resistenza contemporaneamente.
Cosa potrebbe significare per i trattamenti futuri
Unendo danno al DNA e soppressione della telomerasi in una singola molecola ben caratterizzata, ZBH-01 offre un modello per farmaci oncologici di nuova generazione che affrontano la sopravvivenza tumorale da più angolazioni. Nei modelli di laboratorio, questa strategia non solo ha rallentato la crescita cellulare ma ha spinto le cellule tumorali verso una senescenza irreversibile e ha ripristinato la sensibilità ad altre chemioterapie. Pur restando molto lavoro da fare — compresi studi sulla sicurezza e test su animali e su esseri umani — la ricerca suggerisce che farmaci a doppio bersaglio progettati con attenzione potrebbero aiutare a superare l’adattabilità che rende il carcinoma colorettale così difficile da trattare.
Citazione: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
Parole chiave: carcinoma colorettale, chemi-resistenza, telomerasi, danno al DNA, terapia mirata