Clear Sky Science · ar
الاستهداف المزدوج للإنزيم توبوأيزوميراز I وأرباعيات الجوانين في الحمض النووي يعزز الشيخوخة الخلوية والحساسية للعلاج الكيميائي في سرطان القولون والمستقيم
لماذا تهم هذه الاستراتيجية الجديدة للسرطان
كثير من المصابين بسرطان القولون والمستقيم يتوقفون في نهاية المطاف عن الاستجابة للعلاج الكيميائي القياسي، ما يسمح للأورام بالنمو رغم المعالجات المكثفة. تصف هذه الدراسة مرشح دوائي جديداً يُدعى ZBH-01، مصمّمًا لمهاجمة خلايا السرطان على جبهتين حاسمتين في وقت واحد: إحداث ضرر في حمضها النووي وإيقاف محرك رئيسي لعدم الشيخوخة الخلوية. بدمج هذين الفعلين في جزيء واحد أكثر قابلية للذوبان، تقدم الدراسة مسارًا محتملاً لجعل الأورام العنيدة المقاومة للأدوية عرضة للعلاج مرة أخرى.
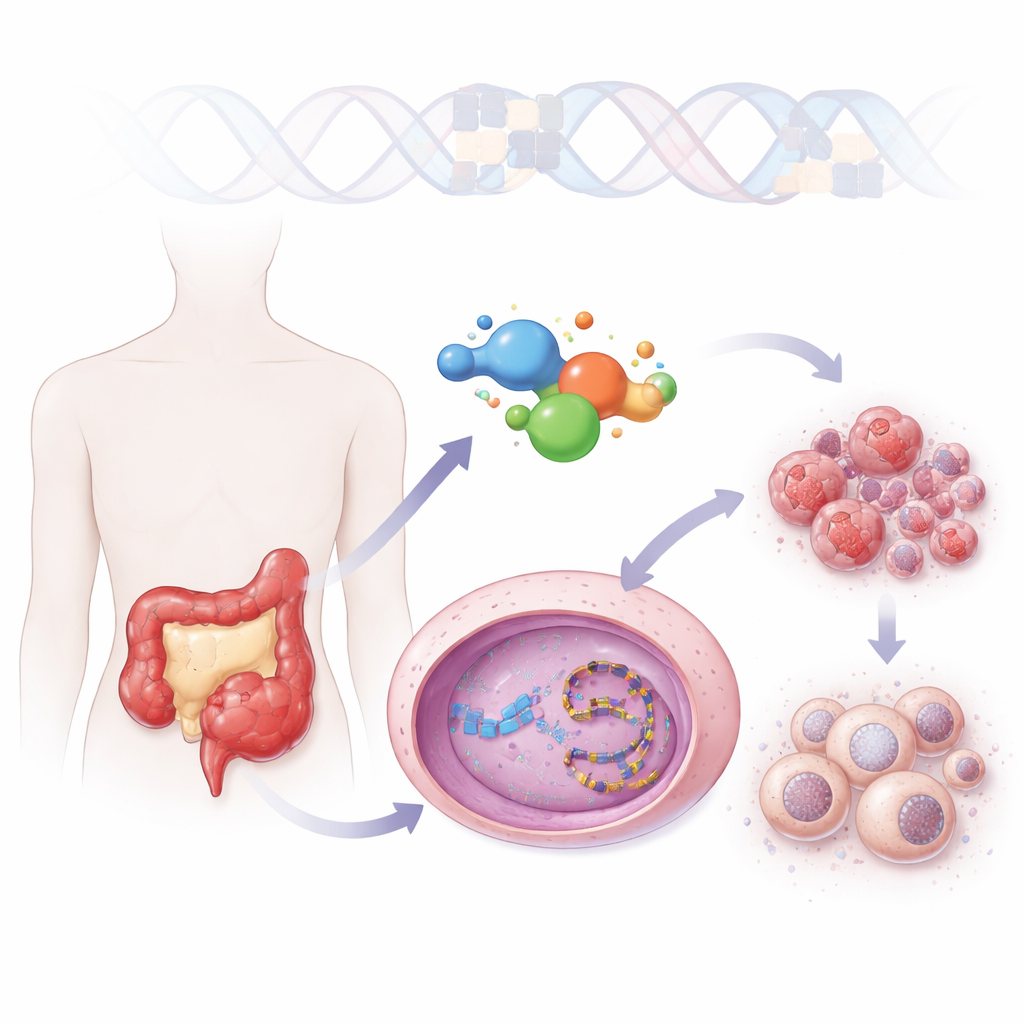
نظرة جديدة على عائلة أدوية قديمة للسرطان
الأطباء يستخدمون بالفعل دواءً يسمى إيرينوتيكان لعلاج سرطان القولون والمستقيم، لكنه يحتاج لأن يتحول داخل الجسم إلى شكل نشط ضعيف الذوبان ويتعطل سريعًا. بني ZBH-01 على نفس الهيكل الكيميائي الأساسي لكنه مُهندَس لتفادي هذه العيوب. يذوب بشكل أفضل بكثير في الماء ويعمل مباشرة دون الحاجة إلى تفعيل أيضي. في اختبارات عبر خطوط خلايا سرطانية متعددة، كان ZBH-01 بنفس قوة أنشط ناتج أيضي معروف للإيرينوتيكان وبوضوح أقوى من الإيرينوتيكان نفسه، حتى بجرعات أقل. أظهرت نمذجة البنية أن ZBH-01 يلتقط نفس إنزيم معالجة الحمض النووي، توبوأيزوميراز I، لكنه يشكل اتصالات إضافية تثبّت الإنزيم عالقًا على الحمض النووي، مما يزيد الضغط على المادة الوراثية للخلية السرطانية.
الضرب حيث تحافظ الخلايا السرطانية على شبابها
تحافظ الخلايا السرطانية غالبًا على قدرتها على الانقسام إلى ما لا نهاية من خلال فرط تفعيل تيلوميراز، الإنزيم الذي يحمي نهايات الكروموسومات. ركز الباحثون على "مفتاح" الحمض النووي الذي يتحكم بالمكوّن الرئيسي للتيلوميراز، hTERT. يمكن أن تطوى هذه المنطقة إلى أشكال رباعية السلاسل غير عادية تُعرف بأرباعيات الجوانين (G-quadruplexes)، والتي تميل إلى إبطاء أو تعطيل نشاط الجين. باستخدام مطيافية الرنين المغناطيسي النووي عالية الدقة وطرق فيزيوكيميائية أخرى، وجد الفريق أن ZBH-01 يتراص أنيقًا على أحد طرفي أرباعية الجوانين الخاصة بـ hTERT. بفعل ذلك، يُثبّت هذا الطيّ ويجعل من الأصعب على بروتينات قوية دافعة للنمو مثل MYC وSP1 أن ترتبط وتفعّل جين hTERT.
إجبار الخلايا المتضررة على التقاعد الدائم
عندما تعرضت خلايا سرطان القولون والمستقيم لـ ZBH-01، تحوّلت أنماط نشاط الجينات لديها بشكل كبير نحو مسارات مرتبطة بضرر الحمض النووي والشيخوخة وتوقّف دورة الخلية. زاد الدواء علامات انقسام الحمض النووي وقصر التيلوميرات — الأغطية الوقائية على الكروموسومات — بشكل أقوى من المركبات المقارنة. في الوقت نفسه خفّض بشدة مستويات hTERT والعديد من الجينات الأخرى التي تدفع الخلايا عادة للاستمرار في الانقسام. ونتيجة لذلك، دخلت العديد من الخلايا المعالجة في الشيخوخة الخلوية: حالة تبقى فيها الخلايا حية لكنها مقفولة نهائيًا خارج دورة الانقسام. تراكمت لدى هذه الخلايا الشيخوخة معالم كيميائية وبنيوية لنوى "مغلقة" وشكلت مستعمرات أقل بكثير مع مرور الوقت.
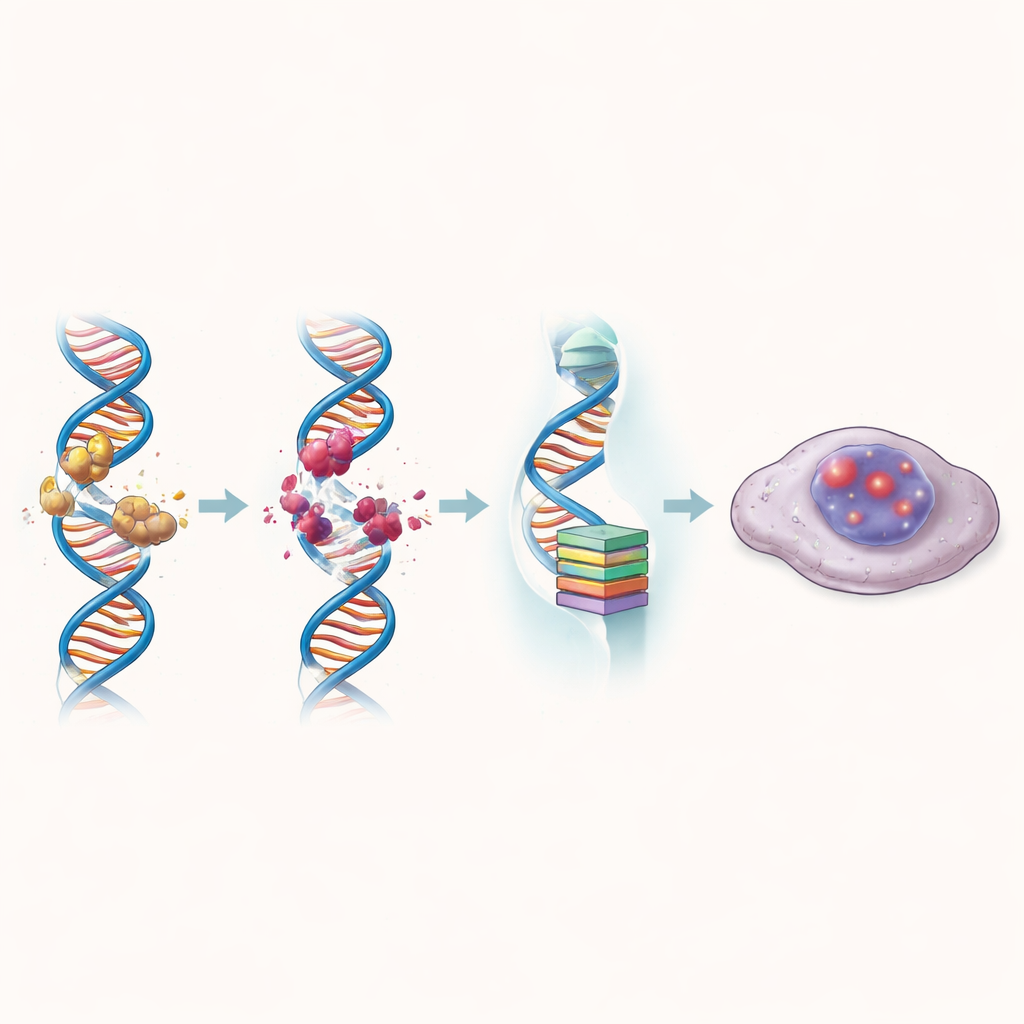
التغلب على المقاومة للعلاج الكيميائي الشائع
اختبارٌ أساسي لأي علاج جديد لسرطان القولون والمستقيم هو ما إذا كان يمكن أن يساعد عندما تفشل الأدوية القياسية. فحص المؤلفون خلايا أصبحت مقاومة للسيزبلاتين أو 5-فلورويوراسيل، وهما عاملان مستخدمان على نطاق واسع. في كلا النموذجين المقاومين، كان ZBH-01 أكثر فعالية بكثير من الإيرينوتيكان أو ناتجه النشط، مما خفّض الجرعة المطلوبة لكبح النمو بمقدار يتراوح حتى عشرات المرات. عند دمجه مع السيزبلاتين أو 5-فلورويوراسيل بتركيزات مختارة بعناية، عمل ZBH-01 بتآزر: معًا، قتلت الأدوية الخلايا المقاومة بكفاءة أكثر مما يستطيع أي منها بمفرده. كما قلّل الجزيء مزدوج الفعل نشاط عدة جينات تساعد الخلايا على ضخ الأدوية خارجها أو إصلاح الضرر الناتج عن العلاج الكيميائي، مما يوحي بأنه قد يعطّل عدة حيل مقاومة في آن واحد.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
بجمعه بين إتلاف الحمض النووي وكبح التيلوميراز في جزيء واحد حسن السلوك، يقدم ZBH-01 نموذجًا أوليًا لأدوية السرطان من الجيل التالي التي تواجه بقاء الورم من أكثر من زاوية واحدة. في نماذج مخبرية، لم تبطئ هذه الاستراتيجية نمو الخلايا فحسب، بل دفعت الخلايا السرطانية إلى الشيخوخة غير القابلة للعكس وأعادت الحساسية لعلاجات كيميائية أخرى. وبينما لا يزال هناك عمل كثير مطلوب — بما في ذلك دراسات السلامة والاختبارات على الحيوانات والبشر — تشير الأبحاث إلى أن الأدوية مزدوجة الاستهداف المصممة بعناية قد تساعد في التفوق على التكيّف الذي يجعل سرطان القولون والمستقيم صعب العلاج.
الاستشهاد: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
الكلمات المفتاحية: سرطان القولون والمستقيم, المقاومة للعلاج الكيميائي, تيلوميراز, ضرر الحمض النووي, العلاج الموجه