Clear Sky Science · ru
Двойное нацеливание на топоизомеразу I и ДНК G-квадруплексы усиливает сенесценцию и хемочувствительность при колоректальном раке
Почему эта новая стратегия в онкологии важна
У многих пациентов с колоректальным раком со временем развиваются резистентность к стандартной химиотерапии — опухоли продолжают расти вопреки агрессивному лечению. В этом исследовании описан новый кандидат в препараты, названный ZBH-01, который нацелен на раковые клетки сразу по двум критическим направлениям: он повреждает их ДНК и одновременно подавляет ключевой механизм их «бессмертия». Объединив эти эффекты в одной более растворимой молекуле, работа предлагает потенциальный способ снова сделать упрямые, лекарственно-резистентные опухоли уязвимыми.
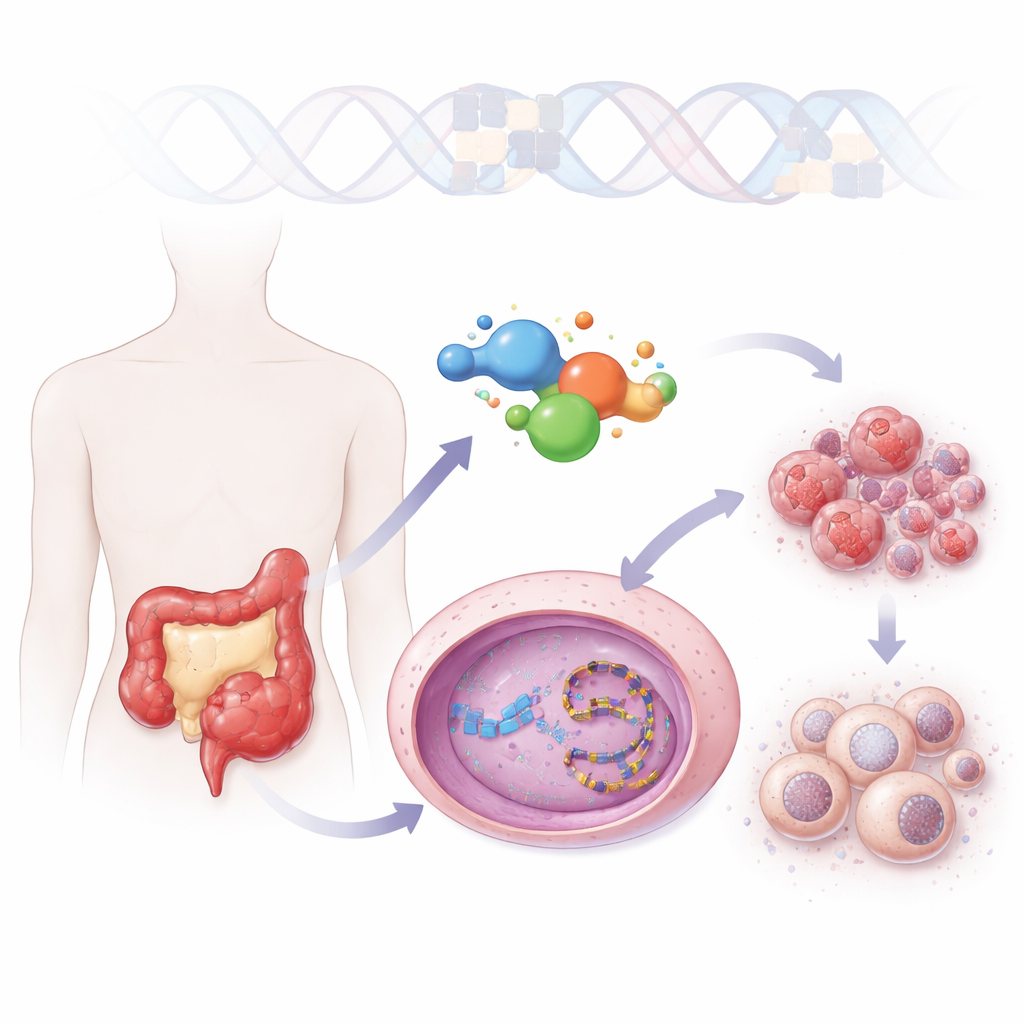
Новый взгляд на старое семейство противораковых препаратов
Врачи уже применяют препарат иринотекан при колоректальном раке, но он должен превращаться в организме в активную форму, которая плохо растворима и быстро инактивируется. ZBH-01 создан на той же базовой химической «раме», но сконструирован так, чтобы избежать этих недостатков. Он гораздо лучше растворяется в воде и действует напрямую, без необходимости метаболической активации. В испытаниях на множестве раковых клеточных линий ZBH-01 оказался таким же мощным, как лучший из известных метаболитов иринотекана, и явно сильнее самого иринотекана, даже при более низких дозах. Структурное моделирование показало, что ZBH-01 захватывает ту же ферментную мишень — топоизомеразу I — но образует дополнительные контакты, стабилизирующие фермент, застрявший на ДНК, повышая нагрузку на генетический материал раковой клетки.
Атака на то, что обеспечивает молодость опухоли
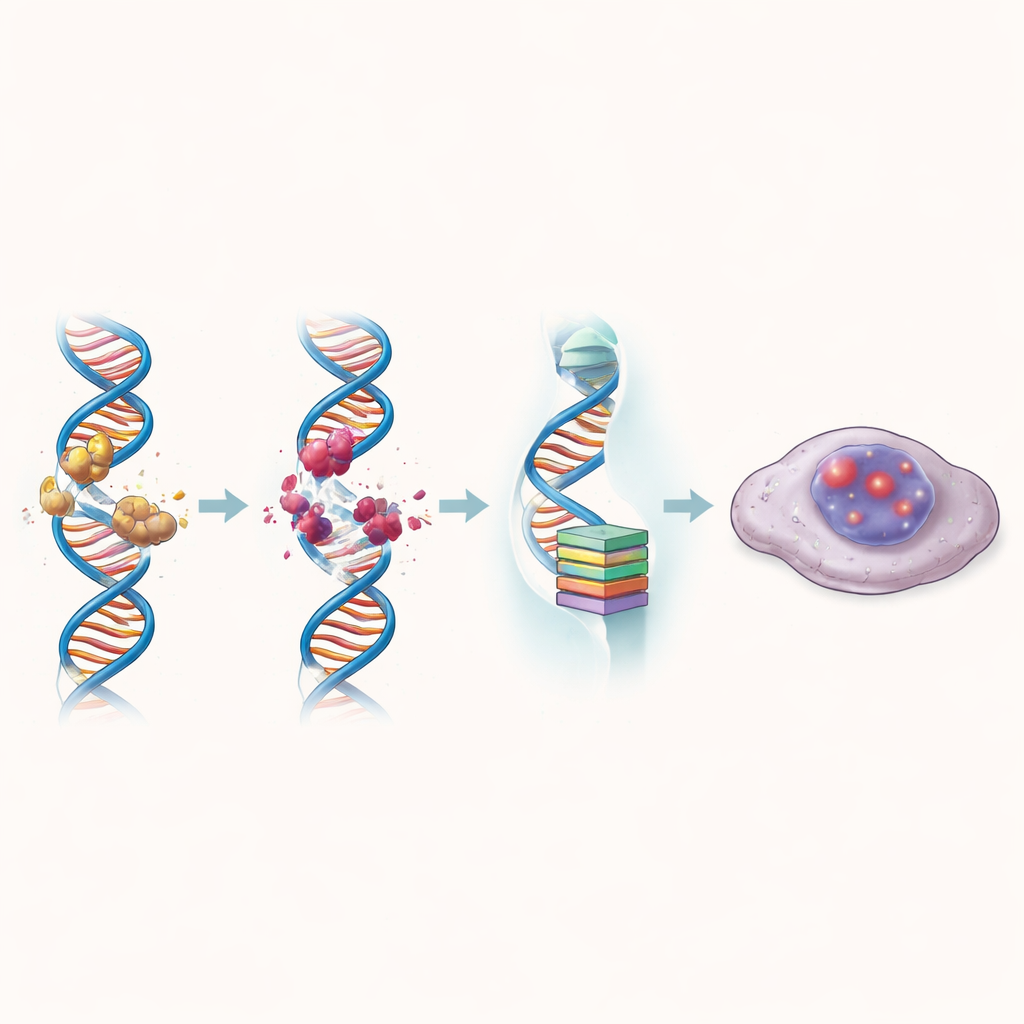
Раковые клетки часто сохраняют способность бесконечно делиться за счёт гиперактивности теломеразы — фермента, защищающего концы хромосом. Исследователи сосредоточились на ДНК‑«переключателе», контролирующем главный компонент теломеразы — hTERT. Этот участок может сворачиваться в необычные четырёхцепочные структуры, известные как G‑квадруплексы, которые склонны замедлять или блокировать активность гена. С помощью высокоразрешающей ЯМР‑спектроскопии и других биофизических методов команда обнаружила, что ZBH-01 аккуратно штабелируется на одном из концов G‑квадруплекса hTERT. Тем самым он стабилизирует эту свернутую структуру и затрудняет связывание мощных протеиновых активаторов роста, таких как MYC и SP1, которые включают ген hTERT.
Вынуждение повреждённых клеток к постоянному «уходу на пенсию»
При обработке колоректальных раковых клеток ZBH-01 их профиль экспрессии генов резко сдвигался в сторону путей, связанных с повреждением ДНК, старением и остановкой клеточного цикла. Препарат усиливал маркеры разрывов ДНК и укорачивал теломеры — защитные наконечники хромосом — сильнее, чем сравниваемые соединения. В то же время он заметно снижал уровни hTERT и нескольких других генов, которые обычно стимулируют непрерывное деление клеток. В результате многие обработанные клетки входили в состояние клеточной сенесценции: состояние, при котором они остаются живыми, но навсегда выпадают из цикла деления. Эти сенесцентные клетки накапливали химические и структурные признаки «запущенных» ядер и со временем образовывали значительно меньше колоний.
Преодоление резистентности к обычной химиотерапии
Ключевым испытанием для любой новой терапии колоректального рака является её эффективность там, где стандартные препараты бессильны. Авторы изучали клетки, ставшие резистентными к цисплатину или 5‑фторурацилу, двум широко используемым средствам. В обеих моделях устойчивости ZBH-01 был значительно эффективнее иринотекана и его активного метаболита, сокращая необходимую дозу для подавления роста в десятки раз. При комбинировании с цисплатином или 5‑фторурацилом в тщательно подобранных концентрациях ZBH-01 действовал синергически: вместе препараты убивали резистентные клетки эффективнее, чем по отдельности. Двухфункциональная молекула также снижала активность нескольких генов, помогающих клеткам выкачивать препараты или ремонтировать повреждения, вызванные химиотерапией, намекая на то, что она может ослаблять несколько механизмов резистентности одновременно.
Что это может означать для будущих методов лечения
Объединяя повреждение ДНК и подавление теломеразы в одной хорошо ведущеся молекуле, ZBH-01 предлагает план для препаратов следующего поколения, которые атакуют выживание опухоли сразу с нескольких сторон. В лабораторных моделях эта стратегия не только замедляла рост клеток, но и переводила раковые клетки в необратимую сенесценцию и восстанавливала чувствительность к другим химиотерапиям. Хотя предстоит ещё много работы — включая исследования безопасности и испытания на животных и людях — исследование указывает на то, что продуманно спроектированные препараты с двойной мишенью могут помочь перехитрить адаптивность, делающую колоректальный рак таким трудным для лечения.
Цитирование: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
Ключевые слова: колоректальный рак, хеморезистентность, теломераза, повреждение ДНК, таргетная терапия