Clear Sky Science · he
טִיוּחַ כפול של טופואיזומרזָה I ו-גְ׳י-קוואדרופלֶקס DNA מחריף זִקנה ותְחִשׁוּב לכימותרפיה בסרטן המעי הגס
מדוע אסטרטגיה חדשה זו חשובה
רבים מהמטופלים בסרטן המעי הגס מפסיקים בסופו של דבר להגיב לכימותרפיה הסטנדרטית, מה שמאפשר לגידולים לגדול אף על פי טיפול אגרסיבי. המחקר הזה מתאר מועמדת-תרופה חדשה בשם ZBH-01, העוצבה לתקוף את תאי הסרטן בשני חזיתות קריטיות בו־זמנית: היא פוגעת ב-DNA שלהם ומכה גם במנוע מרכזי של האלמוות שלהם. על ידי שילוב שתי הפעולות באותה מולקולה אחת, בעלת מסיסות משופרת, העבודה מציעה דרך פוטנציאלית להפוך גידולים עקשניים העמידים לתרופות לפגיעים שוב.
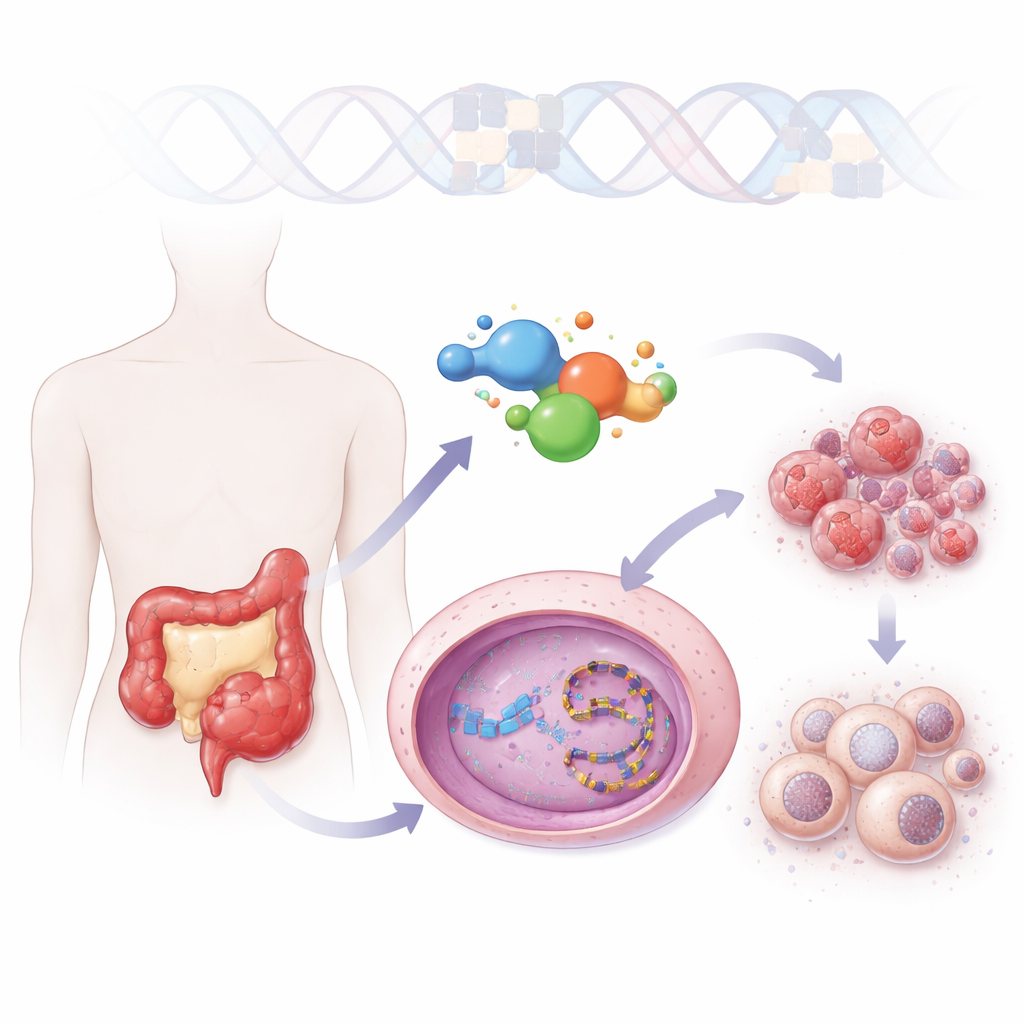
גישה חדשה למשפחת תרופות ותיקה
רופאים כבר משתמשים בתרופה שנקראת אירינוטקאן לטיפול בסרטן המעי הגס, אך היא דורשת המרה בתוך הגוף לצורתה הפעילה שהיא גרועה מסיסות ומהירה לאי-פעלה. ZBH-01 מבוססת על אותו שלד כימי מרכזי אך מהונדסת להימנע מפגמים אלה. היא מתמוססת טוב יותר מאוד במים ופועלת ישירות ללא צורך בהפעלה מטבולית. במבחנים על שורת תאי סרטן שונות, ZBH-01 הייתה בעלת עוצמה שווה לזו של מטבוליט האירינוטקאן הטוב ביותר וברורה חזקה יותר מאירינוטקאן עצמו, אפילו במינונים נמוכים יותר. דגמי מבנה הראו כי ZBH-01 נצמדת לאותו אנזים המעבד DNA, טופואיזומרזָה I, אך יוצרת מגעים נוספים שמייצבים את האנזים כשהוא תקוע על ה-DNA, מה שמגביר את הלחץ על החומר הגנטי של התא הסרטני.
פגיעה במקום שבו הסרטן שומר על נעוריו
תאי סרטן לעיתים שומרים על יכולתם להתחלק ללא הגבלה על ידי הפעלת יתר של הטלומראז, האנזים שמגן על קצוות הכרומוזומים. החוקרים התמקדו במתג ה-DNA ששולט ברכיב המרכזי של הטלומראז, hTERT. אזור זה יכול לקפל לצורות יוצאות דופן בעלות ארבעה גדילים הידועות כ-G-quadruplexes, הנוטות להאט או לחסום פעילות גנטית. באמצעות ספקטרוסקופיית NMR ברזולוציה גבוהה ושיטות ביופיזיקליות נוספות, הצוות מצא ש-ZBH-01 נערמת באופן מסודר על קצה אחד של ה-G-quadruplex של hTERT. בכך היא מייצבת את המבנה המוקפל והופכת את קשירתם של חלבונים בעלי כוח נהגי גדילה, כגון MYC ו-SP1, לקשה יותר ולמניעת הדלקת הגן hTERT.
הכנסת תאים ניזוקים לפרישה קבועה
כאשר תאי סרטן המעי הגס נחשפו ל-ZBH-01, דפוסי הפעילות הגנטית שלהם השתנו באופן דרמטי לכיוון מסלולים הקשורים לנזק ל-DNA, הזדקנות ועצירת מחזור התא. התרופה העלתה סימנים של DNA שבור וקיצרה טלומרים, הכובעים המגנים על הכרומוזומים, בעוצמה חזקה יותר מאשר תרכובות להשוואה. במקביל היא הורידה חזק את רמות hTERT וכמה גנים נוספים שמניעים בדרך כלל המשך חלוקה. כתוצאה מכך, תאים מטופלים רבים נכנסו לסנֵסֶנס (senescence): מצב שבו הם נשארים חיים אך ננעלים לצמיתות מחזור החלוקה. תאים סנֵסנטים אלה צברו סימנים כימיים ומבניים של גרעינים "כבים" והקימו מספר קטן בהרבה של מושבות לאורך זמן.
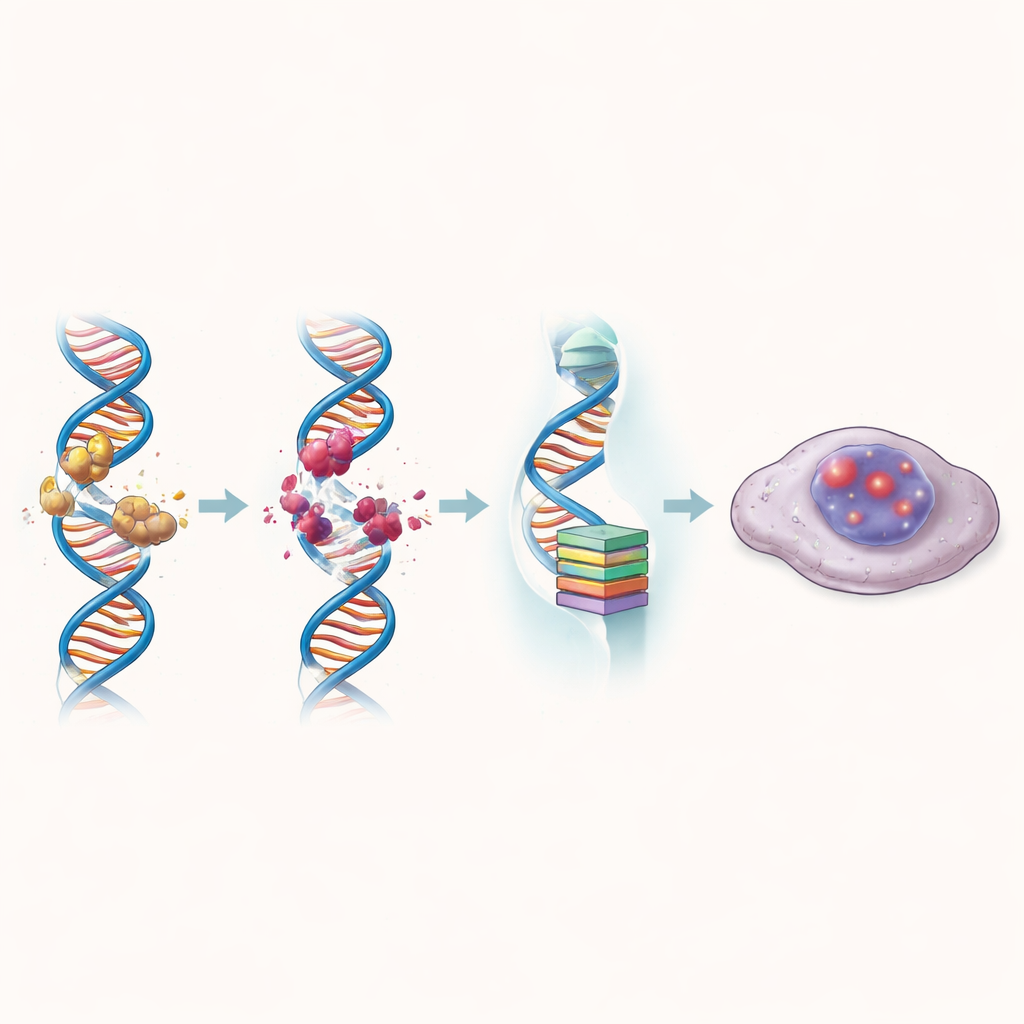
עקיפת עמידות לכימותרפיה נפוצה
מבחן מרכזי לכל טיפול חדש בסרטן המעי הגס הוא האם הוא יכול לסייע כאשר תרופות תקניות נכשלות. המחברים בחנו תאים שהפכו לעמידים לקיספלָטין או ל-5‑פלואורואורציל, שני סוכנים בשימוש נרחב. בשני המודלים העמידים, ZBH-01 הייתה יעילה בהרבה מאירינוטקאן או ממטבוליטו הפעיל, והקטינה את המינון הנדרש לעיקור הצמיחה בעשרות מונים. כאשר שולבה עם קיספלָטין או 5‑פלואורואורציל בריכוזים שנבחרו בקפידה, ZBH-01 פעלה בצורה סינרגטית: יחד, התרופות הרגו תאים עמידים ביעילות רבה יותר מכל אחת מהן בנפרד. המולקולה בעלת הפעולה הכפולה גם הפחיתה את הפעילות של מספר גנים שעוזרים לתאים לשאוב החוצה תרופות או לתקן נזקים שגרמה הכימותרפיה, רמיזה לכך שהיא עשויה לטשטש מספר מהלכי עמידות בבת אחת.
מה זה יכול להשפיע על טיפולים עתידיים
על ידי איחוד נזק ל-DNA ודיכוי טלומראז במולקולה אחת מתפקדת וטובה להתנהגות, ZBH-01 מציעה שרטוט לתרופות סרטניות בדור הבא שמתמודדות עם הישרדות הגידול מכמה זוויות. במודלים מעבדתיים, אסטרטגיה זו לא רק האטה את גדילת התאים אלא דחפה תאי סרטן לסנֵסנס בלתי הפיך והשיבה רגישות לכימותרפיות אחרות. בעוד שעבודת המשך רבה נדרשת — כולל מחקרים בטיחות, ניסויים בחיות ובאנשים — המחקר מצביע על כך שמולקולות דו-מטרתיות מעוצבות בקפידה עשויות לסייע לעקוף את הגמישות שעושה את סרטן המעי הגס כה קשה לטיפול.
ציטוט: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
מילות מפתח: סרטן המעי הגס, התנגדות לכימותרפיה, טלומראז, נזק ל-DNA, טיפול ממוקד