Clear Sky Science · nl
Dubbele targeting van topoisomerase I en DNA G-quadruplexen versterkt senescentie en chemosensitiviteit bij colorectale kanker
Waarom deze nieuwe kankerstrategie ertoe doet
Veel mensen met colorectale kanker verliezen na verloop van tijd hun reactie op de standaardchemotherapie, waardoor tumoren blijven groeien ondanks agressieve behandeling. Deze studie beschrijft een nieuwe medicijnkandidaat, ZBH-01, ontworpen om kankercellen gelijktijdig op twee cruciale fronten aan te vallen: het beschadigt hun DNA en schakelt tegelijk een sleutelmotor van hun onsterfelijkheid uit. Door deze acties te combineren in één beter oplosbaar molecuul, biedt het werk een mogelijke manier om hardnekkige, medicijnresistente tumoren weer kwetsbaar te maken.
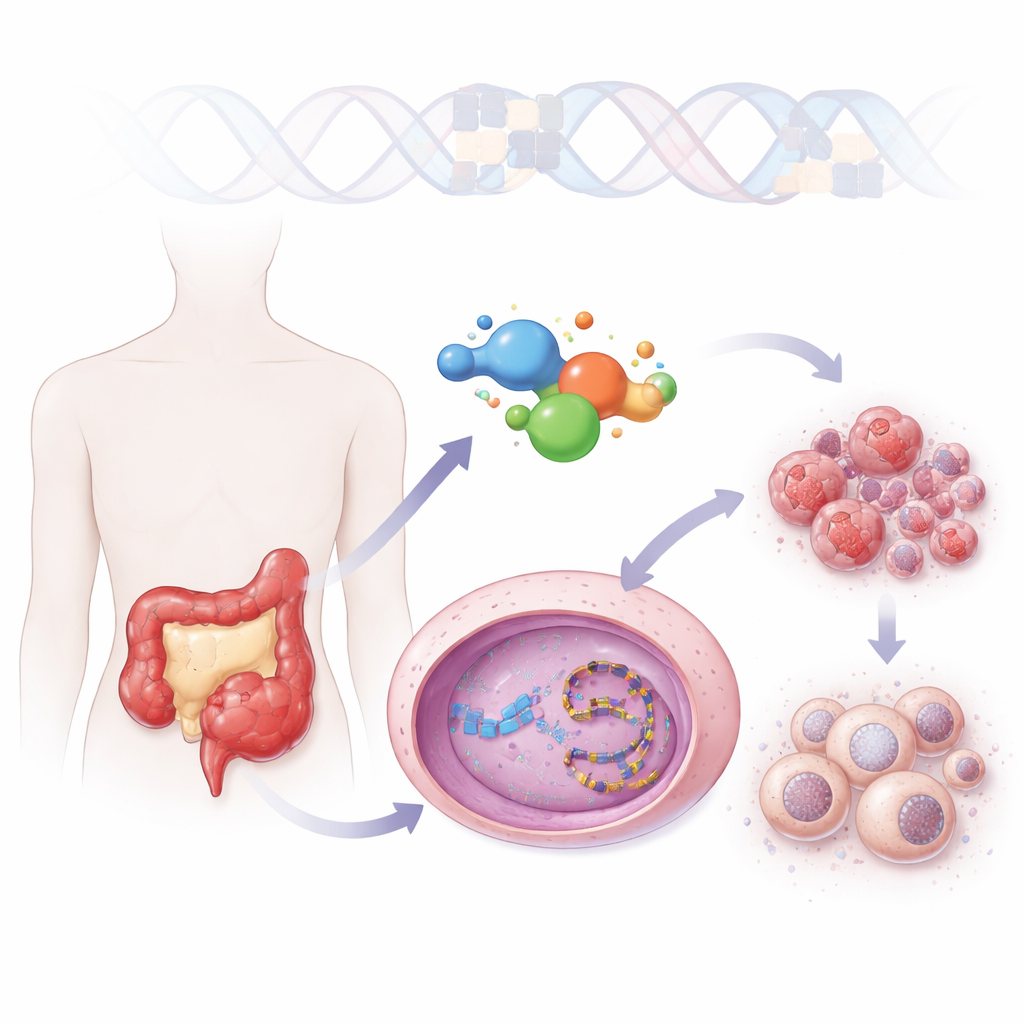
Een frisse blik op een oude geneesmiddelengroep
Artsen gebruiken al een middel genaamd irinotecan bij colorectale kanker, maar dit moet in het lichaam worden omgezet in een actieve vorm die slecht oplosbaar is en snel wordt geïnactiveerd. ZBH-01 is gebouwd op hetzelfde chemische basisskelet maar is zo ontworpen dat het deze nadelen vermijdt. Het lost veel beter op in water en werkt direct zonder metabolische activatie. In tests over meerdere kankercellijnen was ZBH-01 even krachtig als het beste bestaande irinotecanmetaboliet en duidelijk sterker dan irinotecan zelf, zelfs bij lagere doses. Structurele modellering toonde aan dat ZBH-01 zich vastklampt aan hetzelfde DNA-verwerkende enzym, topoisomerase I, maar extra contacten vormt die het enzym op DNA stabiliseren, waardoor de stress op het genetisch materiaal van de kankercel toeneemt.
Raken waar de kanker zijn jeugd bewaart
Kankercellen behouden vaak hun deelcapaciteit door telomerase te overactiveren, een enzym dat de uiteinden van chromosomen beschermt. De onderzoekers richtten zich op de DNA-"schakelaar" die het belangrijkste component van telomerase, hTERT, regelt. Dit gebied kan zich vouwen in ongewone vierstrengige structuren die bekendstaan als G-quadruplexen, die de genactiviteit vertragen of blokkeren. Met hoogresolutie NMR en andere biofysische methoden vonden de onderzoekers dat ZBH-01 netjes op één uiteinde van het hTERT G-quadruplex stapelt. Hierdoor stabiliseert het deze gevouwen structuur en bemoeilijkt het de binding van krachtige groeidrivers zoals MYC en SP1, waardoor het aanzetten van het hTERT-gen wordt tegengehouden.
Beschadigde cellen gedwongen tot permanente uittreding
Wanneer colorectale kankercellen werden blootgesteld aan ZBH-01, verschoof hun genactiviteitsprofiel sterk richting routes die verband houden met DNA-schade, veroudering en celdelingstop. Het middel verhoogde markers van gebroken DNA en verkortte telomeren — de beschermkappen van chromosomen — sterker dan vergelijkingsverbindingen. Tegelijkertijd verlaagde het sterk de niveaus van hTERT en verschillende andere genen die normaal gesproken cellen aanzetten tot blijven delen. Als gevolg daarvan traden veel behandelde cellen in cellulair senescentie: een toestand waarin ze wel leven maar permanent uitgesloten zijn van de delingscyclus. Deze senescente cellen bouwden chemische en structurele kenmerken van "afgeschakelde" kernen op en vormden over tijd veel minder kolonies.
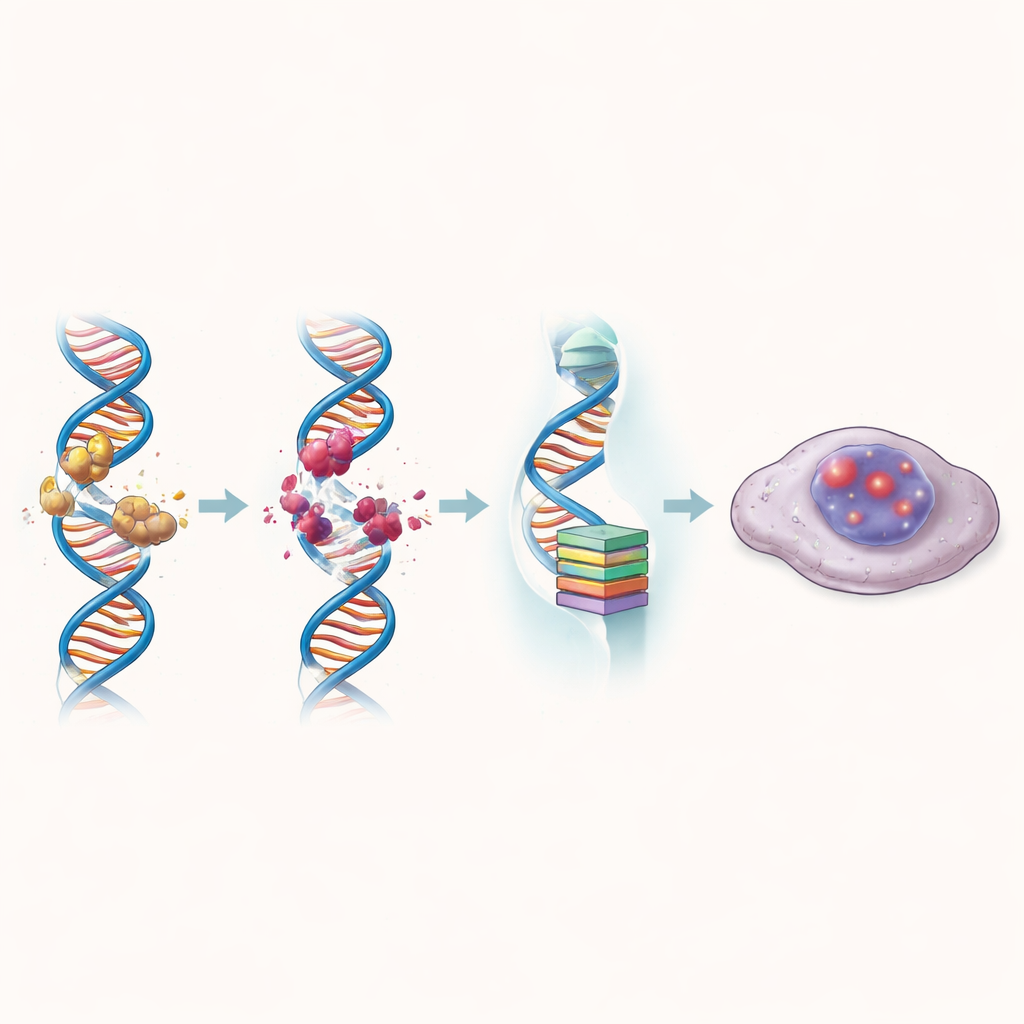
Het overwinnen van resistentie tegen veelgebruikte chemotherapie
Een cruciale test voor elke nieuwe behandeling van colorectale kanker is of ze kan helpen wanneer standaardmiddelen falen. De auteurs onderzochten cellen die resistent waren geworden tegen cisplatine of 5-fluorouracil, twee veelgebruikte middelen. In beide resistente modellen was ZBH-01 veel effectiever dan irinotecan of zijn actieve metaboliet, waarbij de benodigde dosis om groei te remmen tot tientallen keren werd verlaagd. In combinatie met cisplatine of 5-fluorouracil in zorgvuldig gekozen concentraties werkte ZBH-01 synergetisch: samen doodden de middelen resistente cellen efficiënter dan elk middel afzonderlijk. Het dubbelwerkende molecuul verminderde ook de activiteit van verschillende genen die cellen helpen medicijnen uit te pompen of chemotherapie-geïnduceerde schade te repareren, wat erop wijst dat het meerdere resistentiemechanismen tegelijk kan verzwakken.
Wat dit kan betekenen voor toekomstige behandelingen
Door DNA-schade en telomeraseonderdrukking te verenigen in één goed hanteerbaar molecuul, biedt ZBH-01 een blauwdruk voor geneesmiddelen van de volgende generatie die het tumortoevankelijkheid van meerdere kanten aanpakken. In laboratoriummodellen vertraagde deze strategie niet alleen de celgroei, maar duwde kankercellen ook in onomkeerbare senescentie en herstelde de gevoeligheid voor andere chemotherapieën. Hoewel er nog veel werk te doen is — inclusief veiligheidsonderzoeken en testen in dieren en mensen — suggereert het onderzoek dat doordacht ontworpen dubbelgerichte middelen kunnen helpen de aanpasbaarheid te slim af te zijn die colorectale kanker zo moeilijk behandelbaar maakt.
Bronvermelding: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
Trefwoorden: colorectale kanker, chemoresistentie, telomerase, DNA-schade, gerichte therapie