Clear Sky Science · sv
Dubbelriktad målning av topoisomeras I och DNA G‑quadruplexes förstärker senescens och kemosensitivitet vid kolorektal cancer
Varför denna nya cancerstrategi spelar roll
Många patienter med kolorektalcancer slutar så småningom svara på standardkemoterapi, vilket gör att tumörer växer trots aggressiv behandling. Denna studie beskriver en ny läkarkandidat, kallad ZBH‑01, som är utformad för att angripa cancerceller på två kritiska fronter samtidigt: den skadar deras DNA och stänger också av en nyckelmotor för deras odödlighet. Genom att kombinera dessa effekter i en enda, mer löslig molekyl erbjuder arbetet ett potentiellt sätt att göra envisa, läkemedelsresistenta tumörer sårbara igen.
En ny syn på en gammal läkemedelsfamilj
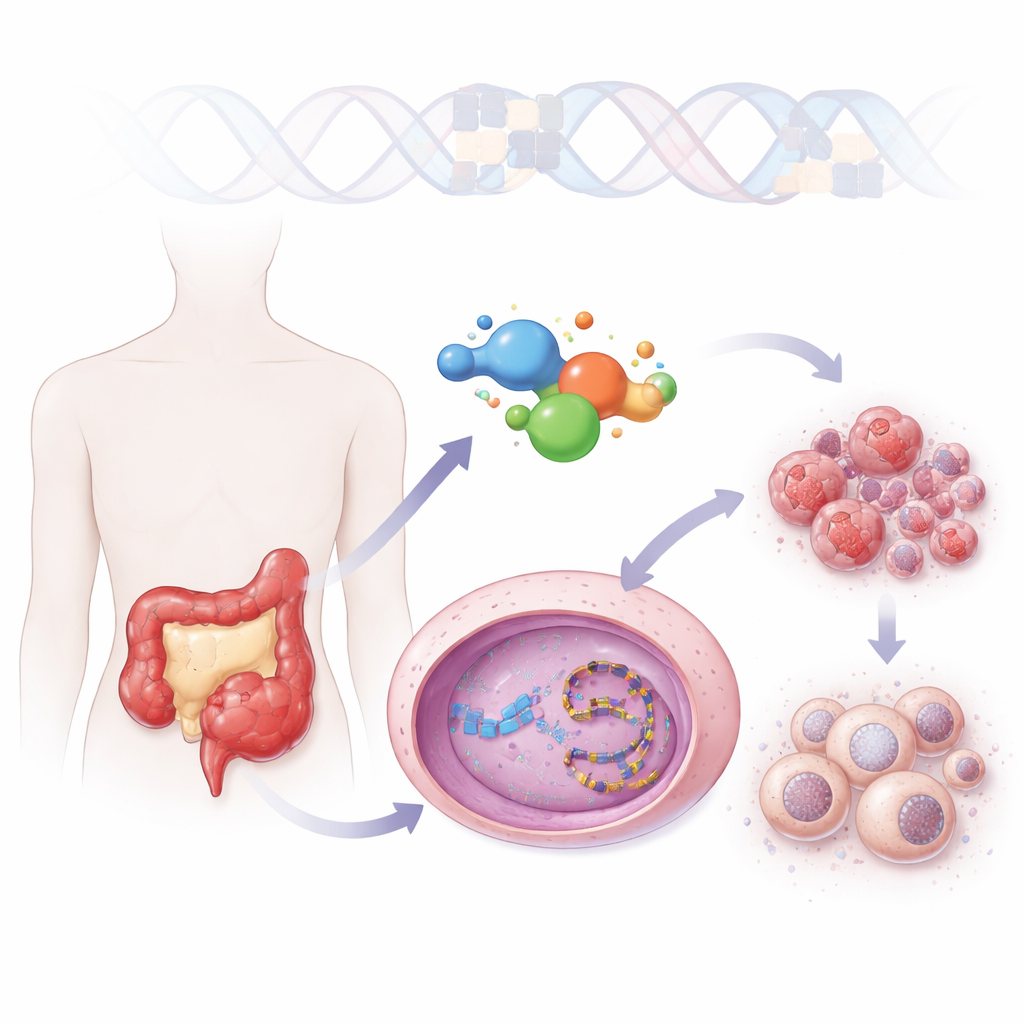
Läkare använder redan ett läkemedel kallat irinotekan för kolorektalcancer, men det måste omvandlas i kroppen till en aktiv form som är dåligt löslig och snabbt inaktiveras. ZBH‑01 bygger på samma kärnkemiska stomme men är konstruerad för att undvika dessa nackdelar. Den löser sig betydligt bättre i vatten och verkar direkt utan behov av metabolisk aktivering. I tester över flera cancercellinjer var ZBH‑01 lika potent som den bästa befintliga irinotekanmetaboliten och tydligt starkare än irinotekan självt, även vid lägre doser. Strukturell modellering visade att ZBH‑01 klämmer fast vid samma DNA‑bearbetande enzym, topoisomeras I, men bildar extra kontakter som stabiliserar enzymet fast på DNA, vilket ökar påfrestningen på cancercellens genetiska material.
Att slå mot varifrån cancern håller sin ungdom
Cancerceller upprätthåller ofta sin förmåga att dela sig obegränsat genom att överaktivera telomeras, ett enzym som skyddar kromosomernas ändar. Forskarna fokuserade på DNA‑”strömbrytaren” som reglerar telomerasens huvudkomponent, hTERT. Detta område kan veckas till ovanliga fyrsträngade former kända som G‑quadruplexes, vilka tenderar att bromsa eller blockera genaktivitet. Genom högupplöst NMR och andra biofysiska metoder fann teamet att ZBH‑01 staplas prydligt på ena änden av hTERT‑G‑quadruplexet. Genom detta stabiliserar den den veckade strukturen och försvårar för starka tillväxtdrivande proteiner, såsom MYC och SP1, att binda och slå på hTERT‑genen.
Tvinga skadade celler in i permanent pension
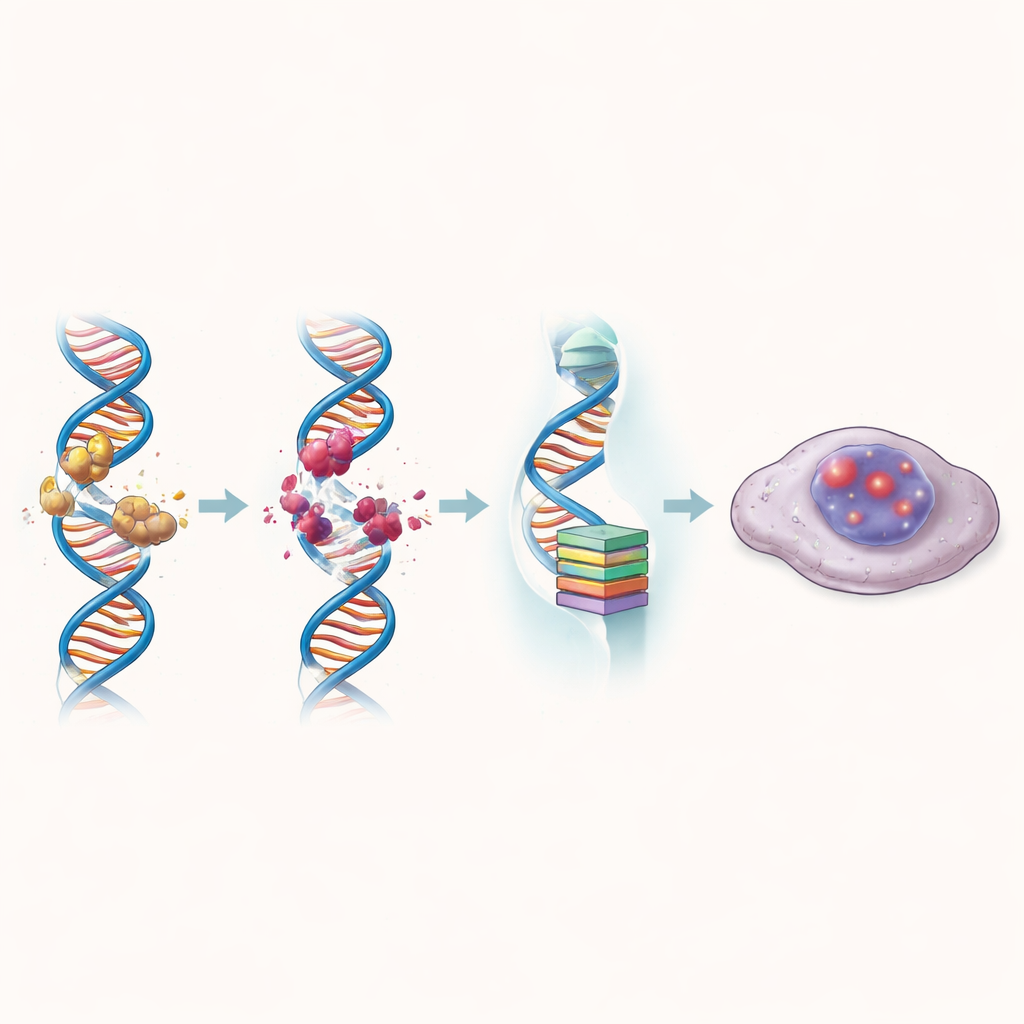
När kolorektala cancerceller exponerades för ZBH‑01 skiftade deras genaktivitetsmönster dramatiskt mot banor kopplade till DNA‑skada, åldrande och cellcykelstopp. Läkemedlet ökade markörer för brutet DNA och förkortade telomererna, kromosomernas skyddande hättor, starkare än jämförelseföreningar. Samtidigt sänktes nivåerna av hTERT och flera andra gener som normalt driver celler att fortsätta dela sig kraftigt. Som ett resultat gick många behandlade celler in i cellulär senescens: ett tillstånd där de förblir levande men permanent utestängda från delningscykeln. Dessa senescenta celler samlade kemiska och strukturella kännetecken för ”avstängda” kärnor och bildade betydligt färre kolonier över tid.
Att övervinna resistens mot vanlig kemoterapi
Ett viktigt test för varje ny terapi mot kolorektalcancer är om den kan hjälpa när standardläkemedel misslyckas. Författarna undersökte celler som blivit resistenta mot cisplatin eller 5‑fluorouracil, två allmänt använda medel. I båda resistenta modellerna var ZBH‑01 mycket mer effektivt än irinotekan eller dess aktiva metabolit och minskade den dos som behövdes för att hämma tillväxten med upp till tiotals gånger. När det kombinerades med cisplatin eller 5‑fluorouracil vid noggrant utvalda koncentrationer fungerade ZBH‑01 synergistiskt: tillsammans dödade läkemedlen resistenta celler mer effektivt än någon av dem ensam. Den dubbelverkande molekylen minskade också aktiviteten hos flera gener som hjälper celler att pumpa ut läkemedel eller reparera kemoterapiskadad vävnad, vilket antyder att den kan dämpa flera resistensstrategier samtidigt.
Vad detta kan innebära för framtida behandlingar
Genom att förena DNA‑skada och telomerasundertryck i en enda, välhanterad molekyl erbjuder ZBH‑01 en ritning för nästa generations cancerläkemedel som angriper tumöroverlevnad från mer än en vinkel. I laboratoriemodeller bromsade denna strategi inte bara celltillväxt utan förde också cancerceller in i irreversibel senescens och återställde känsligheten för andra kemoterapier. Även om mycket arbete återstår — inklusive säkerhetsstudier samt djur‑ och mänskliga prövningar — tyder forskningen på att genomtänkt designade dubbelriktade läkemedel kan hjälpa att överlista den anpassningsförmåga som gör kolorektalcancer så svårbehandlad.
Citering: Li, Y., Ji, D., Jia, Y. et al. Dual targeting of topoisomerase I and DNA G-quadruplexes enhances senescence and chemosensitivity in colorectal cancer. Commun Biol 9, 552 (2026). https://doi.org/10.1038/s42003-026-09801-w
Nyckelord: kolorektalcancer, kemoresistens, telomeras, DNA‑skada, riktad terapi