Clear Sky Science · zh
多组学分析揭示 STIL 在李-弗劳门尼综合征与骨肉瘤中的关键作用
当遗传风险遇上儿童骨癌
有些家族传承的并不仅仅是眼睛颜色或身高——他们还继承了更高的癌症风险。其中一种情况,李-弗劳门尼综合征,会显著提高患骨肉瘤的几率。骨肉瘤是一种罕见但侵袭性强的骨肿瘤,常在儿童和青少年中发生。本研究提出了一个紧迫的问题:除了著名的“守护者”基因 TP53 之外,还有哪些分子将这种遗传风险转化为增长迅速、难以治疗的骨肿瘤?它们是否可能成为新的治疗靶点?
连接遗传风险与肿瘤生长的隐秘桥梁
研究者将注意力集中在李-弗劳门尼综合征上,该病患者自出生起每个细胞中就携带一份有缺陷的 TP53 拷贝。与普通人群相比,这类人群发生骨肉瘤的概率高出数百倍。研究团队利用大量患者组织和细胞数据,扫描了数千个基因,寻找在李-弗劳门尼样本与骨肉瘤肿瘤中共有变化的基因。他们发现了一小组“桥接”基因,这些基因在两种情况下的活性都发生了改变,并集中在控制细胞分裂与染色体复制的过程上——这些核心步骤一旦紊乱,就能驱动癌症发生。
STIL 作为核心麻烦制造者浮出水面
通过应用多种机器学习方法,科学家们将这组桥接基因缩小到四个关键基因,并找到了一个突出者:名为 STIL 的基因。在骨肉瘤样本中,STIL 在已经转移的肿瘤中持续较高,且肿瘤中 STIL 水平较高的患者预后较差。通路分析将高表达的 STIL 与活跃的细胞周期和蛋白质降解联系起来,而低表达的 STIL 则与更强的免疫和炎症信号相关。这一模式提示 STIL 不仅帮助骨癌细胞分裂,还可能削弱机体对其的天然防御。
类干细胞群体与沉寂的免疫系统
为了确定 STIL 在肿瘤内部的作用位置,团队转向单细胞测序,该技术逐个细胞进行分析。他们绘制了来自骨肉瘤样本的十万多个细胞图谱,并识别出若干恶性细胞类型。STIL 在一类高度“类干”肿瘤细胞中尤为丰富,这些细胞位于发育轨迹的起始端——似乎为肿瘤的种子和维持来源。在这些细胞中,高 STIL 与促进自我更新的信号、激活破骨细胞(侵蚀骨骼)以及重塑周围免疫细胞的信号相关。富含 STIL 的肿瘤显示活性杀伤性 T 细胞和关键免疫激活分子减少,这种模式类似于“免疫沙漠”,即免疫系统无法有效识别或攻击肿瘤。
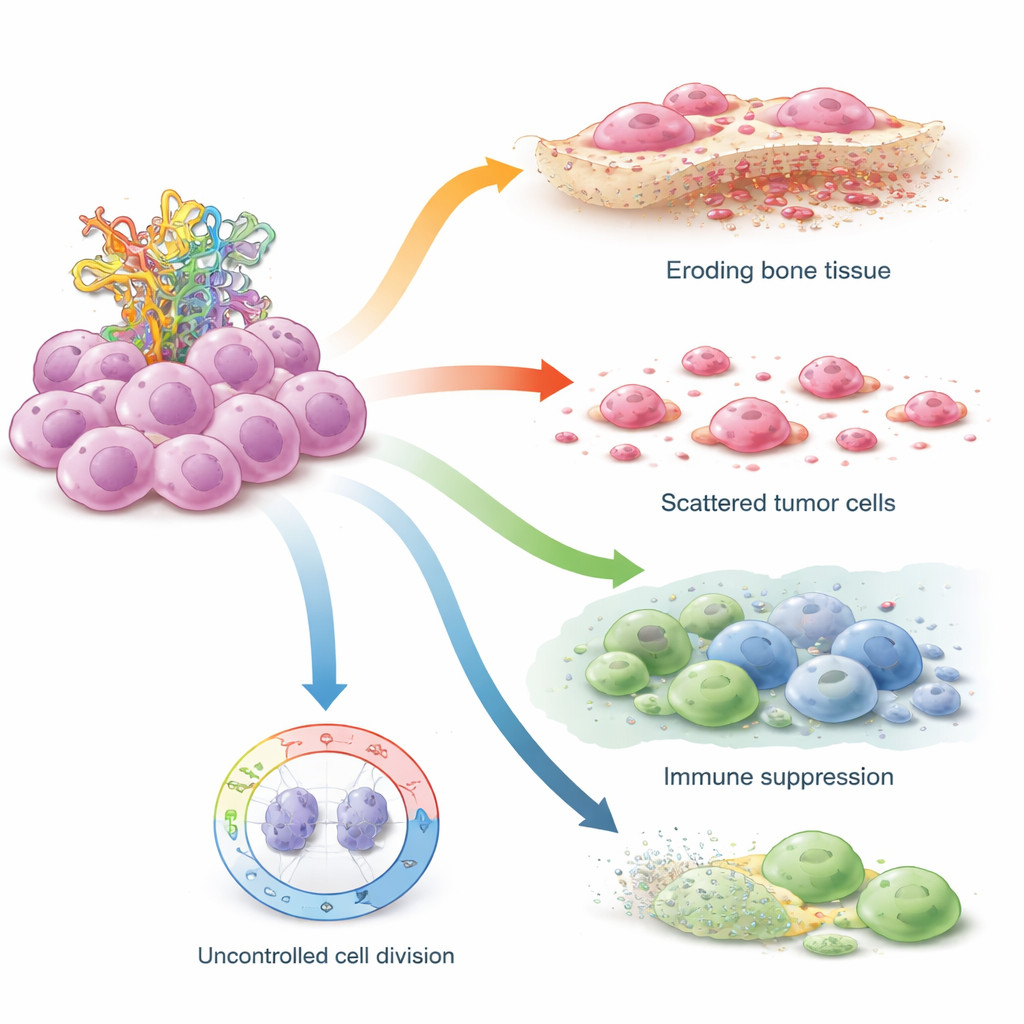
STIL 如何削弱细胞的安全制动
随后研究者在体外培养的骨肉瘤细胞系中直接测试了 STIL,比较了具有正常 TP53 的细胞与携带模拟李-弗劳门尼综合征的 TP53 突变细胞。当他们用小 RNA 分子关闭 STIL 时,两类细胞中的 p53 蛋白水平都上升,细胞形成的克隆和悬浮球体(类干性行为的标志)减少。具有功能性 TP53 的细胞对此尤其敏感,这表明 STIL 通常通过削弱 p53 阻止细胞周期的能力来发挥作用。在已突变的 TP53 细胞中(本已缺乏完整的 p53 功能),阻断 STIL 仍显著影响细胞的运动性:侵袭性突变细胞在去除 STIL 后移动与“伤口愈合”速度变慢,说明其侵袭行为在很大程度上依赖该基因。
对未来更精准治疗的启示
用通俗的话说,这项工作把 STIL 描绘为一个同谋,帮助遗传性的 TP53 缺陷发展为危险的骨癌。STIL 一方面松动细胞内部的安全制动,另一方面支持一小群可侵袭骨骼、转移远处并躲避免疫攻击的类干肿瘤细胞。因为高 STIL 也与对某些药物敏感性改变相关——例如推动已不稳定癌细胞进入致死性分裂的 WEE1 抑制剂——它可能作为一种生物标志,帮助将患者与个体化疗法匹配。尽管还需更多研究在患者中验证这些想法,本研究强调了 STIL 作为理解并最终解除李-弗劳门尼综合征相关骨肉瘤的一个有前景的新切入点。
引用: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
关键词: 李-弗劳门尼综合征, 骨肉瘤, TP53, STIL, 癌症干细胞