Clear Sky Science · he
ניתוח מולטי-אומיקס מגלה את התפקיד המרכזי של STIL בתסמונת לי-פרומני ואוסטאוסארקומה
כשסיכון תורשתי נפגש עם סרטן עצם של הילדות
יש משפחות שמעבירות הלאה יותר מאשר צבע עיניים או גובה — הן גם נושאות סיכון מוגבר משמעותית לפתח סרטן. אחת מהמצבים הללו, תסמונת לי–פרומני, מגדילה באופן דרמטי את הסיכון לאוסטאוסארקומה, סרטן עצם נדיר אך אגרסיבי שלרוב פוגע בילדים ובנערים. המחקר הזה שואל שאלה דחופה: מעבר לגן המפורסם "השומר" TP53, אילו מולקולות נוספות מסייעות להפוך את הסיכון התורשתי הזה לגידול עצם שגדל במהירות וקשה לטיפול, והאם הן יכולות להפוך למטרות טיפוליות חדשות?
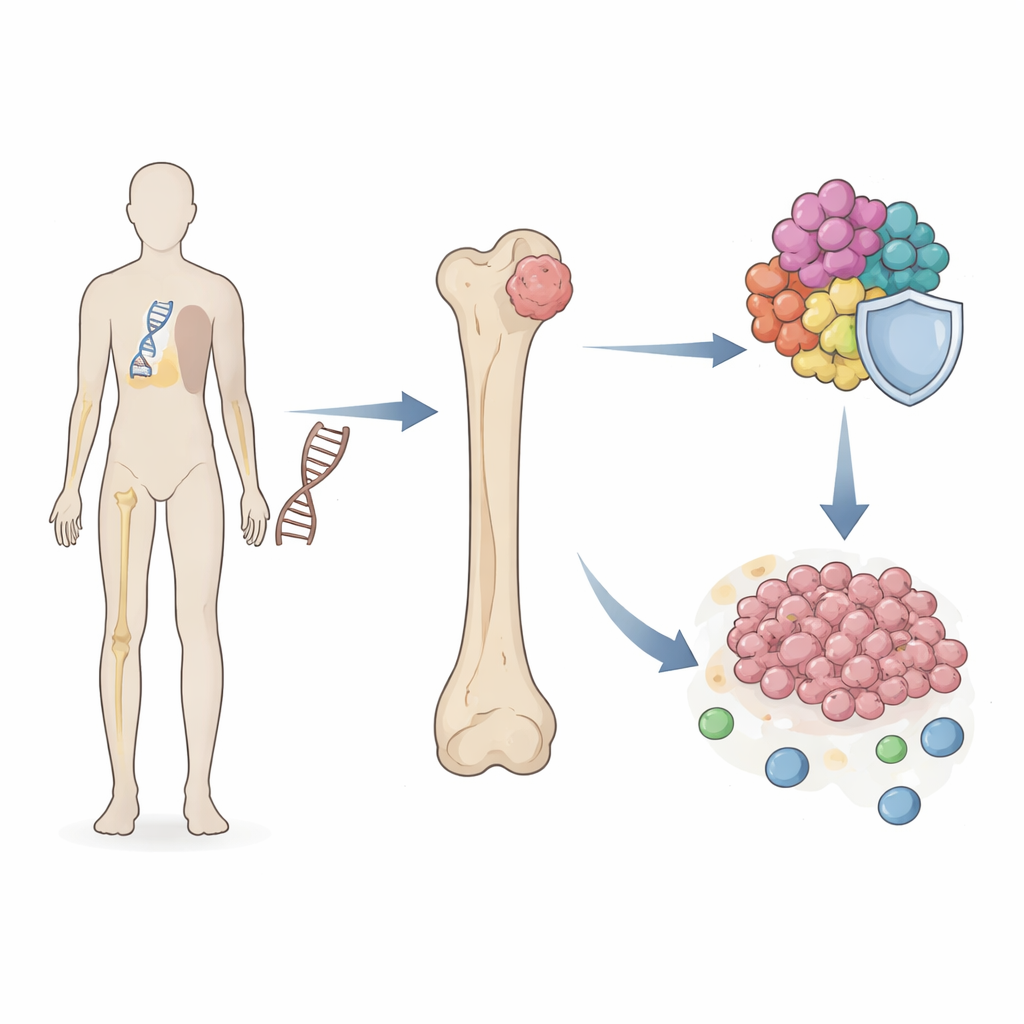
מחבר נסתר בין סיכון תורשתי וצמיחת גידול
החוקרים התמקדו בתסמונת לי–פרומני, שבה עותק פגום של TP53 קיים בכל תא מלידה. אנשים עם תסמונת זו נמצאים בסיכון בשיעורים של מאות פעמים יותר לפתח אוסטאוסארקומה לעומת האוכלוסייה הכללית. בעזרת מאגרים רחבים של דגימות רקמה ותאי מטופלים, הקבוצה סרקה אלפי גנים כדי למצוא אלו שמשותפים לדגימות תסמונת לי–פרומני ולגידולי אוסטאוסארקומה. הם גילו קבוצה קטנה של גנים "גשר" שהפעילות שלהם השתנתה בשתי המצבים והצטברו בתהליכים שמפקחים על חלוקת התאים והכפלת הכרומוזומים — שלבים מרכזיים שכאשר הם מופרעים יכולים להניע סרטן.
STIL בולט כגורם המרכזי
באמצעות מספר שיטות למידת מכונה, המדענים הצליחו לצמצם את קבוצת הגנים הגשרית לארבעה גנים מפתח ומצאו דומיננטי אחד: גן בשם STIL. בדגימות אוסטאוסארקומה רמות STIL היו גבוהות בעקביות בגידולים שכבר פיזרו גרורות, וחולים שלגביהם הגידולים ביטאו יותר STIL נטו לחיות זמן קצר יותר. ניתוחי מסלולים קישרו רמות גבוהות של STIL למחזור תאי מואץ ולפירוק חלבונים, בעוד שרמות נמוכות של STIL נקשרו לאותות חיסוניים ודלקתיים חזקים יותר. התבנית הזו רמזה ש-STIL לא רק מסייעת לתאי סרטן העצם להתחלק אלא גם עשויה להחליש את ההגנות הטבעיות של הגוף נגדם.
תאים דמויי-גֵרָעין, מערכת חיסון שקטה
כדי לזהות היכן STIL פועלת בתוך הגידול, הקבוצה פנתה לריצוף חד-תאי, שמפרט תאים בודדים אחד-אחד. הם מיפו למעלה מ-100,000 תאים מדגימות אוסטאוסארקומה וזיהו מספר סוגי תאים ממאירים. STIL הייתה בשפע במיוחד בתת-קבוצה של תאים ממאירים מאוד "דמויי-גזע" שנמצאים בתחילת מסלולי ההתפתחות — תאים שנראה שמזריעים ומתחזקים את הסרטן. בתאים אלה, רמות גבוהות של STIL נקשרו לאותות שמעודדים חידוש עצמי, מפעילים תאים מפרקי-עצם שמאכלים את השלד ומעצבבים את תאי המערכת החיסונית הסמוכים. גידולים עשירים ב-STIL הראו פחות תאי T קטלניים פעילים ומולקולות מפתח המפעילות חיסון, תבנית המזכירה "מדבר חיסוני" שבו המערכת החיסונית אינה מזהה או תוקפת את הסרטן ביעילות.
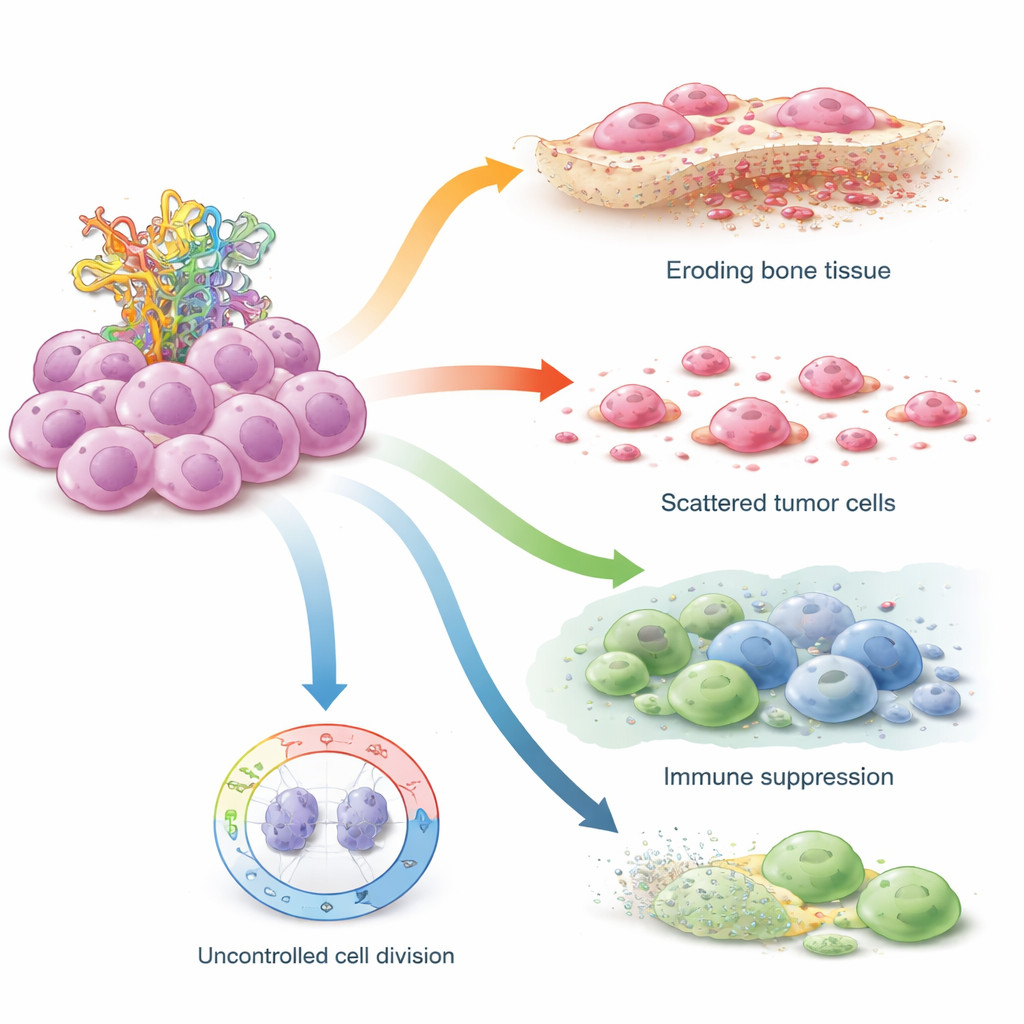
כיצד STIL מחלישה את הבלמים הפנימיים של התא
החוקרים בחנו אז ישירות את STIL בקווי תאי אוסטאוסארקומה שגודלו במעבדה, והשוו תאים עם TP53 תקין לאלו הנושאים מוטציות ב-TP53 המדמות תסמונת לי–פרומני. כאשר השתמשו במולקולות RNA קטנות כדי לכבות את STIL, רמות חלבון p53 עלו בשני סוגי התאים, והתאים יצרו פחות מושבות ופחות כדורים צפים — סימן להתנהגות דמויי-גזע מופחתת. תאים עם TP53 מתפקד היו רגישים במיוחד, מה שמרמז ש-STIL בדרך כלל פועלת להחליש את יכולתו של p53 לעצור את מחזור התא. בתאים עם מוטציית TP53, שכבר חסרה להם פעילות מלאה של p53, חסימת STIL עדיין השפיעה חזק על יכולת התנועה: תאים מוטנטיים אגרסיביים זזו ו"ריפאו" פצעים לאט יותר לאחר הסרת STIL, מה שמצביע על כך שההתנהגות הפולשנית שלהם תלויה במידה רבה בגן זה.
השלכות לטיפולים מדויקים בעתיד
במונחים פשוטים, המחקר מצייר את STIL כשותף לפשע שעוזר לפגמים התורשתיים ב-TP53 לפרוח לסרטנים עצם מסוכנים. STIL משחררת את הבלמים הפנימיים של התא ומעצימה מאגר קטן של תאים דמויי-גזע שיכולים לפלוש לעצם, לפזר לגרורות ולהסתתר מפני התקפות חיסוניות. מאחר שרמות גבוהות של STIL גם נקשרות לשינויים ברגישות לתרופות מסוימות — כגון מעכבי WEE1 שמדחיקים תאים סרטניים בלתי יציבים לחלוק בצורה קטלנית — היא עשויה לשמש כסמן ביולוגי להתאמת מטופלים לטיפולים ממוקדים. אמנם יש צורך בעבודה נוספת כדי לבדוק רעיונות אלה בחולים, המחקר מדגיש את STIL כידית חדשה ומבטיחה להבנת האוסטאוסארקומה ובסופו של דבר לנטרל אותה במשפחות החיות עם תסמונת לי–פרומני.
ציטוט: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
מילות מפתח: תסמונת לי-פרומני, אוסטאוסארקומה, TP53, STIL, תאי גזע ממאירים