Clear Sky Science · de
Multi-omics-Analyse zeigt die Schlüsselrolle von STIL beim Li‑Fraumeni‑Syndrom und Osteosarkom
Wenn vererbtes Risiko auf kindlichen Knochentumor trifft
Manche Familien vererben mehr als Augenfarbe oder Körpergröße — sie geben auch ein deutlich erhöhtes Krebsrisiko weiter. Eine solche Erkrankung, das Li‑Fraumeni‑Syndrom, erhöht das Risiko für ein Osteosarkom erheblich: ein seltener, aber aggressiver Knochentumor, der häufig Kinder und Jugendliche trifft. Die Studie stellt eine drängende Frage: Abgesehen vom bekannten „Wächter“ TP53, welche weiteren Moleküle verwandeln dieses vererbte Risiko in einen schnell wachsenden, schwer zu behandelnden Knochentumor, und könnten sie neue Therapieziele liefern?
Ein verborgener Verbindungspunkt zwischen vererbtem Risiko und Tumorwachstum
Die Forschenden konzentrierten sich auf das Li‑Fraumeni‑Syndrom, bei dem von Geburt an in jeder Zelle eine fehlerhafte TP53‑Kopie vorhanden ist. Menschen mit diesem Syndrom haben ein um das Hundert‑ bis Tausendfache erhöhtes Risiko, ein Osteosarkom zu entwickeln, verglichen mit der Allgemeinbevölkerung. Mithilfe großer Sammlungen von Patientenproben und Zell‑Datensätzen durchsuchte das Team Tausende von Genen, um solche zu finden, die sowohl in Li‑Fraumeni‑Proben als auch in Osteosarkomtumoren verändert sind. Sie entdeckten eine kleine Gruppe von „Brücken“genen, deren Aktivität in beiden Zuständen verändert war und die sich in Prozesse zur Steuerung der Zellteilung und Chromosomenverdopplung bündelten — zentrale Schritte, die bei Störung Krebs antreiben können.
STIL tritt als zentrales Problemgen zutage
Durch den Einsatz mehrerer maschineller Lernverfahren reduzierten die Wissenschaftler diese Brückengruppe auf vier Schlüsselfaktoren und identifizierten ein herausragendes Gen: STIL. In Osteosarkomproben war STIL in Tumoren, die bereits gestreut hatten, konsequent stärker exprimiert, und Patienten mit hoher STIL‑Expression lebten tendenziell kürzer. Signalwegsanalysen verbanden hohe STIL‑Werte mit starker Zellzyklusaktivität und Proteinabbau, während niedrige STIL‑Werte mit stärkeren Immun‑ und Entzündungssignalen assoziiert waren. Dieses Muster legt nahe, dass STIL nicht nur die Zellteilung von Knochenkrebszellen fördert, sondern möglicherweise auch die natürlichen Abwehrmechanismen des Körpers gegen sie dämpft.
Stammzellähnliche Zellen, stilles Immunsystem
Um zu verstehen, wo STIL in einem Tumor wirkt, nutzte das Team Einzelzellsequenzierung, die einzelne Zellen einzeln charakterisiert. Sie kartierten mehr als 100.000 Zellen aus Osteosarkomproben und identifizierten mehrere maligne Zelltypen. STIL war besonders reichlich in einer Untergruppe hoch „stammzellähnlicher“ Tumorzellen vorhanden, die am Beginn von Entwicklungsverläufen standen — Zellen, die offenbar den Tumor säen und erhalten. In diesen Zellen war hohe STIL‑Expression mit Signalen verbunden, die Selbst‑Erneuerung fördern, knochenabbauende Zellen aktivieren und die umgebenden Immunzellen umformen. In STIL‑reichen Tumoren fanden sich weniger aktive Killer‑T‑Zellen und weniger Schlüsselmoleküle zur Immunaktivierung — ein Muster, das einem „immunologischen Wüstengebiet“ ähnelt, in dem das Immunsystem den Tumor nicht wirksam erkennt oder angreift.
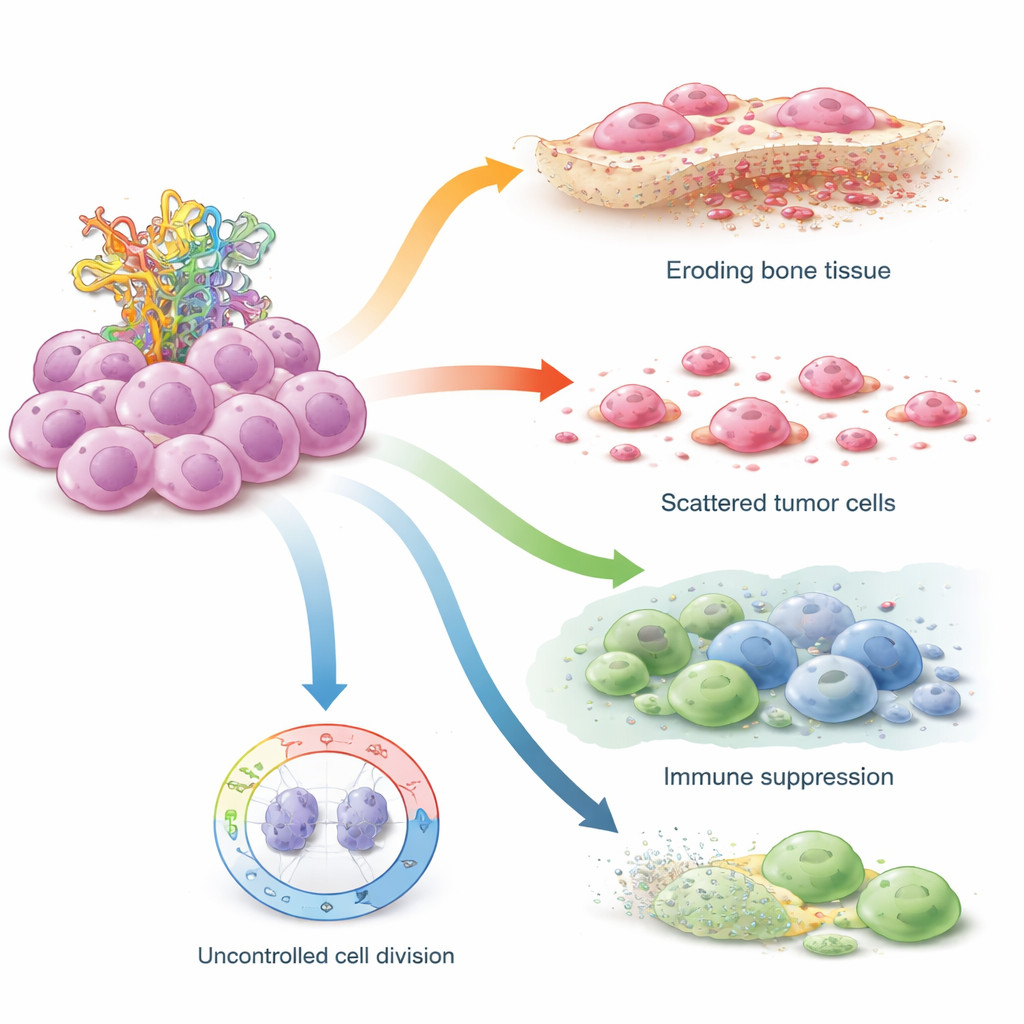
Wie STIL die Sicherheitsbremsen der Zelle untergräbt
Die Forschenden testeten STIL anschließend direkt in im Labor gezüchteten Osteosarkom‑Zelllinien und verglichen Zellen mit intaktem TP53 mit solchen, die TP53‑Mutationen tragen, welche das Li‑Fraumeni‑Syndrom nachahmen. Als sie STIL mit kleinen RNA‑Molekülen ausschalteten, stiegen die p53‑Proteinspiegel in beiden Zelltypen, und die Zellen bildeten weniger Kolonien und weniger frei schwebende Sphären — ein Kennzeichen reduzierten stammzellähnlichen Verhaltens. Zellen mit funktionsfähigem TP53 waren besonders empfindlich, was darauf hindeutet, dass STIL normalerweise die Fähigkeit von p53 schwächt, den Zellzyklus anzuhalten. In TP53‑mutanten Zellen, denen bereits eine volle p53‑Funktion fehlt, hatte die Blockade von STIL dennoch starken Einfluss auf die Motilität: Aggressive Mutantenzellen bewegten sich und „heilten“ Wunden nach Entfernung von STIL langsamer, was darauf hindeutet, dass ihr invasives Verhalten stark von diesem Gen abhängt.
Folgen für künftige, präzisere Behandlungen
Anschaulich betrachtet zeichnet die Arbeit STIL als Komplizen, der vererbte TP53‑Defekte in gefährliche Knochentumoren verwandelt. STIL lockert sowohl die inneren Sicherheitsbremsen der Zelle als auch stärkt einen kleinen Pool stammzellähnlicher Tumorzellen, die in Knochen eindringen, in entfernte Organe streuen und sich vor Immunangriffen verstecken können. Weil hohe STIL‑Werte außerdem mit veränderter Empfindlichkeit gegenüber bestimmten Medikamenten — etwa WEE1‑Inhibitoren, die bereits instabile Krebszellen in tödliche Teilungen treiben — verbunden sind, könnte STIL als Biomarker dienen, um Patienten gezielten Therapien zuzuordnen. Zwar sind weitere Untersuchungen nötig, um diese Befunde klinisch zu prüfen, doch hebt die Studie STIL als vielversprechenden Ansatzpunkt hervor, um Osteosarkome bei Familien mit Li‑Fraumeni‑Syndrom besser zu verstehen und schließlich zu bekämpfen.
Zitation: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Schlüsselwörter: Li‑Fraumeni‑Syndrom, Osteosarkom, TP53, STIL, Krebsstammzellen