Clear Sky Science · fr
Analyse multi-omique révèle le rôle clé de STIL dans le syndrome de Li‑Fraumeni et l’ostéosarcome
Quand le risque héréditaire rencontre le cancer osseux infantile
Certaines familles transmettent plus que la couleur des yeux ou la taille—elles héritent aussi d’un risque beaucoup plus élevé de développer un cancer. Une de ces conditions, le syndrome de Li‑Fraumeni, augmente fortement le risque d’ostéosarcome, un cancer osseux rare mais agressif qui touche souvent les enfants et les adolescents. Cette étude pose une question cruciale : au‑delà du célèbre gène « gardien » TP53, quelles autres molécules contribuent à transformer ce risque hérité en une tumeur osseuse à croissance rapide et difficile à traiter, et pourraient-elles devenir de nouvelles cibles thérapeutiques ?
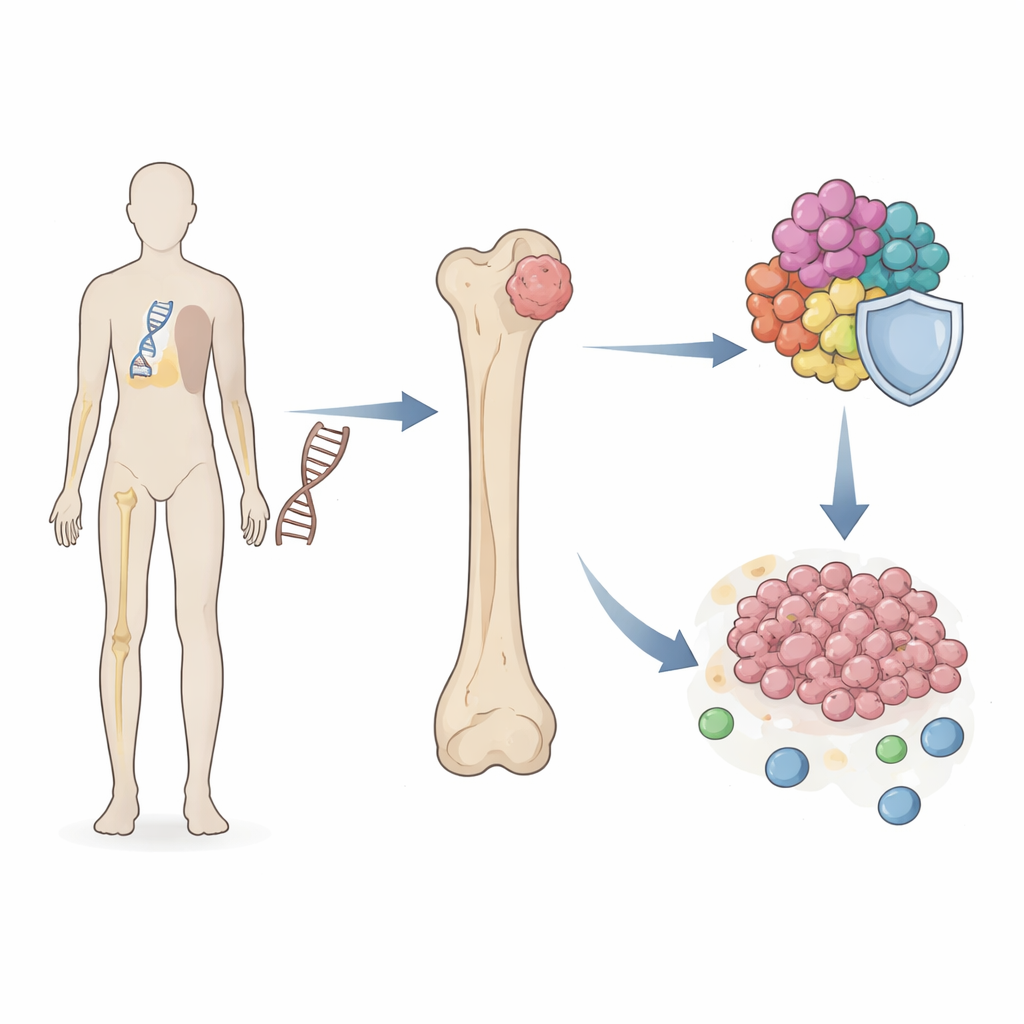
Un lien caché entre le risque héréditaire et la croissance tumorale
Les chercheurs se sont concentrés sur le syndrome de Li‑Fraumeni, où une copie défaillante de TP53 est présente dans chaque cellule dès la naissance. Les personnes atteintes de ce syndrome ont des probabilités des centaines de fois supérieures de développer un ostéosarcome par rapport à la population générale. En utilisant de larges collections de données issues de tissus et de cellules de patients, l’équipe a passé au crible des milliers de gènes pour identifier ceux partagés entre les échantillons de Li‑Fraumeni et les tumeurs d’ostéosarcome. Ils ont découvert un petit ensemble de gènes « passerelles » dont l’activité était altérée dans les deux contextes et qui se regroupaient autour de processus contrôlant la division cellulaire et la copie des chromosomes—des étapes fondamentales qui, lorsque perturbées, peuvent favoriser le cancer.
STIL émerge comme le principal fauteur de troubles
En appliquant plusieurs méthodes d’apprentissage automatique, les scientifiques ont réduit cet ensemble de passerelles à quatre gènes clés et identifié un élément dominant : un gène nommé STIL. Dans les échantillons d’ostéosarcome, les niveaux de STIL étaient systématiquement plus élevés dans les tumeurs déjà métastatiques, et les patients dont la tumeur exprimait davantage STIL avaient tendance à présenter une survie plus courte. Les analyses de voies biologiques ont relié un fort niveau de STIL à un cycle cellulaire soutenu et à un accroissement de la dégradation protéique, tandis qu’un STIL faible s’associait à des signaux immunitaires et inflammatoires plus marqués. Ce schéma suggère que STIL non seulement favorise la division des cellules cancéreuses osseuses, mais peut aussi atténuer les défenses naturelles de l’organisme contre elles.
Cellules de type souche, système immunitaire muet
Pour localiser l’action de STIL au sein d’une tumeur, l’équipe s’est tournée vers le séquençage unicellulaire, qui profile les cellules individuellement. Ils ont cartographié plus de 100 000 cellules issues d’échantillons d’ostéosarcome et identifié plusieurs types cellulaires malins. STIL était particulièrement abondant dans un sous‑ensemble de cellules tumorales fortement « de type souche » qui se situaient au début des trajectoires de développement—des cellules qui semblent ensemencer et entretenir la tumeur. Dans ces cellules, un fort niveau de STIL était lié à des signaux favorisant l’auto‑renouvellement, l’activation d’ostéoclastes qui rongent le squelette, et la reprogrammation des cellules immunitaires environnantes. Les tumeurs riches en STIL montraient moins de lymphocytes T cytotoxiques actifs et de molécules clés d’activation immunitaire, un profil ressemblant à un « désert immunitaire » où le système immunitaire ne parvient pas à reconnaître ou attaquer efficacement le cancer.
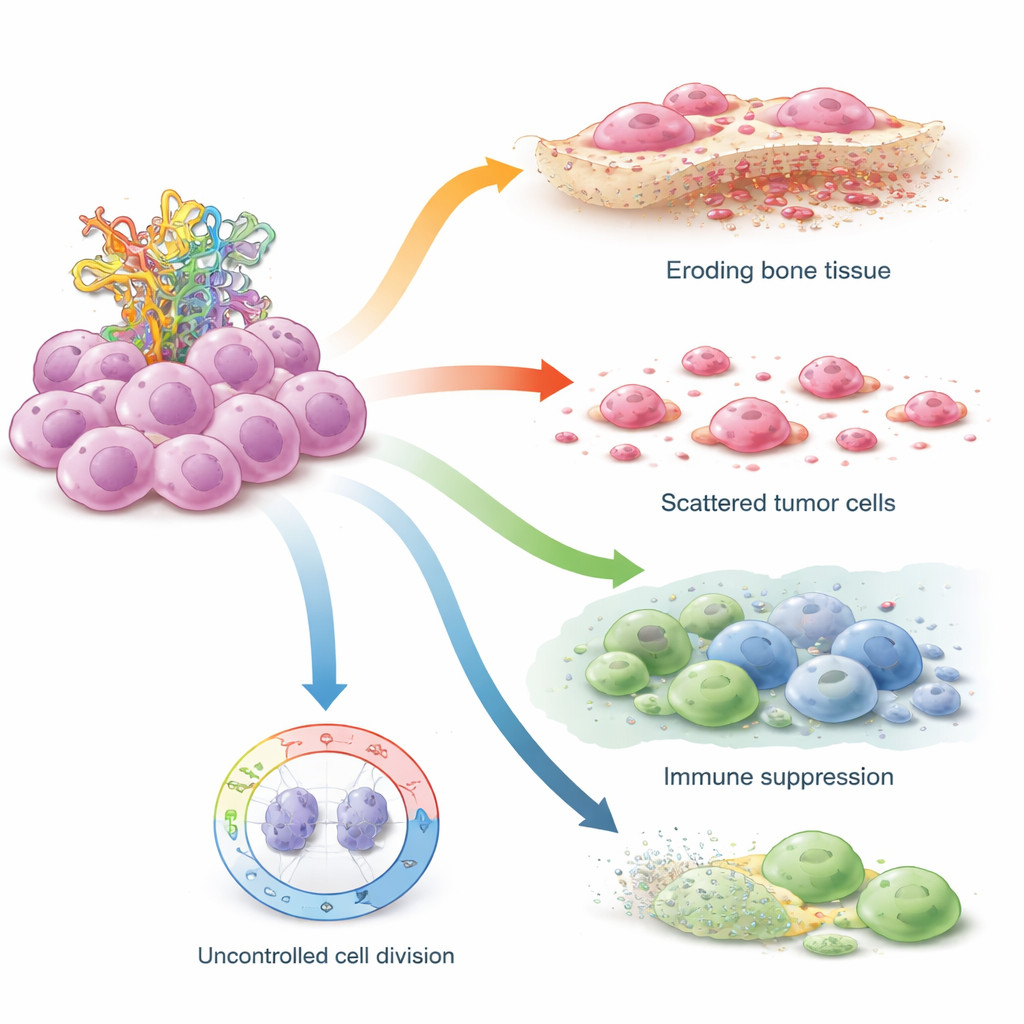
Comment STIL sape les freins de sécurité de la cellule
Les chercheurs ont ensuite testé STIL directement dans des lignées cellulaires d’ostéosarcome cultivées en laboratoire, en comparant des cellules avec un TP53 fonctionnel à celles portant des mutations de TP53 qui miment le syndrome de Li‑Fraumeni. Lorsqu’ils ont utilisé de petits ARN pour éteindre STIL, les niveaux de protéine p53 ont augmenté dans les deux types cellulaires, et les cellules formaient moins de colonies et moins de sphères en suspension—un signe de réduction du comportement de type souche. Les cellules ayant un TP53 fonctionnel étaient particulièrement sensibles, ce qui suggère que STIL agit normalement pour affaiblir la capacité de p53 à arrêter le cycle cellulaire. Dans les cellules mutées pour TP53, qui ont déjà une fonction p53 compromise, le blocage de STIL a néanmoins eu un fort impact sur la motilité : les cellules mutants agressives se déplaçaient et « recouvraient » les plaies plus lentement une fois STIL supprimé, indiquant que leur comportement invasif dépend largement de ce gène.
Implications pour des traitements futurs plus précis
En termes concrets, ce travail présente STIL comme un complice qui aide les défauts héréditaires de TP53 à se transformer en cancers osseux dangereux. STIL relâche à la fois les freins internes de la cellule et nourrit une petite population de cellules tumorales de type souche capables d’envahir l’os, de se propager à distance et de se cacher de l’attaque immunitaire. Parce qu’un fort niveau de STIL est aussi associé à une sensibilité modifiée à certains médicaments—comme les inhibiteurs de WEE1 qui poussent des cellules cancéreuses déjà instables vers des divisions létales—il pourrait servir de biomarqueur pour associer les patients à des thérapies adaptées. Bien que des travaux supplémentaires soient nécessaires pour tester ces idées chez les patients, l’étude met en avant STIL comme une nouvelle poignée prometteuse pour comprendre et, à terme, neutraliser l’ostéosarcome dans les familles porteuses du syndrome de Li‑Fraumeni.
Citation: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Mots-clés: syndrome de Li‑Fraumeni, ostéosarcome, TP53, STIL, cellules souches cancéreuses