Clear Sky Science · pt
Análise multiômica revela o papel chave de STIL na síndrome de Li‑Fraumeni e no osteossarcoma
Quando o Risco Herdado Encontra o Câncer Ósseo Infantil
Algumas famílias transmitem mais do que cor dos olhos ou altura — elas também herdam uma probabilidade muito maior de desenvolver câncer. Uma dessas condições, a síndrome de Li–Fraumeni, aumenta drasticamente o risco de osteossarcoma, um câncer ósseo raro mas agressivo que frequentemente atinge crianças e adolescentes. Este estudo investiga uma questão urgente: além do famoso gene “guardião” TP53, quais outras moléculas ajudam a transformar esse risco herdado em um tumor ósseo de crescimento rápido e difícil de tratar, e elas poderiam se tornar novos alvos terapêuticos?
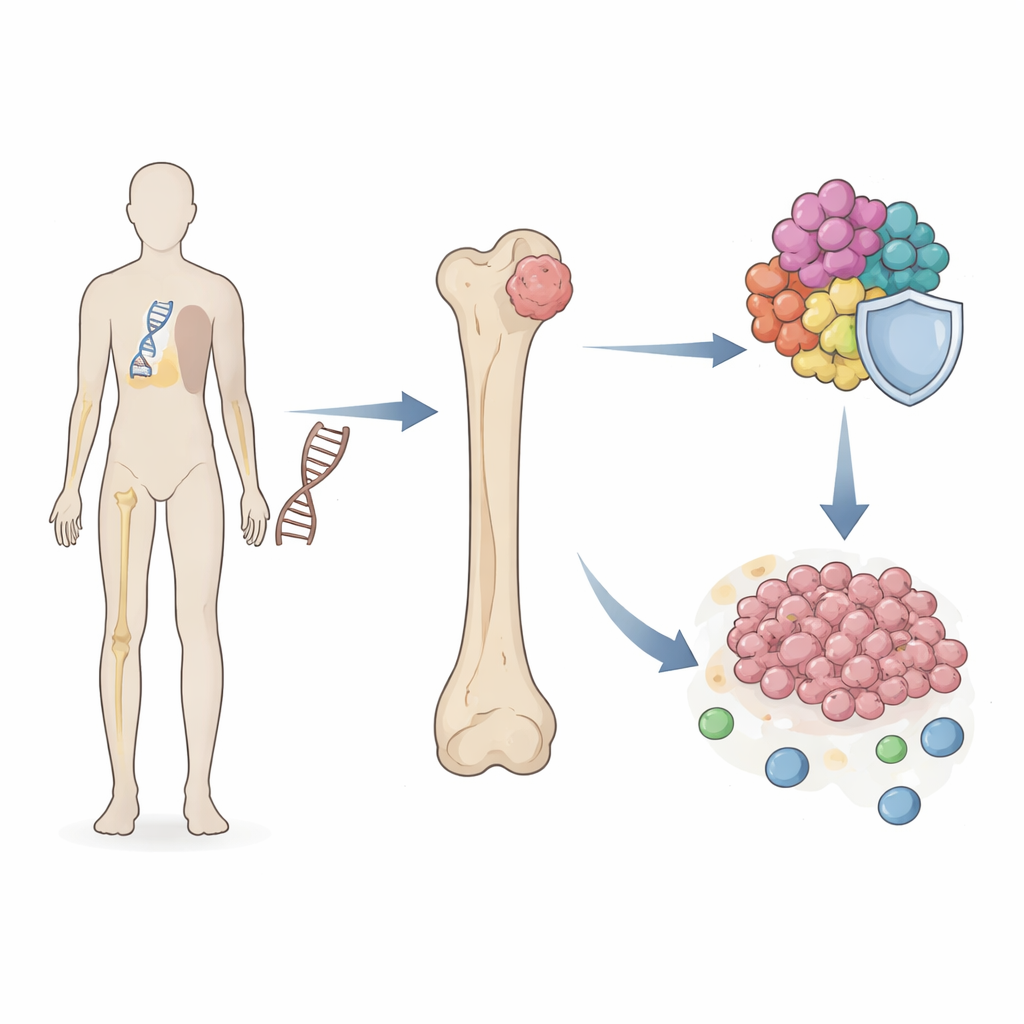
Um Conector Oculto Entre o Risco Herdado e o Crescimento Tumoral
Os pesquisadores concentraram‑se na síndrome de Li–Fraumeni, em que uma cópia defeituosa de TP53 está presente em todas as células desde o nascimento. Pessoas com essa síndrome têm centenas de vezes mais probabilidade de desenvolver osteossarcoma do que a população em geral. Usando grandes coleções de dados de tecidos e células de pacientes, a equipe vasculhou milhares de genes para encontrar aqueles compartilhados entre amostras de Li–Fraumeni e tumores de osteossarcoma. Descobriram um pequeno conjunto de genes “ponte” cuja atividade estava alterada em ambas as condições e que se agrupavam em processos que controlam divisão celular e replicação cromossômica — etapas centrais que, quando perturbadas, podem impulsionar o câncer.
STIL Surge como o Principal Ator Problemático
Ao aplicar vários métodos de aprendizado de máquina, os cientistas reduziram esse conjunto de genes‑ponte para quatro genes-chave e identificaram um destaque: um gene chamado STIL. Nas amostras de osteossarcoma, os níveis de STIL eram consistentemente maiores em tumores que já haviam se espalhado, e pacientes cujos tumores expressavam mais STIL tendiam a ter sobrevida mais curta. Análises de vias ligaram STIL alto a ciclo celular acelerado e degradação proteica, enquanto STIL baixo foi associado a sinais imunológicos e inflamatórios mais fortes. Esse padrão sugeriu que STIL não apenas ajuda as células do câncer ósseo a se dividirem, mas também pode atenuar as defesas naturais do corpo contra elas.
Células com Traços de Tronco, Sistema Imune Silencioso
Para ver onde STIL age dentro de um tumor, a equipe recorreu ao sequenciamento de célula única, que perfila células individuais uma a uma. Eles mapearam mais de 100.000 células de amostras de osteossarcoma e identificaram vários tipos de células malignas. STIL era especialmente abundante em um subconjunto de células tumorais altamente “semelhantes a tronco” que se posicionavam no início dos trajetos de desenvolvimento — células que parecem semear e sustentar o câncer. Nessas células, STIL alto esteve ligado a sinais que incentivam a autorrenovação, ativam células que reabsorvem osso e remodelam as células imunes ao redor. Tumores ricos em STIL exibiam menos células T assassinas ativas e menos moléculas chave de ativação imune, um padrão semelhante a um “deserto imune” em que o sistema imune falha em reconhecer ou atacar o câncer de forma eficaz.
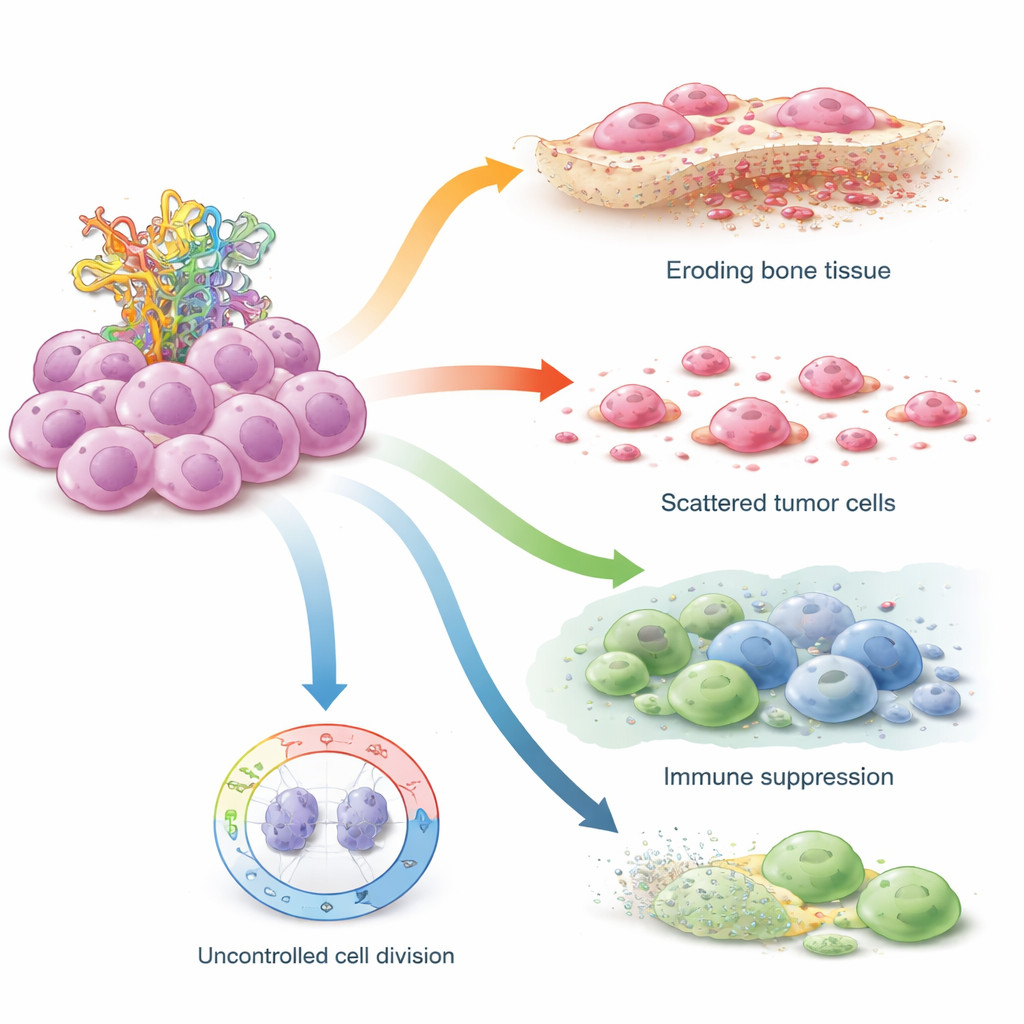
Como STIL Minada os Freios de Segurança da Célula
Os pesquisadores então testaram STIL diretamente em linhas celulares de osteossarcoma cultivadas em laboratório, comparando células com TP53 normal àquelas que carregavam mutações em TP53 que imitam a síndrome de Li–Fraumeni. Quando usaram pequenas moléculas de RNA para desligar STIL, os níveis da proteína p53 aumentaram em ambos os tipos celulares, e as células formaram menos colônias e menos esferas em suspensão — um marco de comportamento com menos características de célula‑tronco. Células com TP53 funcional foram particularmente sensíveis, sugerindo que STIL normalmente atua para enfraquecer a capacidade de p53 de interromper o ciclo celular. Em células com mutações em TP53, que já carecem da função plena de p53, bloquear STIL ainda apresentou forte impacto sobre a motilidade: células mutantes agressivas se moviam e “cicatrizavam” feridas mais lentamente uma vez que STIL foi removido, indicando que seu comportamento invasivo depende fortemente desse gene.
Implicações para Tratamentos Futuros Mais Precisos
Em termos práticos, este trabalho pinta STIL como um cúmplice que ajuda defeitos herdados em TP53 a desabrocharem em cânceres ósseos perigosos. STIL tanto afrouxa os freios internos de segurança da célula quanto potencializa um pequeno reservatório de células tumorais com traços de tronco que podem invadir o osso, disseminar‑se para locais distantes e escapar do ataque imunológico. Como STIL alto também está ligado a sensibilidade alterada a certos fármacos — como inibidores de WEE1, que forçam células cancerígenas já instáveis a entrarem em divisões letais — ele pode servir como biomarcador para casar pacientes com terapias sob medida. Embora sejam necessários mais estudos para testar essas ideias em pacientes, o estudo destaca STIL como uma alça promissora para entender e, eventualmente, desarmar o osteossarcoma em famílias que vivem com a síndrome de Li–Fraumeni.
Citação: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Palavras-chave: Síndrome de Li‑Fraumeni, osteossarcoma, TP53, STIL, células‑tronco cancerígenas