Clear Sky Science · ru
Мультиомный анализ выявляет ключевую роль STIL при синдроме Ли — Фраумени и остеосаркоме
Когда наследственный риск встречается с детским раком кости
Некоторые семьи передают не только цвет глаз или рост — они унаследуют существенно повышенный риск развития рака. Одно из таких состояний, синдром Ли–Фраумени, резко увеличивает вероятность развития остеосаркомы, редкой, но агрессивной опухоли кости, которая часто поражает детей и подростков. В этом исследовании поставлен важный вопрос: кроме знаменитого «стража» TP53, какие ещё молекулы превращают этот наследственный риск в быстро растущую, трудно поддающуюся лечению опухоль кости и могут ли они стать новыми мишенями для терапии?
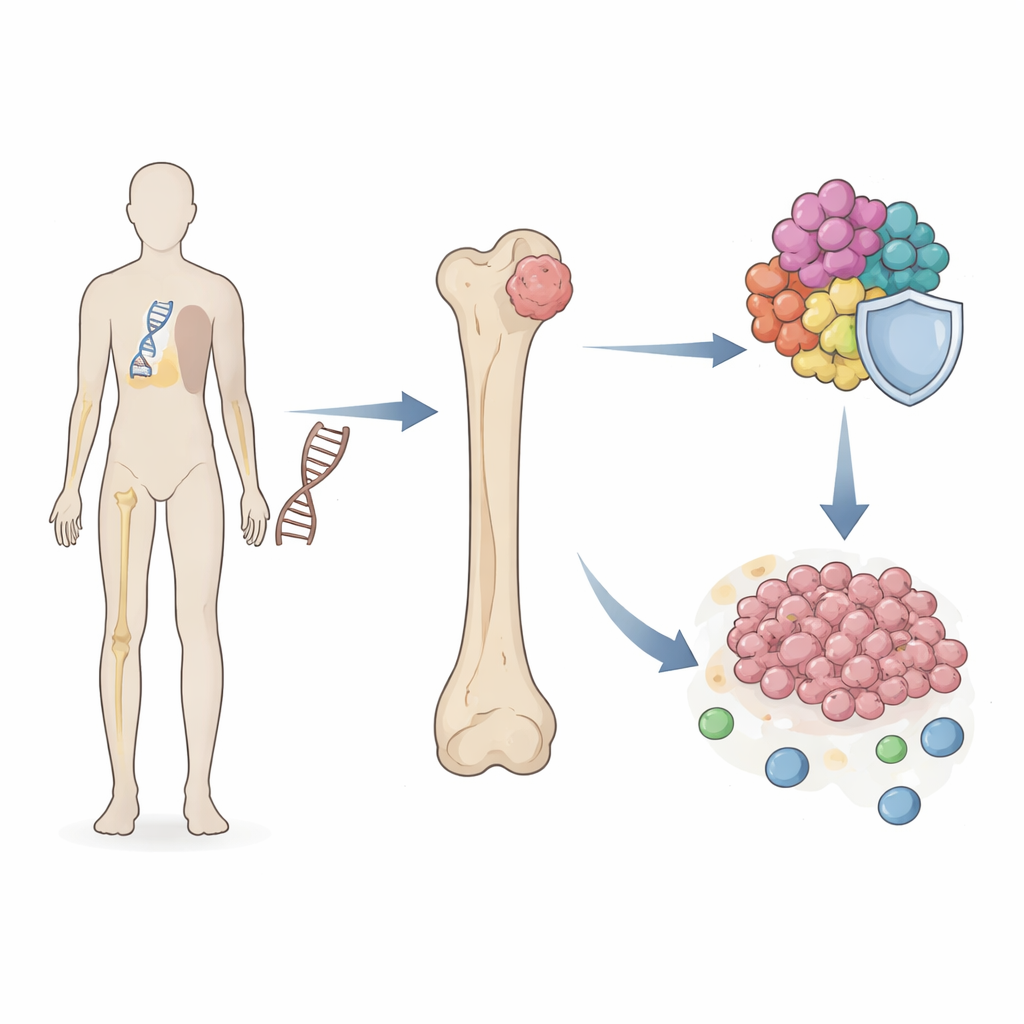
Скрытое звено между наследственным риском и ростом опухоли
Исследователи сосредоточились на синдроме Ли–Фраумени, при котором дефектная копия TP53 присутствует в каждой клетке с рождения. Люди с этим синдромом имеют на сотни раз более высокий риск развития остеосаркомы по сравнению с общей популяцией. Используя крупные коллекции образцов тканей и данные клеточных линий пациентов, команда просканировала тысячи генов в поисках тех, которые общие для образцов Ли–Фраумени и опухолей остеосаркомы. Они обнаружили небольшой набор «мостовых» генов, активность которых изменялась в обоих состояниях и которые объединялись в процессы, контролирующие деление клетки и копирование хромосом — ключевые этапы, нарушение которых может приводить к раку.
STIL выявлен как центральный виновник
Применив несколько методов машинного обучения, учёные сократили этот набор мостовых генов до четырёх ключевых и выделили один выдающийся — ген STIL. В образцах остеосаркомы уровни STIL были последовательно выше в опухолях, которые уже дали метастазы, а у пациентов с опухолями, экспрессировавшими больше STIL, выживаемость была ниже. Анализы путей связывали высокую экспрессию STIL с активным клеточным циклом и распадом белков, тогда как низкая экспрессия STIL ассоциировалась с усиленными иммунными и воспалительными сигналами. Такая картина намекала, что STIL не только способствует делению клеток опухоли кости, но и ослабляет естественные защитные механизмы организма против них.
Клетки-подобные стволовым, молчаливая иммунная система
Чтобы выяснить, где именно внутри опухоли действует STIL, команда обратилась к сиквенированию по отдельным клеткам, которое профилирует индивидуальные клетки по‑отдельности. Они картировали более 100 000 клеток из образцов остеосаркомы и идентифицировали несколько типов злокачественных клеток. STIL оказался особенно обилен в подмножестве высоко «стволоподобных» опухолевых клеток, находящихся в начале траекторий развития — клетках, которые, по‑видимому, сеют и поддерживают опухоль. В этих клетках высокая экспрессия STIL связывалась с сигналами, поощряющими самоподдержание, активацией остеокластов, разрушающих кость, и перестройкой окружающих иммунных клеток. Опухоли с высоким уровнем STIL демонстрировали меньше активных убивающих Т‑клеток и ключевых иммунно‑активирующих молекул — модель, напоминающую «иммунную пустыню», в которой иммунная система не распознаёт или не атакует опухоль эффективно.
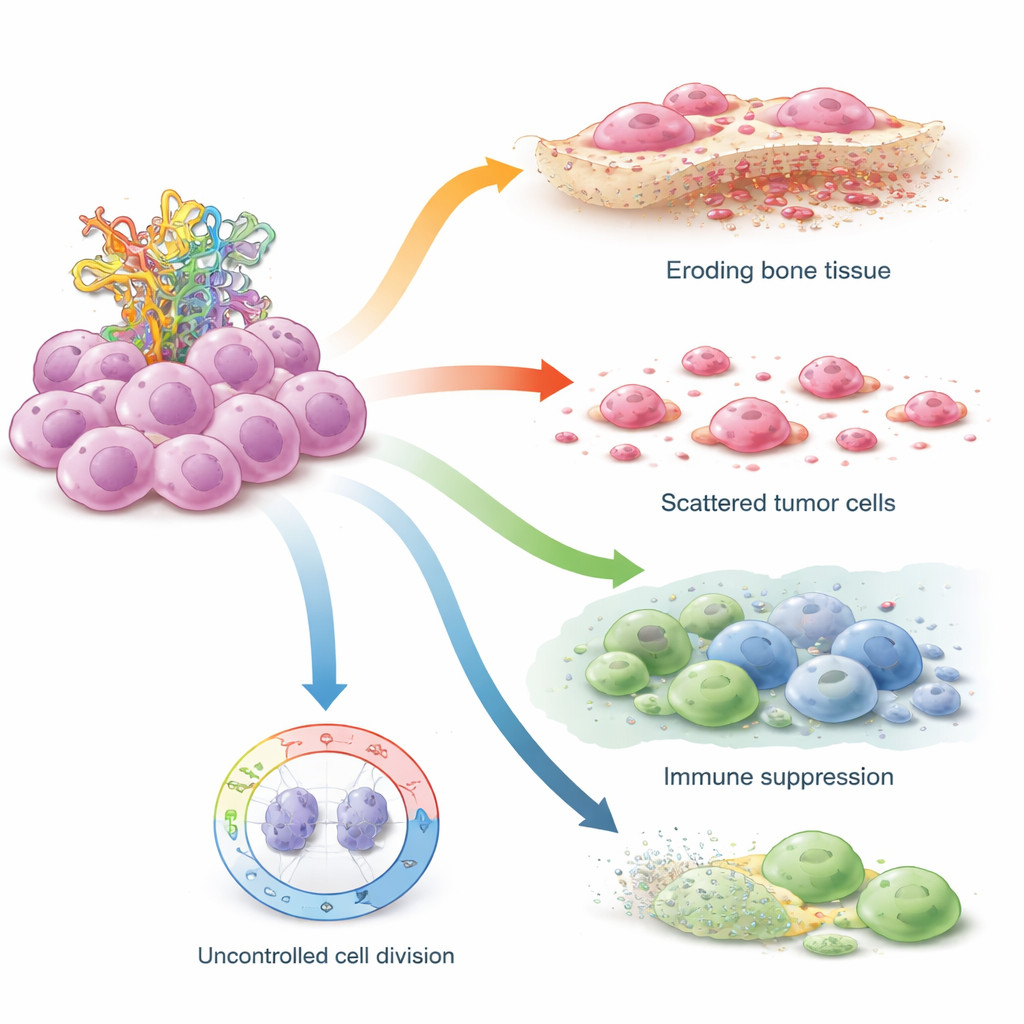
Как STIL подрывает тормоза безопасности клетки
Затем исследователи протестировали роль STIL напрямую на клеточных линиях остеосаркомы, выращенных в лаборатории, сравнивая клетки с нормальным TP53 и с мутациями TP53, имитирующими синдром Ли–Фраумени. При использовании коротких РНК для выключения STIL уровни белка p53 повышались в обоих типах клеток, и клетки формировали меньше колоний и меньше свободно плавающих сфер — признака уменьшения стволоподобного поведения. Клетки с функциональным TP53 оказались особенно чувствительными, что указывает на то, что STIL обычно ослабляет способность p53 останавливать клеточный цикл. В клетках с мутантным TP53, которые уже лишены полной функции p53, блокирование STIL всё ещё сильно влияло на подвижность: агрессивные мутантные клетки двигались и «заживали» раны медленнее после удаления STIL, что указывает на сильную зависимость их инвазивного поведения от этого гена.
Последствия для будущего, более точного лечения
Проще говоря, эта работа рисует STIL как соучастника, который помогает наследственным дефектам TP53 превратиться в опасные опухоли кости. STIL и ослабляет внутренние «тормоза» клетки, и поддерживает небольшой пул стволоподобных опухолевых клеток, способных вторгаться в кость, распространяться в отдалённые участки и прятаться от иммунной атаки. Поскольку высокая экспрессия STIL также связана с изменённой чувствительностью к определённым лекарствам — например, к ингибиторам WEE1, которые толкают уже нестабильные раковые клетки к губительному делению — он может служить биомаркером для подбора пациентам таргетной терапии. Хотя необходимы дополнительные исследования и клиническая проверка этих идей, исследование подчёркивает STIL как перспективную новую точку опоры для понимания и в конечном счёте нейтрализации остеосаркомы в семьях с синдромом Ли–Фраумени.
Цитирование: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Ключевые слова: синдром Ли‑Фраумени, остеосаркома, TP53, STIL, раковые стволовые клетки