Clear Sky Science · es
Análisis multi-ómico revela el papel clave de STIL en el síndrome de Li-Fraumeni y el osteosarcoma
Cuando el riesgo hereditario se encuentra con el cáncer óseo infantil
Algunas familias transmiten más que el color de ojos o la estatura: también heredan una probabilidad mucho mayor de desarrollar cáncer. Una de estas condiciones, el síndrome de Li–Fraumeni, aumenta drásticamente el riesgo de osteosarcoma, un cáncer óseo raro pero agresivo que suele afectar a niños y adolescentes. Este estudio plantea una pregunta urgente: más allá del famoso gen “guardián” TP53, ¿qué otras moléculas convierten ese riesgo hereditario en un tumor óseo de crecimiento rápido y difícil de tratar, y podrían ser nuevos objetivos terapéuticos?
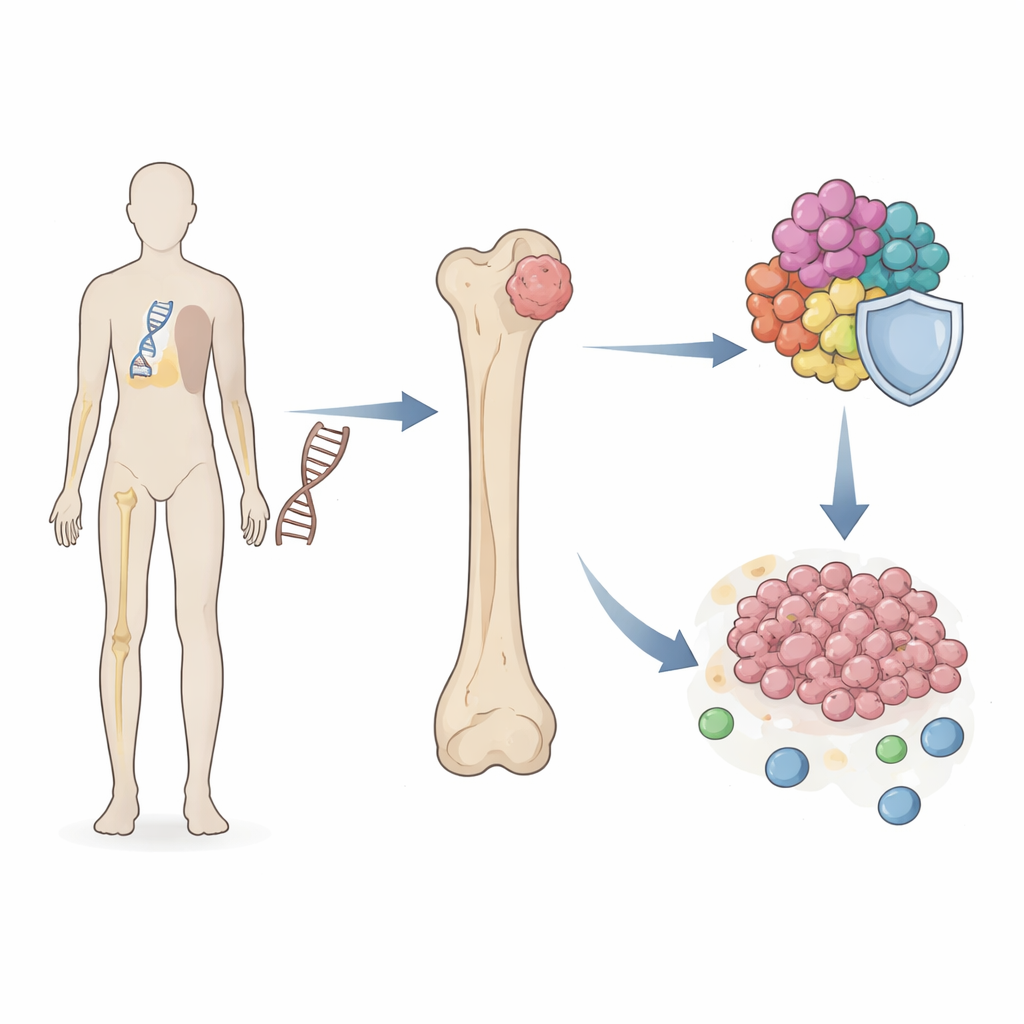
Un conector oculto entre el riesgo hereditario y el crecimiento tumoral
Los investigadores se centraron en el síndrome de Li–Fraumeni, en el que una copia defectuosa de TP53 está presente en cada célula desde el nacimiento. Las personas con este síndrome tienen cientos de veces más probabilidades de desarrollar osteosarcoma que la población general. Utilizando grandes colecciones de muestras de tejido y datos celulares de pacientes, el equipo escaneó miles de genes para encontrar aquellos compartidos entre muestras de Li–Fraumeni y tumores de osteosarcoma. Descubrieron un pequeño conjunto de genes “puente” cuya actividad estaba alterada en ambas condiciones y que se agrupaban en procesos que controlan la división celular y la replicación cromosómica: pasos centrales que, cuando se perturban, pueden impulsar el cáncer.
STIL emerge como el principal causante
Aplicando varios métodos de aprendizaje automático, los científicos redujeron este conjunto puente a cuatro genes clave y encontraron un destacado: un gen llamado STIL. En las muestras de osteosarcoma, los niveles de STIL eran sistemáticamente más altos en tumores que ya se habían diseminado, y los pacientes cuyos tumores producían más STIL tendían a tener una supervivencia más corta. Los análisis de vías asociaron altos niveles de STIL con un ciclo celular activo y degradación de proteínas, mientras que bajos niveles de STIL se relacionaron con señales inmunes e inflamatorias más fuertes. Este patrón sugiere que STIL no solo ayuda a las células del cáncer óseo a dividirse, sino que también puede atenuar las defensas naturales del organismo contra ellas.
Células con rasgos de madre y un sistema inmune silencioso
Para ver dónde actúa STIL dentro de un tumor, el equipo recurrió a la secuenciación unicelular, que perfila las células individuales una por una. Mapearon más de 100.000 células de muestras de osteosarcoma e identificaron varios tipos celulares malignos. STIL fue especialmente abundante en un subconjunto de células tumorales altamente “con rasgos de madre” que se situaban al inicio de las trayectorias de desarrollo: células que parecen sembrar y sostener el cáncer. En estas células, altos niveles de STIL se vincularon con señales que fomentan la autorrenovación, activan células que degradan el hueso y remodelan las células inmunes circundantes. Los tumores ricos en STIL mostraron menos células T asesinas activas y menos moléculas clave que activan la respuesta inmune, un patrón que recuerda a un “desierto inmunológico” en el que el sistema inmune no reconoce o ataca eficazmente al cáncer.
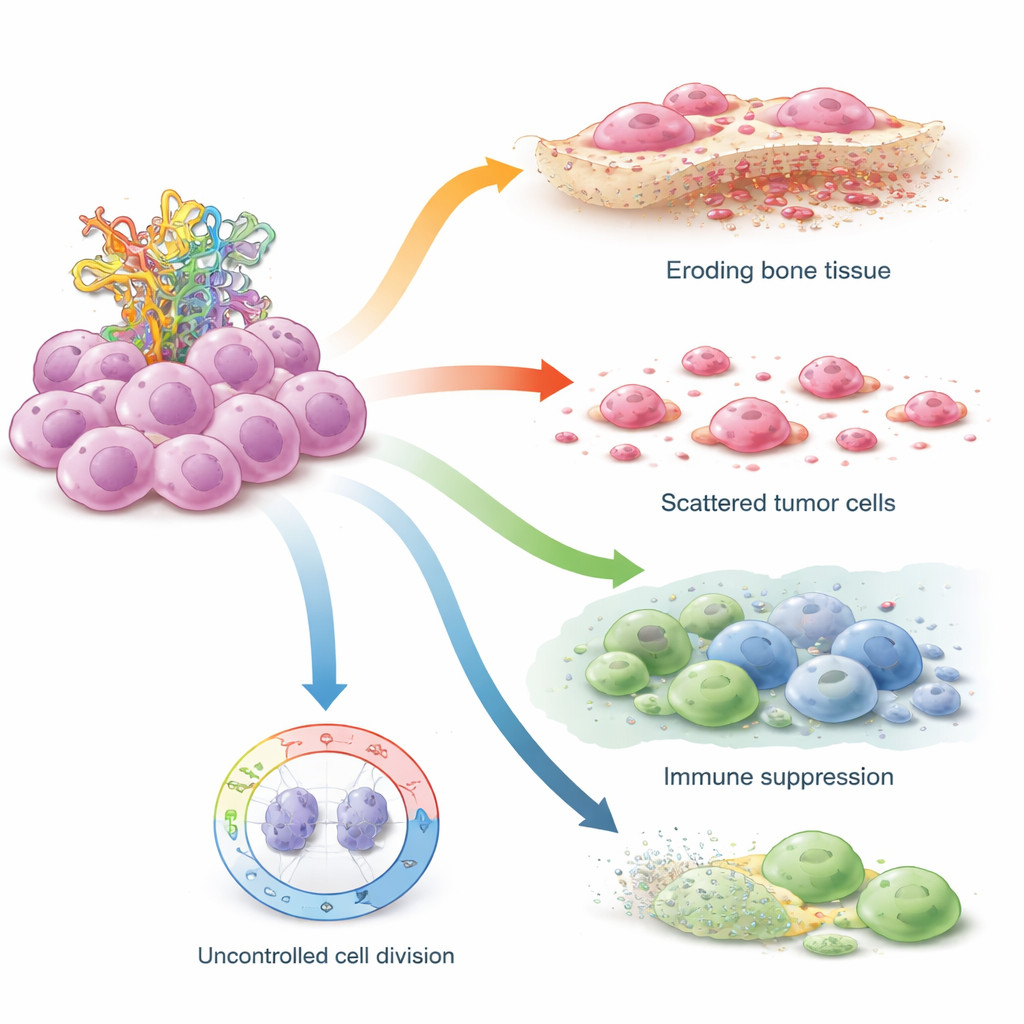
Cómo STIL socava los frenos de seguridad de la célula
Los investigadores probaron después STIL directamente en líneas celulares de osteosarcoma cultivadas en el laboratorio, comparando células con TP53 normal con otras portadoras de mutaciones en TP53 que imitan el síndrome de Li–Fraumeni. Cuando usaron pequeñas moléculas de ARN para apagar STIL, los niveles de proteína p53 aumentaron en ambos tipos celulares, y las células formaron menos colonias y menos esferas libres flotantes—un sello de reducción del comportamiento con rasgos de madre. Las células con TP53 funcional fueron particularmente sensibles, lo que sugiere que STIL normalmente actúa para debilitar la capacidad de p53 de detener el ciclo celular. En las células con mutaciones en TP53, que ya carecen de la función plena de p53, bloquear STIL siguió teniendo un fuerte impacto en la motilidad: las células mutantes agresivas se movieron y “curaron” heridas más lentamente una vez eliminado STIL, indicando que su comportamiento invasivo depende en gran medida de este gen.
Implicaciones para tratamientos futuros más precisos
En términos prácticos, este trabajo presenta a STIL como un cómplice que ayuda a que los defectos hereditarios de TP53 se conviertan en cánceres óseos peligrosos. STIL tanto afloja los frenos internos de la célula como potencia una pequeña reserva de células tumorales con rasgos de madre capaces de invadir el hueso, diseminarse a sitios distantes y esconderse del ataque inmune. Dado que altos niveles de STIL también se asocian con una sensibilidad alterada a ciertos fármacos—como los inhibidores de WEE1 que empujan a células cancerosas ya inestables a divisiones letales—podría servir como biomarcador para emparejar pacientes con terapias a medida. Aunque hacen falta más estudios para probar estas ideas en pacientes, el trabajo destaca a STIL como una nueva diana prometedora para comprender y, eventualmente, neutralizar el osteosarcoma en familias con síndrome de Li–Fraumeni.
Cita: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Palabras clave: Síndrome de Li-Fraumeni, osteosarcoma, TP53, STIL, células madre cancerosas