Clear Sky Science · it
Analisi multi-omica rivela il ruolo chiave di STIL nella sindrome di Li-Fraumeni e nell’osteosarcoma
Quando il rischio ereditario incontra il tumore osseo dell’infanzia
Alcune famiglie trasmettono più del colore degli occhi o dell’altezza: ereditano anche una probabilità molto più alta di sviluppare il cancro. Una di queste condizioni, la sindrome di Li–Fraumeni, aumenta drasticamente il rischio di osteosarcoma, un tumore osseo raro ma aggressivo che colpisce spesso bambini e adolescenti. Questo studio pone una domanda urgente: oltre al famoso gene «guardiano» TP53, quali altre molecole contribuiscono a trasformare questo rischio ereditario in un tumore osseo a rapida crescita e difficile da trattare, e potrebbero diventare nuovi bersagli terapeutici?
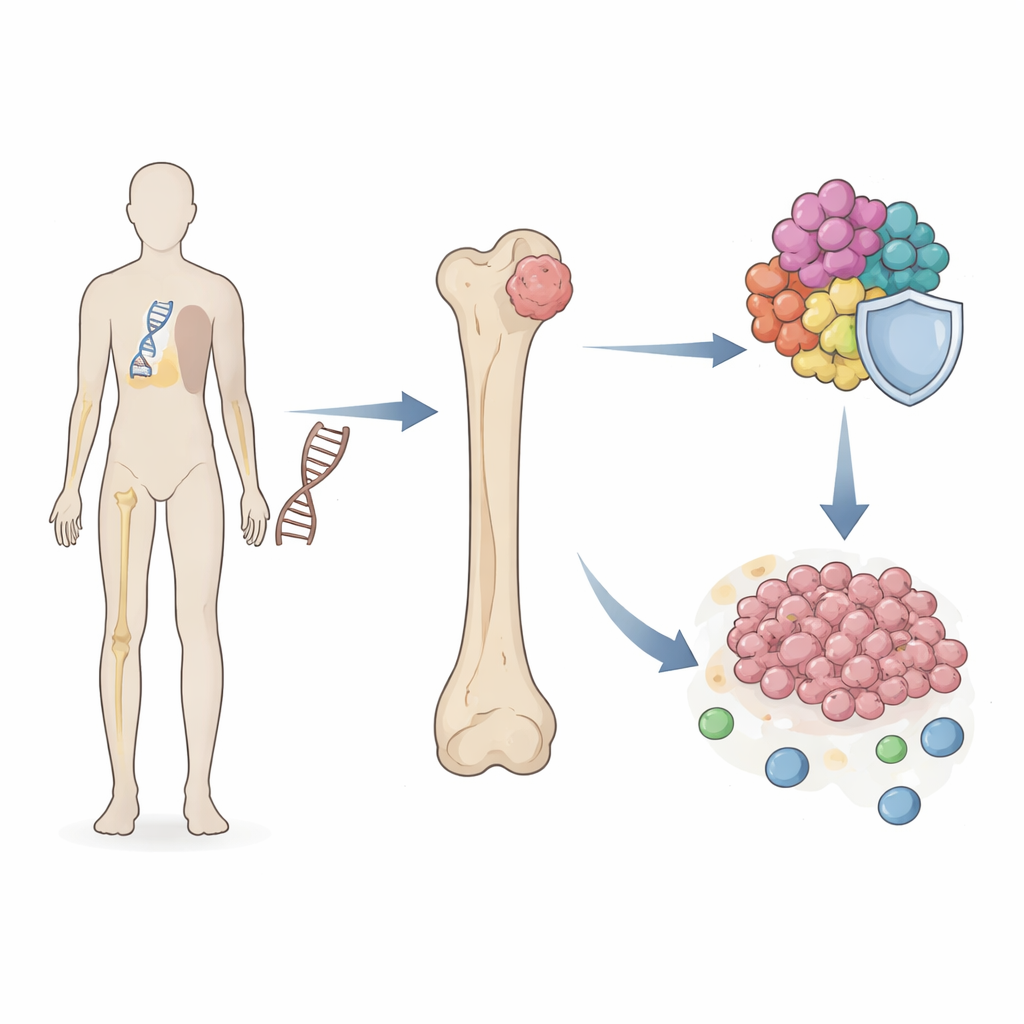
Un collegamento nascosto tra rischio ereditario e crescita tumorale
I ricercatori si sono concentrati sulla sindrome di Li–Fraumeni, in cui una copia difettosa di TP53 è presente in ogni cellula fin dalla nascita. Le persone con questa sindrome hanno centinaia di volte più probabilità di sviluppare osteosarcoma rispetto alla popolazione generale. Usando ampie raccolte di tessuti e dati cellulari dei pazienti, il team ha scandagliato migliaia di geni per trovare quelli condivisi tra campioni di Li–Fraumeni e tumori di osteosarcoma. Hanno scoperto un piccolo insieme di geni «ponte» la cui attività risultava alterata in entrambe le condizioni e che si raggruppavano in processi che controllano la divisione cellulare e la copia dei cromosomi — passaggi fondamentali che, quando perturbati, possono guidare il cancro.
STIL emerge come il principale colpevole
Applicando diversi metodi di machine learning, gli scienziati hanno ristretto questo gruppo di ponte a quattro geni chiave e ne hanno identificato uno di spicco: il gene STIL. Nei campioni di osteosarcoma, i livelli di STIL erano costantemente più alti nei tumori già metastatizzati, e i pazienti i cui tumori esprimevano più STIL tendevano ad avere una sopravvivenza più breve. Le analisi di vie biologiche hanno collegato l’elevato STIL a un intenso ciclo cellulare e a un aumento della degradazione proteica, mentre il basso STIL è risultato associato a segnali immunitari e infiammatori più forti. Questo quadro suggerisce che STIL non solo favorisce la divisione delle cellule del cancro osseo, ma può anche attenuare le difese naturali dell’organismo contro di esse.
Cellule simili a staminali, sistema immunitario silente
Per capire dove agisce STIL all’interno di un tumore, il team ha utilizzato il sequenziamento a singola cellula, che profila le singole cellule una per una. Hanno mappato più di 100.000 cellule da campioni di osteosarcoma e identificato diversi tipi di cellule maligne. STIL era particolarmente abbondante in un sottogruppo di cellule tumorali altamente «simili a staminali» che si trovavano all’inizio dei percorsi di sviluppo — cellule che sembrano seminare e sostenere il tumore. In queste cellule, l’elevato STIL era legato a segnali che favoriscono l’auto-rinnovamento, attivano gli osteoclasti che erodono lo scheletro e rimodellano le cellule immunitarie circostanti. I tumori ricchi di STIL mostravano meno cellule T citotossiche attive e molecole chiave per l’attivazione immunitaria, un modello che assomiglia a un «deserto immunitario» in cui il sistema immunitario non riconosce o non attacca efficacemente il cancro.
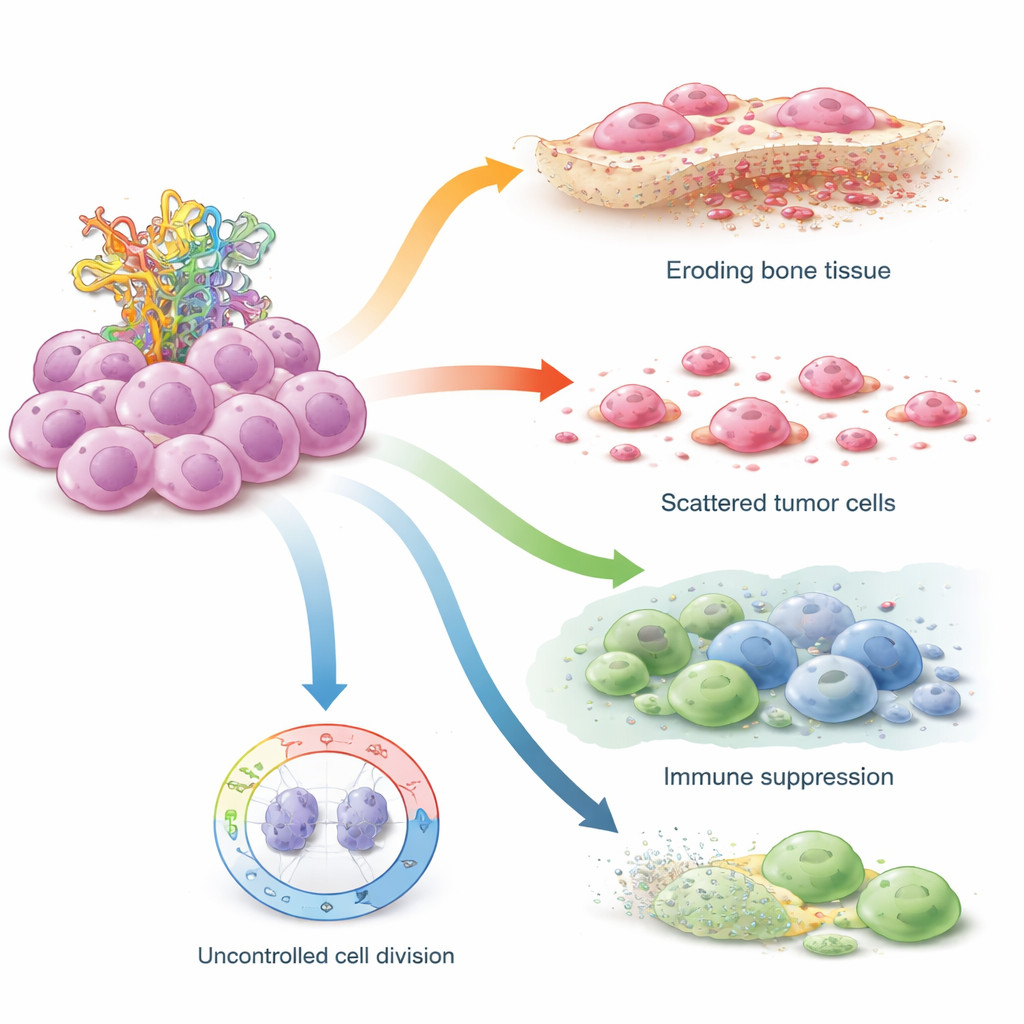
Come STIL mina i freni di sicurezza della cellula
I ricercatori hanno quindi testato STIL direttamente in linee cellulari di osteosarcoma coltivate in laboratorio, confrontando cellule con TP53 funzionante con altre portatrici di mutazioni TP53 che imitano la sindrome di Li–Fraumeni. Quando hanno usato piccoli RNA per spegnere STIL, i livelli della proteina p53 sono aumentati in entrambi i tipi cellulari e le cellule hanno formato meno colonie e meno sfere libere — un marcatore della ridotta capacità simile a quella staminale. Le cellule con TP53 funzionante si sono rivelate particolarmente sensibili, suggerendo che STIL normalmente agisca indebolendo la capacità di p53 di arrestare il ciclo cellulare. Nelle cellule con TP53 mutato, che hanno già una funzione p53 compromessa, il blocco di STIL ha comunque avuto un forte impatto sulla motilità: le cellule mutanti aggressive si muovevano e «riparavano» le ferite più lentamente una volta rimosso STIL, indicando che il loro comportamento invasivo dipende in larga misura da questo gene.
Implicazioni per trattamenti futuri più mirati
In termini concreti, questo lavoro dipinge STIL come un complice che aiuta i difetti ereditari di TP53 a trasformarsi in tumori ossei pericolosi. STIL allenta i freni di sicurezza interni della cellula e potenzia una piccola riserva di cellule tumorali simili a staminali che possono invadere l’osso, diffondersi in sedi distanti e nascondersi dall’attacco immunitario. Poiché l’alto STIL è anche collegato a una sensibilità alterata a certi farmaci — come gli inibitori di WEE1 che spingono cellule tumorali già instabili in divisioni letali — potrebbe servire come biomarcatore per abbinare i pazienti a terapie personalizzate. Pur richiedendo ulteriori studi per verificare queste idee nei pazienti, lo studio individua STIL come una nuova e promettente leva per comprendere e, in ultima analisi, disarmare l’osteosarcoma nelle famiglie affette dalla sindrome di Li–Fraumeni.
Citazione: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Parole chiave: Sindrome di Li-Fraumeni, osteosarcoma, TP53, STIL, cellule staminali tumorali