Clear Sky Science · pl
Analiza multi-omiczna ujawnia kluczową rolę STIL w zespole Li-Fraumeni i mięsakach kości
Gdy dziedziczne ryzyko spotyka nowotwór kości u dzieci
Niektóre rodziny przekazują sobie więcej niż kolor oczu czy wzrost — dziedziczą również znacznie większe ryzyko zachorowania na raka. Jednym z takich schorzeń jest zespół Li–Fraumeni, który znacząco zwiększa ryzyko wystąpienia mięsaków kości (osteosarcoma), rzadkiego, ale agresywnego nowotworu, często dotykającego dzieci i nastolatków. W tym badaniu postawiono istotne pytanie: poza słynnym „strażnikiem” genomu, genem TP53, jakie inne cząsteczki pomagają przekształcić to dziedziczne ryzyko w szybko rosnący, trudny do leczenia guz kości i czy mogą one stać się nowymi celami terapeutycznymi?
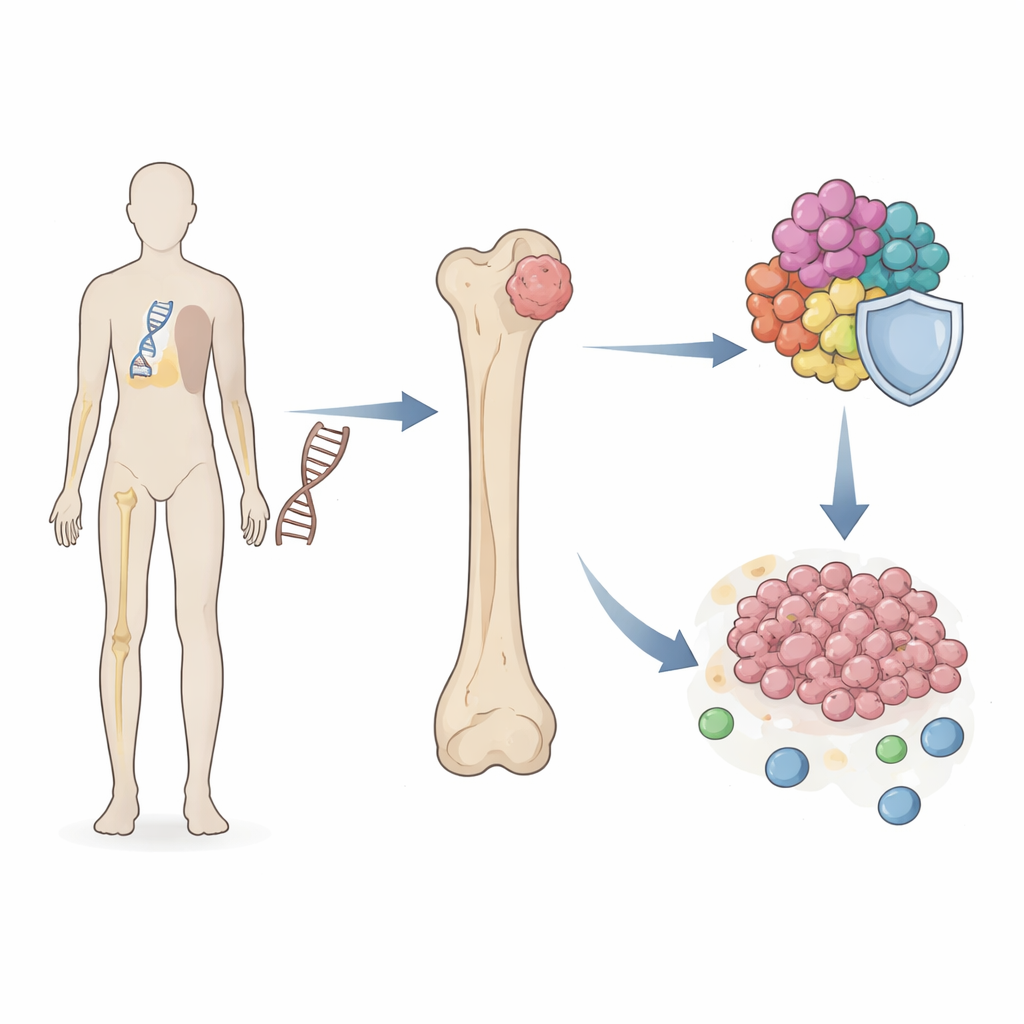
Ukryty łącznik między ryzykiem dziedzicznym a wzrostem guza
Naukowcy skupili się na zespole Li–Fraumeni, w którym wadliwa kopia TP53 występuje w każdej komórce od urodzenia. Osoby z tym zespołem mają setki razy większe ryzyko rozwoju osteosarcomy niż populacja ogólna. Wykorzystując duże zbiory próbek tkankowych i danych komórkowych od pacjentów, zespół przeskanował tysiące genów, aby znaleźć te wspólne dla próbek z Li–Fraumeni i guzów osteosarcoma. Odkryto niewielki zestaw „mostowych” genów, których aktywność była zmieniona w obu stanach i które grupowały się w procesach kontrolujących podział komórkowy i kopiowanie chromosomów — kluczowych etapach, których zaburzenie może napędzać nowotworzenie.
STIL ujawnia się jako centralny sprawca
Stosując kilka metod uczenia maszynowego, naukowcy zawęzili zestaw „mostowych” genów do czterech kluczowych i wyróżnili jeden gen: STIL. W próbkach osteosarcomy poziomy STIL były konsekwentnie wyższe w guzach, które już dały przerzuty, a pacjenci, których guzy wykazywały wyższą ekspresję STIL, mieli tendencję do krótszego przeżycia. Analizy szlaków wskazały, że wysoki poziom STIL wiąże się z intensywnym cyklem komórkowym i nasilonym rozkładem białek, podczas gdy niski STIL kojarzył się z silniejszymi sygnałami odpornościowymi i zapalnymi. Ten wzorzec sugeruje, że STIL nie tylko pomaga komórkom raka kości się dzielić, ale może także tłumić naturalne mechanizmy obronne organizmu przeciw tym komórkom.
Komórki o cechach macierzystych, uciszony układ odpornościowy
Aby ustalić, gdzie STIL działa wewnątrz guza, zespół sięgnął po sekwencjonowanie pojedynczych komórek, które profiluje komórki indywidualnie. Zamapowali ponad 100 000 komórek z próbek osteosarcomy i zidentyfikowali kilka typów złośliwych komórek. STIL występował szczególnie obficie w podgrupie wysoce „macierzystych” komórek nowotworowych, które znajdowały się na początku ścieżek rozwojowych — komórek, które wydają się zasiewać i podtrzymywać nowotwór. W tych komórkach wysoki STIL wiązał się z sygnałami sprzyjającymi samoodnawianiu, aktywacją osteoklastów rozpuszczających kość oraz przekształcaniem otaczających komórek układu odpornościowego. Guzy bogate w STIL wykazywały mniejszą liczbę aktywnych limfocytów T zabójczych i niższe poziomy kluczowych molekuł aktywujących odporność — wzorzec przypominający „pustynię immunologiczną”, w której układ odpornościowy nie rozpoznaje lub nie atakuje skutecznie nowotworu.
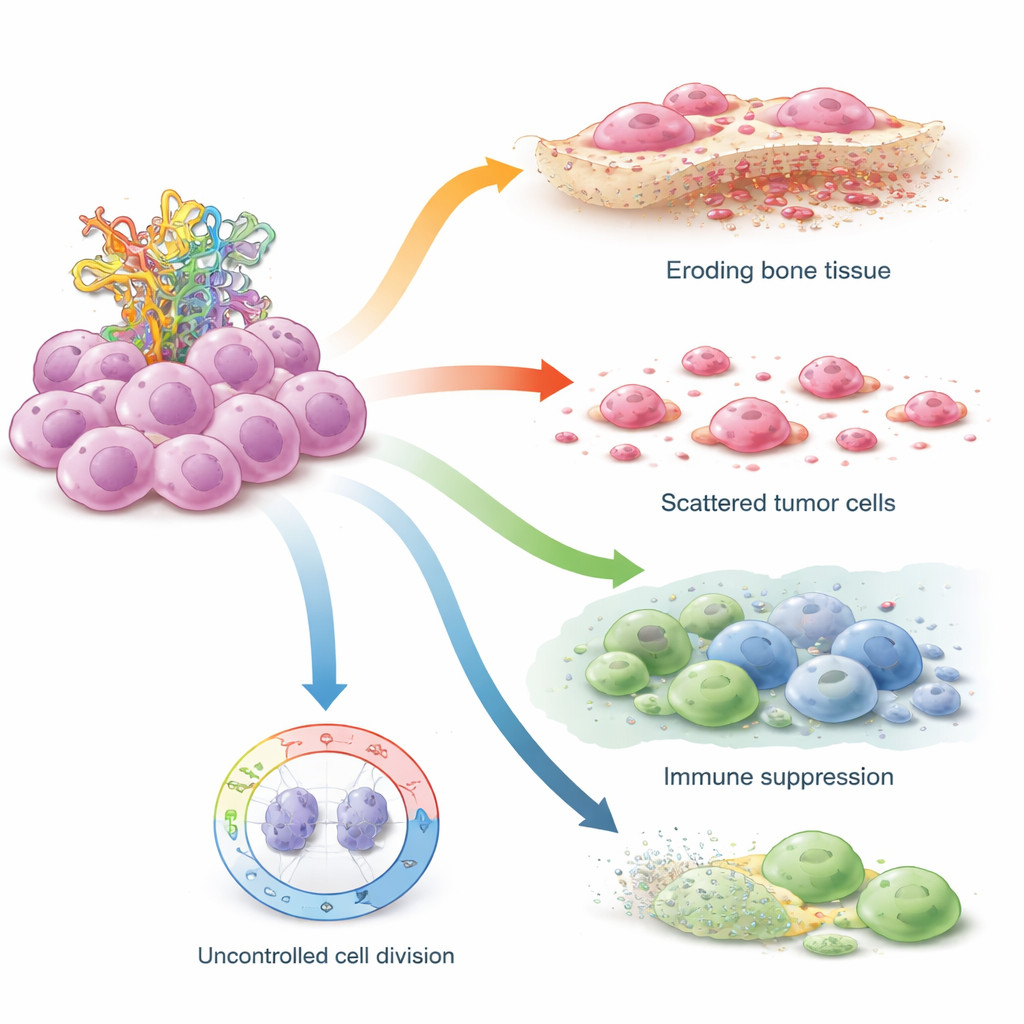
Jak STIL podważa hamulce bezpieczeństwa komórki
Następnie badacze przetestowali STIL bezpośrednio w liniach komórkowych osteosarcomy hodowanych w laboratorium, porównując komórki z prawidłowym TP53 z tymi noszącymi mutacje TP53 naśladujące zespół Li–Fraumeni. Gdy użyto krótkich cząsteczek RNA do wyłączenia STIL, poziomy białka p53 wzrosły w obu typach komórek, a komórki tworzyły mniej kolonii i mniej unoszących się sfer — objaw zmniejszonego zachowania podobnego do komórek macierzystych. Komórki z funkcjonalnym TP53 były szczególnie wrażliwe, co sugeruje, że STIL normalnie osłabia zdolność p53 do zatrzymywania cyklu komórkowego. W komórkach z mutacją TP53, które już nie mają pełnej funkcji p53, blokada STIL nadal miała silny wpływ na zdolność ruchu: agresywne komórki z mutacjami poruszały się i „zasklepiały” rany wolniej po usunięciu STIL, co wskazuje, że ich inwazyjne zachowanie w dużej mierze zależy od tego genu.
Implikacje dla przyszłych, bardziej precyzyjnych terapii
Mówiąc prosto, to badanie przedstawia STIL jako wspólnika, który pomaga dziedzicznym defektom TP53 rozwinąć się w niebezpieczne nowotwory kości. STIL zarówno poluzowuje wewnętrzne hamulce bezpieczeństwa komórki, jak i wzmacnia małą pulę komórek o cechach macierzystych, które mogą naciekać kość, rozprzestrzeniać się i ukrywać przed atakiem układu odpornościowego. Ponieważ wysoki poziom STIL wiąże się także ze zmienioną wrażliwością na niektóre leki — na przykład inhibitory WEE1, które zmuszają już niestabilne komórki nowotworowe do zabójczych podziałów — może on służyć jako biomarker do dopasowania pacjentów do spersonalizowanych terapii. Choć potrzebne są dalsze badania, by sprawdzić te koncepcje u pacjentów, studium podkreśla STIL jako obiecujący punkt zaczepienia do zrozumienia i w końcu obezwładnienia osteosarcomy w rodzinach dotkniętych zespołem Li–Fraumeni.
Cytowanie: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Słowa kluczowe: zespół Li-Fraumeni, mięsak kości, TP53, STIL, komórki macierzyste nowotworu