Clear Sky Science · tr
Çoklu omiks analizi, Li‑Fraumeni sendromu ve osteosarkomda STIL’in kilit rolünü ortaya koyuyor
Miras Kalan Risk Çocukluk Çağı Kemik Kanseriyle Buluştuğunda
Bazı aileler sadece göz rengi veya boy değil, aynı zamanda kanser gelişme olasılığında çok daha yüksek bir yatkınlık da aktarır. Bu durumlardan biri olan Li–Fraumeni sendromu, nadir ama saldırgan bir kemik kanseri olan osteosarkom riskini büyük ölçüde artırır; genellikle çocukları ve gençleri etkiler. Bu çalışma, sıkça anılan “koruyucu” gen TP53’nin ötesinde, bu kalıtsal riski hızlı büyüyen, tedavisi zor bir kemik tümörüne dönüştürmeye yardımcı olan hangi moleküllerin bulunduğu ve bunların yeni tedavi hedefleri olup olamayacağı sorusunu ele alıyor.
Kalıtsal Risk ile Tümör Büyümesi Arasındaki Gizli Bağlayıcı
Araştırmacılar, kusurlu bir TP53 kopyasının doğuştan her hücrede bulunduğu Li–Fraumeni sendromuna odaklandı. Bu sendroma sahip kişiler, genel nüfusa kıyasla osteosarkom geliştirme olasılığı yüzlerce kat daha yüksektir. Geniş hasta doku ve hücre veri setlerini kullanarak ekip, Li–Fraumeni örnekleri ile osteosarkom tümörleri arasında paylaşılan genleri bulmak için binlerce geni taradı. Her iki durumda da etkinliği değişmiş ve hücre bölünmesi ile kromozom kopyalanmasını kontrol eden süreçlerde kümelenen, kanseri tetikleyebilecek ana adımlara bağlı küçük bir “köprü” gen seti keşfettiler.
STIL Merkezi Sorunlu Oyuncu Olarak Öne Çıkıyor
Çeşitli makine öğrenmesi yöntemleri uygulayarak bilim insanları bu köprü setini dört ana gende daralttı ve öne çıkan bir gen buldu: STIL. Osteosarkom örneklerinde STIL düzeyleri, zaten yayılmış olan tümörlerde tutarlı şekilde daha yüksekti ve tümörleri daha fazla STIL üreten hastaların yaşama süreleri genellikle daha kısaydı. Yolak analizleri yüksek STIL’i hızlı hücre döngüsü ve protein yıkımı ile ilişkilendirirken, düşük STIL daha güçlü bağışıklık ve inflamasyon sinyalleriyle bağlantılıydı. Bu desen, STIL’in sadece kemik kanseri hücrelerinin bölünmesini desteklemekle kalmayıp aynı zamanda vücudun doğal savunmalarını da zayıflatabileceğini düşündürdü.
Kök Hücremsi Hücreler, Sessiz İmmün Sistem
STIL’in bir tümör içinde nerede etkili olduğunu görmek için ekip tek hücre dizilemeye yöneldi; bu yöntem tek tek hücreleri profilleştirir. Osteosarkom örneklerinden 100.000’den fazla hücreyi haritaladılar ve birkaç malign hücre tipi tanımladılar. STIL özellikle gelişim yollarının başlangıcında yer alan ve kanseri tohumlayıp sürdüren gibi görünen yüksek oranda “kök hücremsi” tümör hücrelerinin bir alt kümesinde boldu. Bu hücrelerde yüksek STIL, öz‑yenilenmeyi teşvik eden, iskeleti aşındıran kemik yiyici hücreleri (osteoklastları) aktive eden ve çevresindeki bağışıklık hücrelerini yeniden şekillendiren sinyallerle ilişkilendirildi. STIL bakımından zengin tümörler daha az aktif öldürücü T hücresi ve önemli immün aktive edici molekül gösteriyordu; bu desen, bağışıklık sisteminin kanseri etkin şekilde tanıyamadığı veya saldırmadığı bir “immün çöl”e benziyordu.
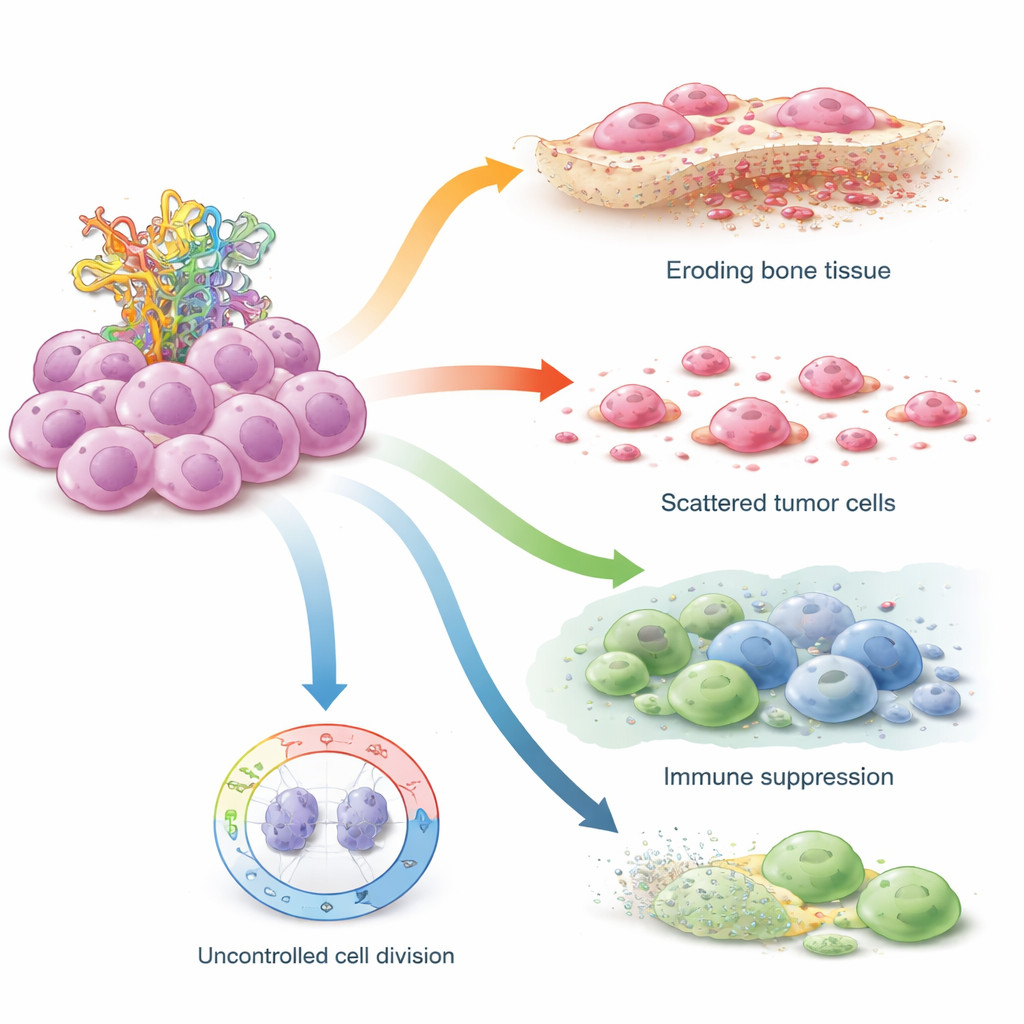
STIL Hücrenin Güvenlik Frenlerini Nasıl Aşındırıyor
Araştırmacılar daha sonra STIL’i laboratuvarda yetiştirilen osteosarkom hücre hatlarında doğrudan test etti; bunlar normal TP53 taşıyan hücrelerle Li–Fraumeni sendromunu taklit eden TP53 mutasyonlarını içeren hücrelerle karşılaştırıldı. Küçük RNA molekülleri kullanarak STIL’i kapattıklarında, her iki hücre tipinde de p53 proteini düzeyleri yükseldi ve hücreler daha az koloni ve daha az serbest yüzen küre oluşturdular—bu, kök hücremsi davranışta azalma belirtisidir. Çalışan TP53’ye sahip hücreler özellikle duyarlıydı; bu, STIL’in normalde p53’ün hücre döngüsünü durdurma yeteneğini zayıflatmaya hizmet ettiğini düşündürür. Zaten tam p53 fonksiyonundan yoksun olan TP53‑mutant hücrelerde bile STIL blokajı hareketlilik üzerinde güçlü bir etki yaptı: agresif mutant hücreler STIL ortadan kaldırıldığında daha yavaş hareket etti ve “yaraları” daha yavaş kapattı; bu, invaziv davranışlarının büyük ölçüde bu gene bağımlı olduğunu gösterir.
Gelecekte Daha Hassas Tedaviler İçin Çıkarımlar
Günlük ifadeyle, bu çalışma STIL’i kalıtsal TP53 kusurlarının tehlikeli kemik kanserlerine dönüşmesine yardımcı olan bir suç ortağı olarak resmediyor. STIL hem hücrenin iç güvenlik frenlerini gevşetiyor hem de kemiğe saldırıp uzak bölgelere yayılabilen ve immün saldırıdan saklanabilen küçük bir kök hücremsi tümör hücresi havuzunu güçlendiriyor. Yüksek STIL aynı zamanda belirli ilaçlara karşı duyarlılık değişiklikleriyle—örneğin zaten kararsız kanser hücrelerini ölümcül bölünmelere iten WEE1 inhibitörleri gibi—ilişkili olduğundan, hastaları kişiselleştirilmiş tedavilerle eşleştirebilecek bir biyobelirteç olarak hizmet edebilir. Bu fikirleri hastalarda test etmek için daha fazla çalışma gerekse de, çalışma Li–Fraumeni sendromu yaşayan ailelerde osteosarkomu anlamak ve nihayetinde etkisiz hale getirmek için STIL’i umut verici bir yeni tutacak olarak öne çıkarıyor.
Atıf: Qiao, Y., Hao, J., Yuan, F. et al. Multi-omics analysis reveals the key role of STIL in Li-Fraumeni syndrome and osteosarcoma. npj Precis. Onc. 10, 159 (2026). https://doi.org/10.1038/s41698-026-01432-y
Anahtar kelimeler: Li‑Fraumeni sendromu, osteosarkom, TP53, STIL, kanser kök hücreleri