Clear Sky Science · zh
GLUD1通过对抗失锚性凋亡并通过ARAF/MEK/ERK信号通路促进卵巢癌进展
这项研究为何重要
卵巢癌常在已悄然扩散到腹腔后才被发现,使其成为影响女性的最致命癌症之一。这种扩散依赖于从卵巢脱落、在腹腔液中漂浮且即便失去与周围组织的锚定仍能存活的癌细胞。本文所述的研究揭示了一种关键的辅助分子,它使这些漂流的细胞能够抵抗细胞死亡并播种新的肿瘤,为未来医生阻止癌症转移提出了新的思路。
漂流的癌细胞如何躲避死亡
大多数健康细胞必须保持附着;一旦失去附着,它们会启动一种称为“失锚性凋亡”的自毁程序。然而,腹腔内的卵巢癌细胞会聚集成小球,能够在无附着的情况下存活,并能在之后附着到新的表面。研究人员筛查了大型基因表达数据库,重点关注与死亡抗性和氨基酸代谢相关的基因。其中一个基因GLUD1显著突出:它在卵巢肿瘤中的表达高于正常组织,尤其是在来自转移灶的样本中。患者中较高的GLUD1水平与整体生存期缩短和疾病更快复发密切相关,提示该分子有助于肿瘤进展。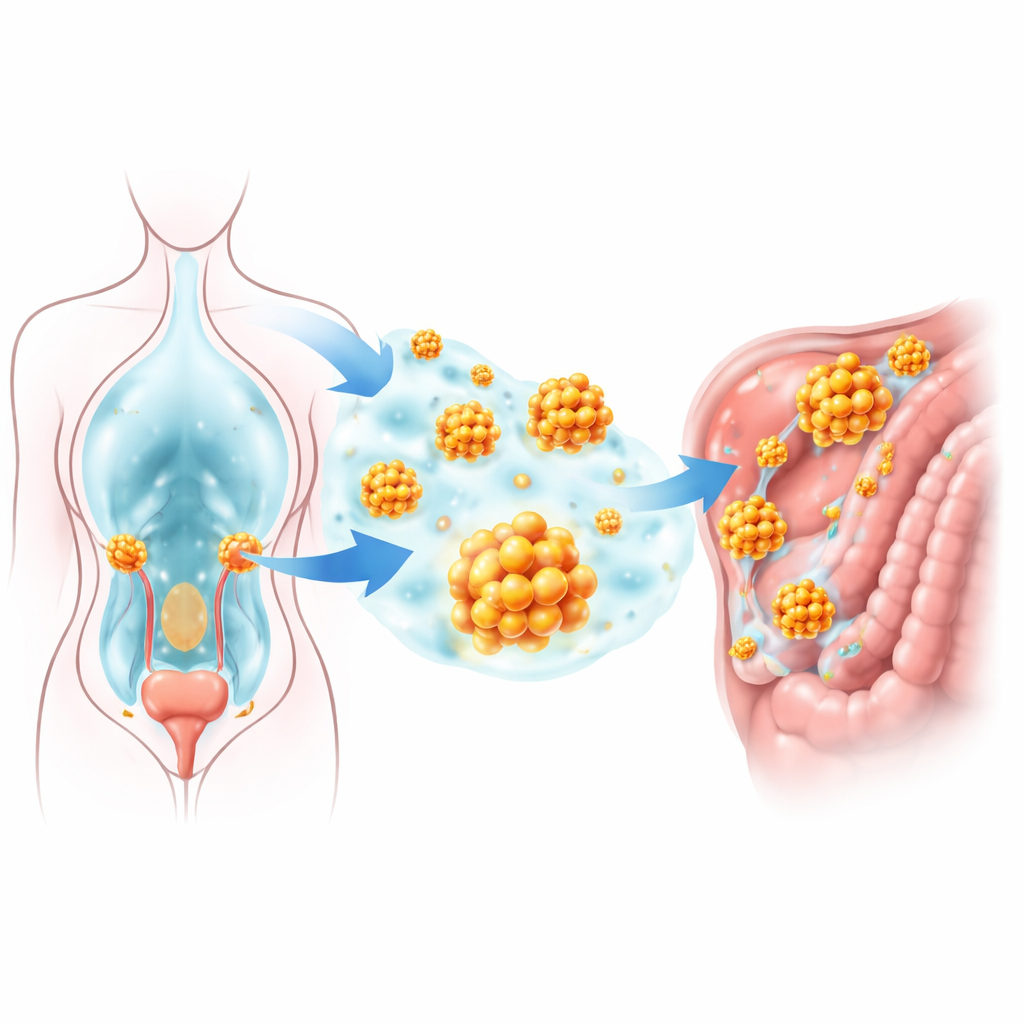
肿瘤扩散中的隐秘同谋
为了超越统计关联,研究团队在体外培养的卵巢癌细胞系中操纵GLUD1的表达。降低GLUD1时,悬浮的细胞团变小,细胞在悬浮状态下更容易死亡,细胞在常规迁移实验中的迁移能力也下降。提高GLUD1则出现相反现象:细胞更能抵抗死亡并表现出更强的迁移性。在腹腔内注入卵巢癌细胞的小鼠模型中,沉默GLUD1导致诸如脾脏和肝脏等器官上的肿瘤结节减少、肿瘤生长放缓且小鼠存活期延长。来自这些小鼠的肿瘤样本显示更多死亡细胞和更少分裂细胞,进一步支持GLUD1对于使脱离的癌细胞在形成新病灶前保持存活至关重要的观点。
癌细胞内的保护性伙伴关系
接着,研究者探究GLUD1如何发挥这种保命作用。通过蛋白质互作筛查,他们发现GLUD1与另一种蛋白ARAF有物理结合,后者是驱动细胞存活与生长的著名信号级联的一部分。在癌细胞内,GLUD1和ARAF主要共同存在于细胞质而非产生能量的细胞器中,提示其可能参与信号传导。当降低GLUD1时,ARAF水平下降,而其近亲BRAF和CRAF则无明显变化。ARAF减少伴随下游MEK/ERK通路活性减弱以及趋向促死蛋白的变化。将ARAF重新引入GLUD1缺失的细胞能显著恢复存活信号并减少细胞死亡,表明ARAF是连接GLUD1与抗失锚性凋亡作用之间的关键中介。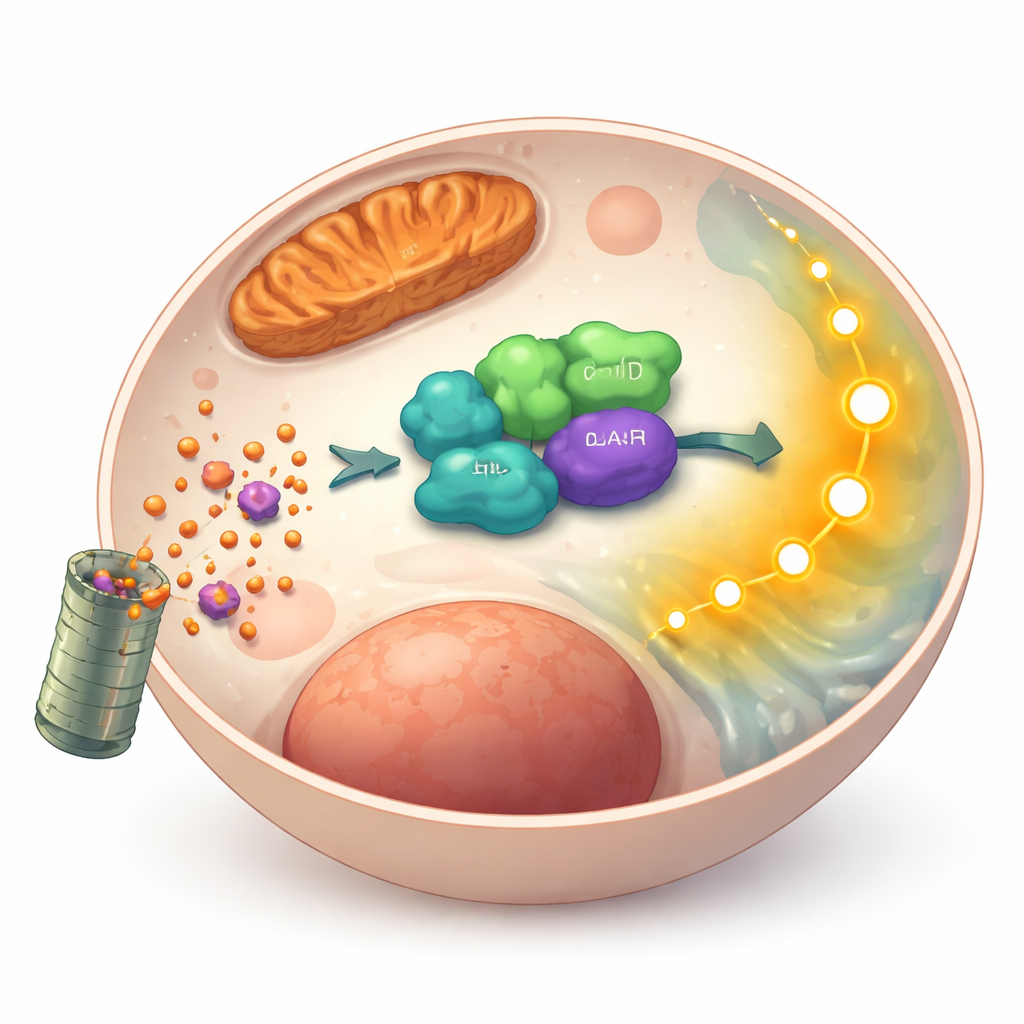
GLUD1如何保护关键信号
进一步研究表明,GLUD1像保镖一样防止ARAF被细胞的蛋白质回收系统标记并降解。当用化学方法阻断该回收机制时,GLUD1缺失后ARAF的下降被逆转。时间过程实验显示,在缺失GLUD1时ARAF的降解速度明显加快,生化检测也显示ARAF被更多地“标记”以便被清除。过表达GLUD1会减少这些标记。综合结果表明,GLUD1通过阻断ARAF的降解来稳定它,从而在脱离的卵巢癌细胞中维持存活信号。有趣的是,尽管GLUD1最为人知的是在谷氨酰胺代谢中的作用,补回其代谢产物之一仅能部分恢复ARAF及其信号,提示在此情境下GLUD1对蛋白的保护作用至少与其酶学活性一样重要。
这对未来治疗可能意味着什么
通过揭示GLUD1如何保护ARAF并维持存活通路活性,这项研究暴露了游离卵巢癌细胞生命周期中的一个脆弱点。如果能开发出减弱GLUD1对ARAF稳定作用的药物——或阻断下游MEK/ERK信号——可能会迫使脱落的癌细胞进入失锚性凋亡,而非在腹腔内形成新肿瘤。由于GLUD1在正常细胞代谢中也发挥核心作用,此类治疗需要谨慎权衡疗效与副作用。不过,发现这一GLUD1–ARAF伙伴关系为理解卵巢癌如何扩散提供了更清晰的地图,并突出了若干有希望的分子靶点,旨在在疾病在全身播散前阻止其扎根扩展。
引用: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
关键词: 卵巢癌, 转移, 失锚性凋亡耐受, GLUD1, 细胞存活信号