Clear Sky Science · de
GLUD1 unterstützt das Fortschreiten von Eierstockkrebs, indem es Anoikis über ARAF/MEK/ERK-Signalweg entgegenwirkt
Warum diese Forschung wichtig ist
Eierstockkrebs wird häufig erst entdeckt, nachdem er sich still im Bauchraum ausgebreitet hat, weshalb er zu den tödlichsten Krebserkrankungen bei Frauen gehört. Diese Ausbreitung beruht auf Krebszellen, die sich von den Eierstöcken lösen, in der Bauchflüssigkeit schweben und dennoch überleben, obwohl sie nicht mehr an das umgebende Gewebe gebunden sind. Die zugrunde liegende Studie identifiziert ein zentrales Helfermolekül, das diesen treibenden Zellen erlaubt, dem Zelltod zu widerstehen und neue Tumoren zu begründen, und liefert damit neue Ansatzpunkte dafür, wie Ärzte die Ausbreitung des Krebses künftig stoppen könnten.
Wie wandernde Krebszellen dem Tod entkommen
Die meisten gesunden Zellen müssen an ihrer örtlichen Stützstruktur haften; verlieren sie diesen Halt, aktivieren sie ein Selbstzerstörungsprogramm, das als „Anoikis“ bezeichnet wird. Eierstockkrebszellen in der Bauchhöhle hingegen bilden kleine Kugelansammlungen, die ohne Anheftung überleben und später an neuen Oberflächen haften können. Die Forschenden durchsuchten große Genexpressionsdatenbanken mit Fokus auf Gene, die sowohl mit Todesresistenz als auch mit Aminosäurestoffwechsel verknüpft sind. Ein Gen, GLUD1, hob sich deutlich ab: Es war in Eierstocktumoren stärker aktiv als im Normalgewebe, besonders in Proben von metastatischen Stellen. Höhere GLUD1-Werte bei Patientinnen korrelierten stark mit kürzerem Gesamtüberleben und schnellerem Rückfall, was darauf hindeutet, dass dieses Molekül das Fortschreiten von Tumoren fördert. 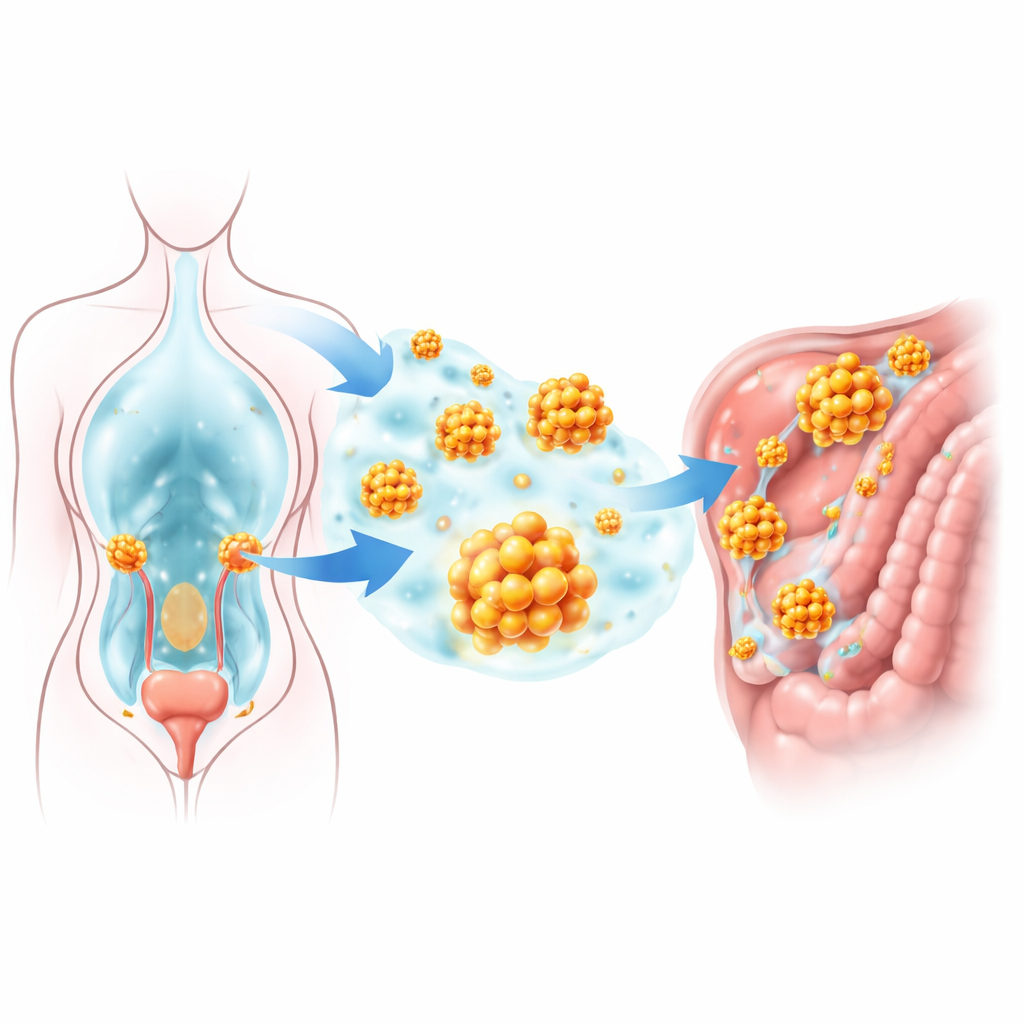
Ein verborgener Komplize bei der Tumorausbreitung
Um über statistische Zusammenhänge hinauszugehen, veränderte das Team die GLUD1-Spiegel in im Labor gezüchteten Zelllinien von Eierstockkrebs. Bei Reduktion von GLUD1 schrumpften frei schwebende Zellcluster, Krebszellen starben im Schwebestatus leichter und die Zellen zeigten in Standard-Migrationsassays eine verringerte Wanderfähigkeit. Bei verstärkter GLUD1-Expression trat das Gegenteil auf: Die Zellen widerstanden dem Tod und bewegten sich aggressiver. In Mäusen, denen Eierstockkrebszellen in die Bauchhöhle injiziert worden waren, führte das Abschalten von GLUD1 zu weniger Tumorknoten auf Organen wie Milz und Leber, zu langsamerem Tumorwachstum und zu längerer Überlebenszeit. Tumorproben dieser Mäuse zeigten mehr sterbende und weniger teilende Zellen, was die Idee stärkt, dass GLUD1 entscheidend dafür ist, gelöste Krebszellen lange genug am Leben zu erhalten, damit sie neue Kolonien bilden können.
Eine schützende Partnerschaft innerhalb der Krebszellen
Die Forschenden fragten dann, wie GLUD1 diesen überlebensfördernden Effekt ausübt. Mit Methoden zur Proteinsuche entdeckten sie, dass GLUD1 physisch an ein anderes Protein namens ARAF bindet, das Teil einer bekannten Signalkette ist, die Zellüberleben und -wachstum antreibt. Innerhalb der Krebszellen befinden sich GLUD1 und ARAF überwiegend im Zellplasma und nicht in energieproduzierenden Organellen, was auf eine Signalübertragungsfunktion hinweist. Bei vermindertem GLUD1 sanken die ARAF-Spiegel, während die verwandten Proteine BRAF und CRAF unverändert blieben. Dieser ARAF-Verlust ging einher mit abgeschwächter Aktivität im nachgeschalteten MEK/ERK-Weg und einer Verschiebung hin zu pro-apoptotischen Proteinen. Die Wiedereinführung von ARAF in GLUD1-defiziente Zellen stellte einen Großteil der Überlebenssignale wieder her und verringerte den Zelltod, womit gezeigt wurde, dass ARAF eine wichtige Vermittlerrolle zwischen GLUD1 und der Anoikis-Resistenz einnimmt. 
Wie GLUD1 ein zentrales Signal schützt
Tiefergehende Untersuchungen ergaben, dass GLUD1 wie ein Leibwächter wirkt, der verhindert, dass ARAF vom zellulären Proteinfaltungs- und -recycling-System markiert und abgebaut wird. Wenn dieses Recycling- bzw. Abbausystem chemisch blockiert wurde, kehrte der nach GLUD1-Verlust beobachtete ARAF-Abfall um. Zeitverlaufsexperimente zeigten, dass ARAF deutlich schneller abgebaut wurde, wenn GLUD1 fehlte, und biochemische Tests offenbarten eine stärkere Markierung von ARAF für die Entsorgung. Eine Überexpression von GLUD1 verringerte diese Markierungen. Zusammengenommen deuten die Ergebnisse darauf hin, dass GLUD1 ARAF stabilisiert, indem es dessen Abbau verhindert und so das Überlebenssignal in losgelösten Eierstockkrebszellen aufrechterhält. Interessanterweise ist GLUD1 zwar vor allem dafür bekannt, beim Abbau der Aminosäure Glutamin zu helfen; das Zurückgeben eines seiner Stoffwechselprodukte konnte ARAF und dessen Signalaktivität jedoch nur teilweise wiederherstellen, was nahelegt, dass die protektive Rolle von GLUD1 gegenüber Proteinen in diesem Zusammenhang mindestens ebenso wichtig ist wie seine enzymatische Aktivität.
Was das für zukünftige Behandlungen bedeuten könnte
Indem sie offenlegen, wie GLUD1 ARAF schützt und Überlebenswege aktiv hält, macht diese Studie einen verwundbaren Punkt im Lebenszyklus wandernder Eierstockkrebszellen sichtbar. Wenn Medikamente entwickelt werden könnten, die den stabilisierenden Effekt von GLUD1 auf ARAF abschwächen — oder die nachgeschalteten MEK/ERK-Signale blockieren —, könnten sie gelöste Krebszellen dazu zwingen, Anoikis zu durchlaufen, anstatt neue Tumoren im Bauchraum zu bilden. Da GLUD1 auch zentrale Rollen im normalen Zellstoffwechsel spielt, müsste eine solche Behandlung Vor- und Nachteile sorgfältig abwägen. Dennoch liefert die Entdeckung der GLUD1–ARAF-Partnerschaft eine klarere Karte dafür, wie sich Eierstockkrebs ausbreitet, und hebt eine vielversprechende Gruppe molekularer Ziele für Therapien hervor, die darauf abzielen, die Krankheit zu stoppen, bevor sie sich im Körper festsetzt.
Zitation: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Schlüsselwörter: Eierstockkrebs, Metastasen, Anoikis-Resistenz, GLUD1, zelluläre Überlebenssignale