Clear Sky Science · it
GLUD1 favorisce la progressione del cancro ovarico contrastando l'anoikis tramite la via ARAF/MEK/ERK
Perché questa ricerca è importante
Il cancro ovarico viene spesso scoperto solo dopo essersi diffuso silenziosamente nella cavità addominale, rendendolo uno dei tumori più letali nelle donne. Questa diffusione dipende da cellule tumorali che si staccano dall’ovaio, fluttuano nel liquido addominale e riescono comunque a sopravvivere pur non essendo più ancorate ai tessuti circostanti. Lo studio alla base di questo articolo individua una molecola chiave che permette a queste cellule in sospensione di resistere alla morte cellulare e dare origine a nuovi tumori, suggerendo nuove idee su come i medici potrebbero in futuro impedire la diffusione del cancro.
Come le cellule tumorali vagabonde sfuggono alla morte
La maggior parte delle cellule sane deve restare attaccata alla propria struttura di supporto; quando perdono quell’ancoraggio avviano un programma di autodistruzione noto come “anoikis”. Le cellule di cancro ovarico nella cavità addominale, però, si aggregano in piccoli sfere che sopravvivono senza attaccamento e possono poi aderire a nuove superfici. I ricercatori hanno analizzato grandi banche dati di espressione genica, concentrandosi sui geni collegati sia alla resistenza alla morte cellulare sia all’utilizzo degli amminoacidi. Un gene, chiamato GLUD1, è emerso chiaramente: era più attivo nei tumori ovarici rispetto al tessuto normale, in particolare nei campioni prelevati da siti metastatici. Livelli più elevati di GLUD1 nei pazienti risultavano fortemente associati a una sopravvivenza complessiva più breve e a una recidiva più rapida della malattia, suggerendo che questa molecola favorisca la progressione tumorale. 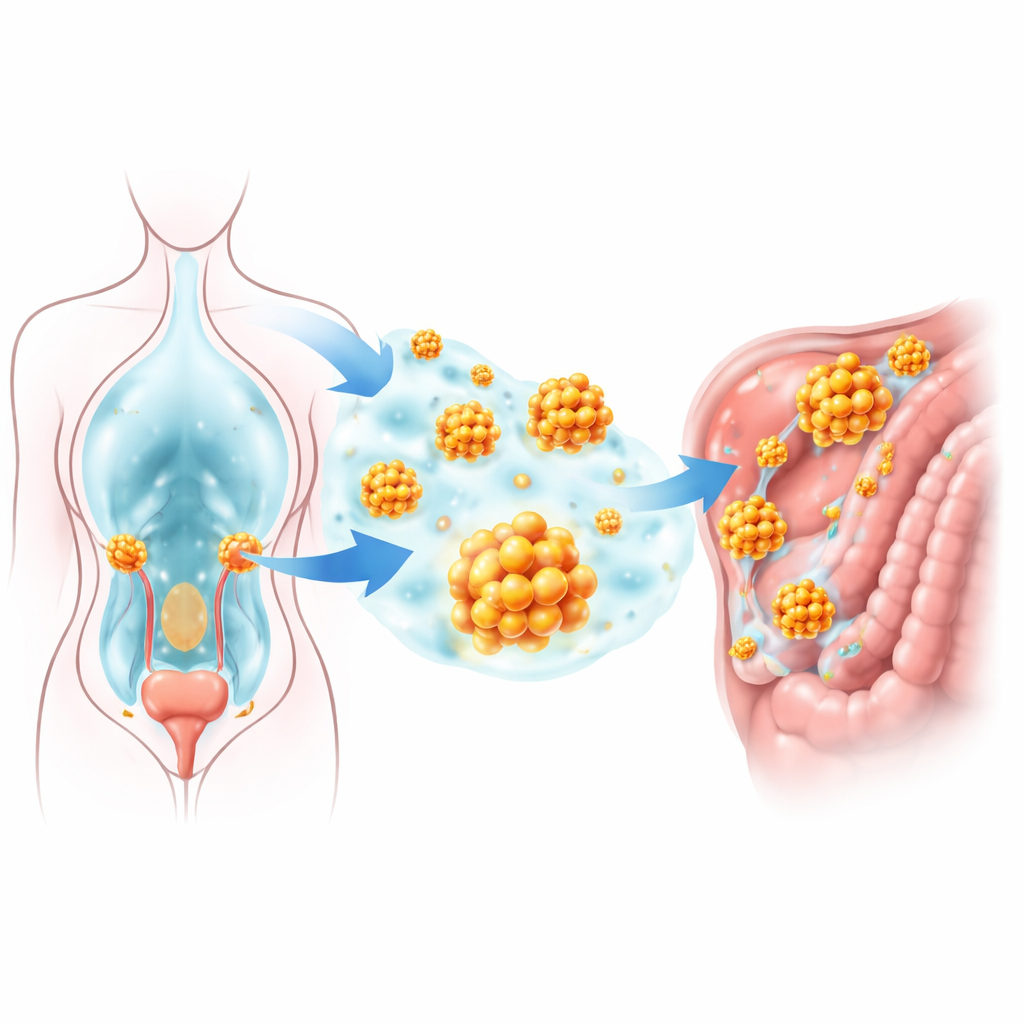
Un complice nascosto nella diffusione tumorale
Per andare oltre i semplici legami statistici, il team ha manipolato i livelli di GLUD1 in linee cellulari di cancro ovarico coltivate in laboratorio. Quando hanno ridotto GLUD1, gli ammassi cellulari liberi si sono rimpiccioliti, le cellule tumorali sono morte più facilmente in sospensione e la loro capacità di migrare nei test standard è diminuita. Quando hanno aumentato GLUD1, è successo il contrario: le cellule hanno resistito alla morte e si sono mosse più aggressivamente. In topi in cui sono state iniettate cellule di cancro ovarico nella cavità addominale, il silenziamento di GLUD1 ha portato a un numero ridotto di noduli tumorali su organi come milza e fegato, a una crescita tumorale più lenta e a una sopravvivenza prolungata. I campioni tumorali di questi animali mostravano più cellule in morte e meno cellule in divisione, rafforzando l’idea che GLUD1 sia cruciale per mantenere vive le cellule tumorali staccate abbastanza a lungo da formare nuove colonie.
Un partenariato protettivo all’interno delle cellule tumorali
I ricercatori hanno quindi indagato come GLUD1 eserciti questa influenza salvavita. Utilizzando metodi per cercare interazioni proteiche, hanno scoperto che GLUD1 si lega fisicamente a un’altra proteina chiamata ARAF, parte di una nota cascata di segnali che promuove la sopravvivenza e la crescita cellulare. Nelle cellule tumorali, GLUD1 e ARAF si trovano insieme soprattutto nel citoplasma piuttosto che negli organelli produttori di energia, suggerendo un ruolo nella segnalazione. Quando GLUD1 è stato ridotto, i livelli di ARAF sono diminuiti, mentre i suoi stretti parenti BRAF e CRAF sono rimasti invariati. Questa perdita di ARAF è stata accompagnata da una minore attività della via MEK/ERK a valle e da uno spostamento verso proteine pro‑morte. Reintrodurre ARAF nelle cellule carenti di GLUD1 ha ripristinato gran parte della segnalazione di sopravvivenza e ridotto la morte cellulare, mostrando che ARAF è un importante mediatore che collega GLUD1 alla resistenza all’anoikis. 
Come GLUD1 protegge un segnale chiave
Approfondendo, il gruppo ha scoperto che GLUD1 funziona come una scorta che impedisce ad ARAF di essere etichettato e degradato dal sistema di riciclo proteico della cellula. Quando questo meccanismo di riciclo è stato bloccato chimicamente, il calo di ARAF osservato dopo la perdita di GLUD1 è stato invertito. Esperimenti a tempo hanno mostrato che ARAF decadrebbe molto più rapidamente in assenza di GLUD1, e test biochimici hanno rivelato una maggiore «etichettatura» di ARAF per la degradazione. L’iperespressione di GLUD1 ha ridotto questi segni. Nel complesso, i risultati indicano che GLUD1 stabilizza ARAF bloccandone la degradazione, mantenendo così attivo il segnale di sopravvivenza nelle cellule ovariche distaccate. È interessante che, sebbene GLUD1 sia più noto per il suo ruolo nel metabolismo del glutammato, reintegrare uno dei suoi prodotti metabolici abbia ripristinato solo parzialmente ARAF e la sua segnalazione, suggerendo che il ruolo di GLUD1 nella protezione delle proteine è almeno importante quanto la sua attività enzimatica in questo contesto.
Cosa potrebbe significare per i trattamenti futuri
Rivelando come GLUD1 protegge ARAF e mantiene attive le vie di sopravvivenza, questo studio espone un punto vulnerabile nel ciclo vitale delle cellule tumorali ovariche vaganti. Se si riuscisse a sviluppare farmaci in grado di attenuare l’effetto stabilizzante di GLUD1 su ARAF — o di bloccare i segnali MEK/ERK a valle — si potrebbe indurre le cellule tumorali distaccate a subire l’anoikis anziché formare nuovi tumori nell’addome. Poiché GLUD1 svolge anche ruoli centrali nel metabolismo delle cellule normali, un trattamento del genere dovrebbe bilanciare attentamente benefici ed effetti collaterali. Tuttavia, la scoperta di questa partnership GLUD1–ARAF offre una mappa più chiara di come il cancro ovarico si diffonde e mette in luce un promettente insieme di bersagli molecolari per terapie mirate a fermare la malattia prima che si radichi in tutto il corpo.
Citazione: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Parole chiave: cancro ovarico, metastasi, resistenza all'anoikis, GLUD1, segnalazione per la sopravvivenza cellulare