Clear Sky Science · nl
GLUD1 ondersteunt de progressie van eierstokkanker door anoikis tegen te werken via ARAF/MEK/ERK-signaaltransductie
Waarom dit onderzoek ertoe doet
Eierstokkanker wordt vaak pas ontdekt nadat het zich stilletjes door de buikholte heeft verspreid, waardoor het een van de dodelijkste vormen van kanker bij vrouwen is. Deze verspreiding berust op kankercellen die losraken van de eierstok, in het buikvocht rondzweven en toch weten te overleven hoewel ze niet langer aan het omringende weefsel vastzitten. De studie achter dit artikel ontmaskert een belangrijke hulpstof die deze zwerfende cellen in staat stelt celdood te weerstaan en nieuwe tumoren te vormen, en biedt daarmee nieuwe invalshoeken voor hoe artsen mogelijk de verdere uitzaaiing kunnen stoppen.
Hoe zwerfcellen de dood omzeilen
De meeste gezonde cellen moeten aan hun lokale steunstructuur vastzitten; wanneer ze dat contact verliezen, zetten ze een zelfvernietigingsprogramma in gang dat bekendstaat als “anoikis.” Eierstokkankercellen in de buikholte clusteren echter tot kleine bolletjes die zonder bevestiging kunnen overleven en later aan nieuwe oppervlakken kunnen hechten. De onderzoekers doorzochten grote genexpressiedatabases, met de nadruk op genen die zowel met resistentie tegen celdood als met aminozuurgebruik te maken hebben. Eén gen, GLUD1, sprong er duidelijk uit: het was actiever in eierstoktumoren dan in normaal weefsel, vooral in monsters afkomstig van metastatische locaties. Hogere GLUD1-niveaus bij patiënten waren sterk geassocieerd met een kortere algehele overleving en snellere terugkeer van de ziekte, wat suggereert dat dit molecuul tumorgroei bevordert. 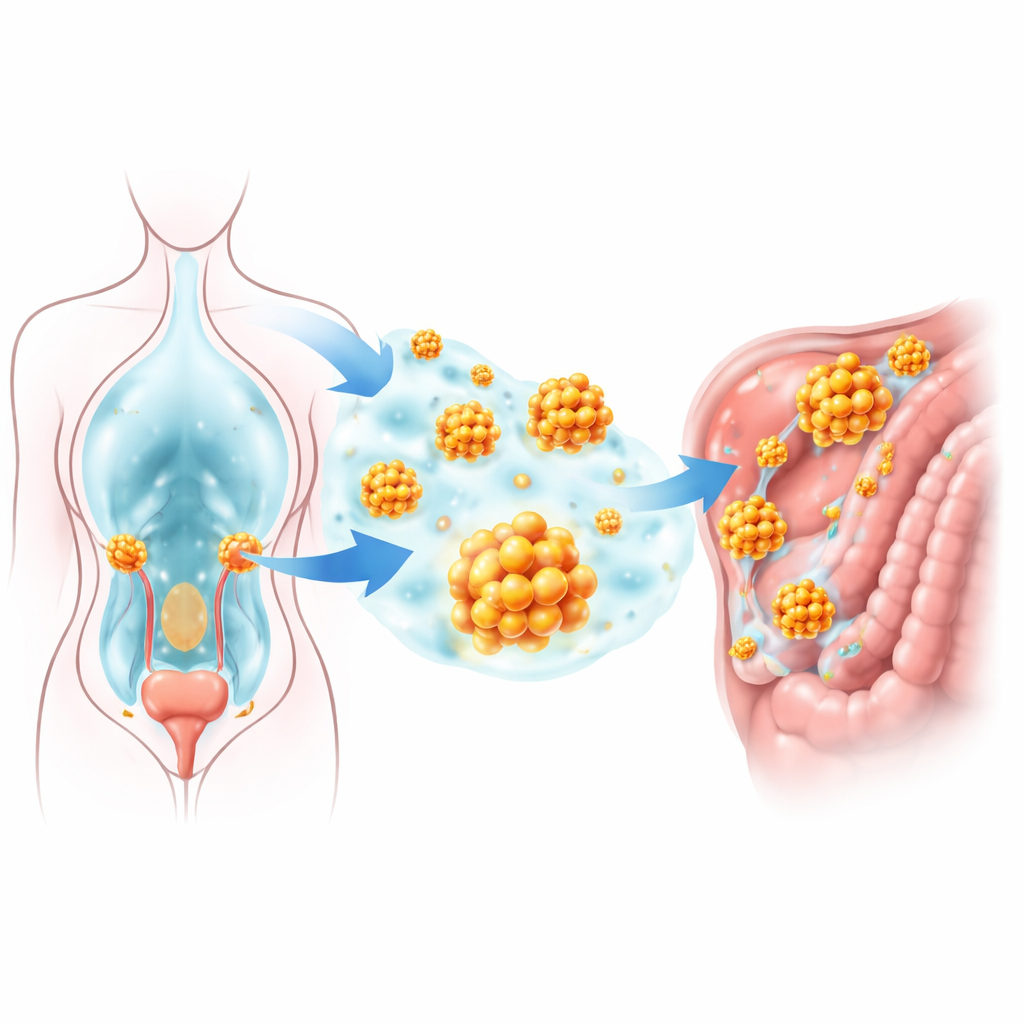
Een verborgen medeplichtige bij tumorspreiding
Om verder te komen dan statistische verbanden manipuleerde het team GLUD1-niveaus in in het laboratorium gekweekte eierstokkankercellijnen. Wanneer ze GLUD1 verlaagden, krimpten de vrijzwevende celclusters, stierven kankercellen gemakkelijker in suspensie en verminderde hun migratievermogen in standaard migratietests. Wanneer ze GLUD1 verhoogden, gebeurde het omgekeerde: de cellen weerstonden celdood en bewogen zich agressiever. In muizen die intraperitoneaal werden geïnjecteerd met eierstokkankercellen leidde het uitschakelen van GLUD1 tot minder tumorknobbels op organen zoals de milt en de lever, vertraagde tumorgroei en langere overleving. Tumormonsters van deze muizen toonden meer stervende cellen en minder delende cellen, wat de gedachte versterkt dat GLUD1 cruciaal is om losgeraakte kankercellen lang genoeg in leven te houden om nieuwe kolonies te vormen.
Een beschermende samenwerking binnen kankercellen
Vervolgens vroegen de onderzoekers hoe GLUD1 dit levensbehoudende effect uitoefent. Met eiwitzoekmethoden ontdekten ze dat GLUD1 fysiek bindt aan een ander eiwit genaamd ARAF, dat deel uitmaakt van een bekend signaalpad dat celoverleving en groei bevordert. Binnen kankercellen bevinden GLUD1 en ARAF zich vooral samen in het cytosol en niet in de energieproducerende structuren, wat wijst op een signalerende rol. Wanneer GLUD1 werd verminderd, daalden ARAF-niveaus, terwijl de nauwe verwanten BRAF en CRAF onaangetast bleven. Dit verlies van ARAF ging gepaard met verminderde activiteit in het downstream MEK/ERK-pad en een verschuiving naar pro-death-eiwitten. Het herintroduceren van ARAF in GLUD1-deficiënte cellen herstelde veel van de overlevingssignalisatie en verminderde celdood, wat aantoont dat ARAF een belangrijke schakel is die GLUD1 verbindt met resistentie tegen anoikis. 
Hoe GLUD1 een sleutel‑signaal beschermt
Dieper gravend vonden de onderzoekers dat GLUD1 fungeert als een lijfwacht die voorkomt dat ARAF gelabeld en afgebroken wordt door het proteïne-recyclingmechanisme van de cel. Wanneer dit recyclingmechanisme chemisch werd geblokkeerd, keerde de daling van ARAF na verlies van GLUD1 om. Tijdstudiën toonden aan dat ARAF veel sneller degradeerde wanneer GLUD1 ontbrak, en biochemische tests lieten zien dat ARAF zwaarder werd “getagd” voor afbraak. Overexpressie van GLUD1 verminderde deze tags. Samen wijzen de resultaten erop dat GLUD1 ARAF stabiliseert door het afbraakproces te blokkeren, waardoor het overlevingssignaal in losgeraakte eierstokkankercellen actief blijft. Interessant genoeg is GLUD1 vooral bekend om zijn rol bij de verwerking van het voedingsstof glutamine; het teruggeven van een van zijn metabole producten herstelde ARAF en de signalisatie slechts gedeeltelijk, wat suggereert dat de eiwitbeschermende rol van GLUD1 in deze context minstens zo belangrijk is als zijn enzymatische activiteit.
Wat dit kan betekenen voor toekomstige behandelingen
Door te onthullen hoe GLUD1 ARAF beschermt en overlevingspaden actief houdt, legt deze studie een kwetsbaar punt bloot in de levenscyclus van zwerfende eierstokkankercellen. Als geneesmiddelen ontwikkeld zouden kunnen worden die het stabiliserende effect van GLUD1 op ARAF verminderen — of die de downstream MEK/ERK-signalen blokkeren — zouden ze losgeraakte kankercellen kunnen dwingen tot anoikis in plaats van nieuwe tumoren te vormen in de buikholte. Omdat GLUD1 ook een centrale rol speelt in het normale celmetabolisme, zou een dergelijke behandeling zorgvuldig de balans moeten bewaren tussen voordelen en bijwerkingen. Toch biedt de ontdekking van deze GLUD1–ARAF-samenwerking een helderder beeld van hoe eierstokkanker zich verspreidt en markeert het veelbelovende moleculaire doelen voor therapieën die gericht zijn op het voorkomen dat de ziekte zich door het lichaam wortelt.
Bronvermelding: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Trefwoorden: eierstokkanker, metastase, weerstand tegen anoikis, GLUD1, celoverlevingssignalen