Clear Sky Science · ru
GLUD1 поддерживает прогрессирование рака яичников, противодействуя аноикису через сигнализацию ARAF/MEK/ERK
Почему это исследование важно
Рак яичников часто обнаруживают лишь после того, как он тихо распространился по брюшной полости, что делает его одним из наиболее смертельных онкологических заболеваний у женщин. Это распространение зависит от опухолевых клеток, которые отрываются от яичника, плавают в брюшной жидкости и умудряются выживать, потеряв прикрепление к окружающей ткани. Исследование, лежащее в основе этой статьи, выявляет ключевую молекулу-помощницу, позволяющую таким плавающим клеткам противостоять смерти и порождать новые опухоли, что открывает новые идеи для возможных способов предотвращения распространения рака.
Как блуждающие опухолевые клетки обманывают смерть
Большинству здоровых клеток необходимо оставаться прикреплёнными к опорной среде; при потере этого контакта они запускают программу самоуничтожения, называемую «аноикис». Клетки рака яичников в брюшной полости, однако, образуют кластеры — небольшие сферические агрегаты, которые выживают без прикрепления и позднее могут прикрепляться к новым поверхностям. Исследователи проанализировали крупные базы данных экспрессии генов, сосредоточив внимание на генах, связанных одновременно с устойчивостью к гибели клеток и с использованием аминокислот. Один ген, названный GLUD1, выделялся особенно: он был более активен в опухолях яичников по сравнению с нормальной тканью, особенно в образцах из метастатических очагов. Более высокий уровень GLUD1 у пациентов был тесно связан с более короткой общей выживаемостью и более быстрым возвращением болезни, что говорит о том, что эта молекула способствует прогрессированию опухоли. 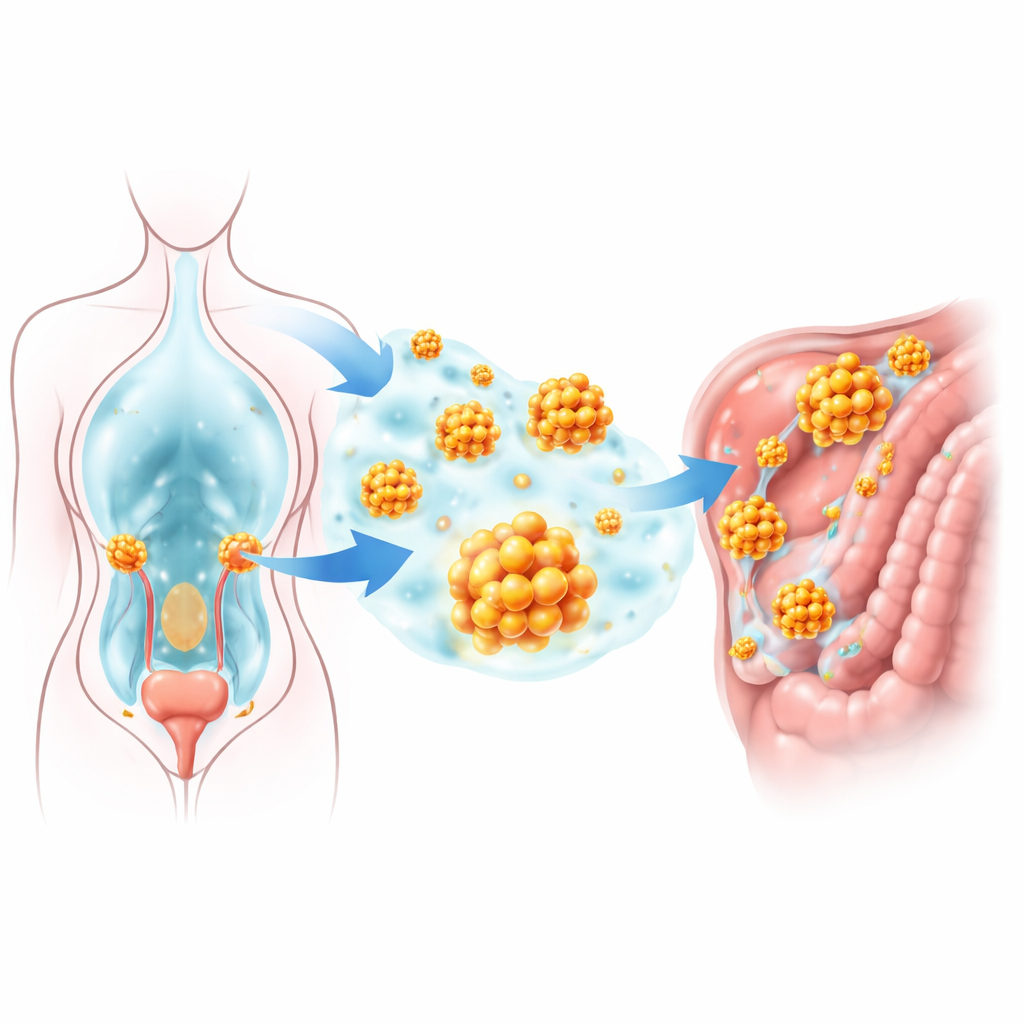
Скрытый сообщник в распространении опухоли
Чтобы выйти за пределы статистических ассоциаций, команда модифицировала уровень GLUD1 в клеточных линиях рака яичников, выращенных в лаборатории. При снижении GLUD1 свободноплавающие кластеры уменьшались в размере, клетки в суспензии умирали чаще, и способность клеток к миграции в стандартных тестах снижалась. При повышении экспрессии GLUD1 наблюдалось обратное: клетки сопротивлялись гибели и становились более подвижными. В моделях с мышами, которым вводили клетки рака яичников в брюшную полость, подавление GLUD1 приводило к меньшему числу опухолевых узелков на органах, таких как селезенка и печень, к замедленному росту опухолей и к увеличению выживаемости животных. Образцы опухолей от таких мышей показывали больше умирающих клеток и меньше делящихся, что подкрепляет идею о критической роли GLUD1 в поддержании жизни оторванных клеток достаточно долго для образования новых очагов.
Защитное партнерство внутри опухолевой клетки
Исследователи затем задались вопросом, как именно GLUD1 обеспечивает это сохраняющее жизнь действие. С помощью методов поиска белков они обнаружили, что GLUD1 физически связывается с другим белком — ARAF, частью хорошо известного каскада сигналов, который стимулирует выживание и рост клеток. В опухолевых клетках GLUD1 и ARAF располагаются вместе преимущественно в цитозоле, а не в энергообразующих органеллах, что указывает на сигнальную роль. При снижении GLUD1 уровень ARAF падал, тогда как его близкие родственники BRAF и CRAF оставались неизменными. Эта потеря ARAF сопровождалась ослаблением активности нижележащего пути MEK/ERK и сдвигом в сторону протеинов, способствующих гибели. Повторное введение ARAF в клетки с дефицитом GLUD1 восстановило значительную часть сигнала выживания и уменьшило гибель клеток, показав, что ARAF является ключевым посредником, связывающим GLUD1 с устойчивостью к аноикису. 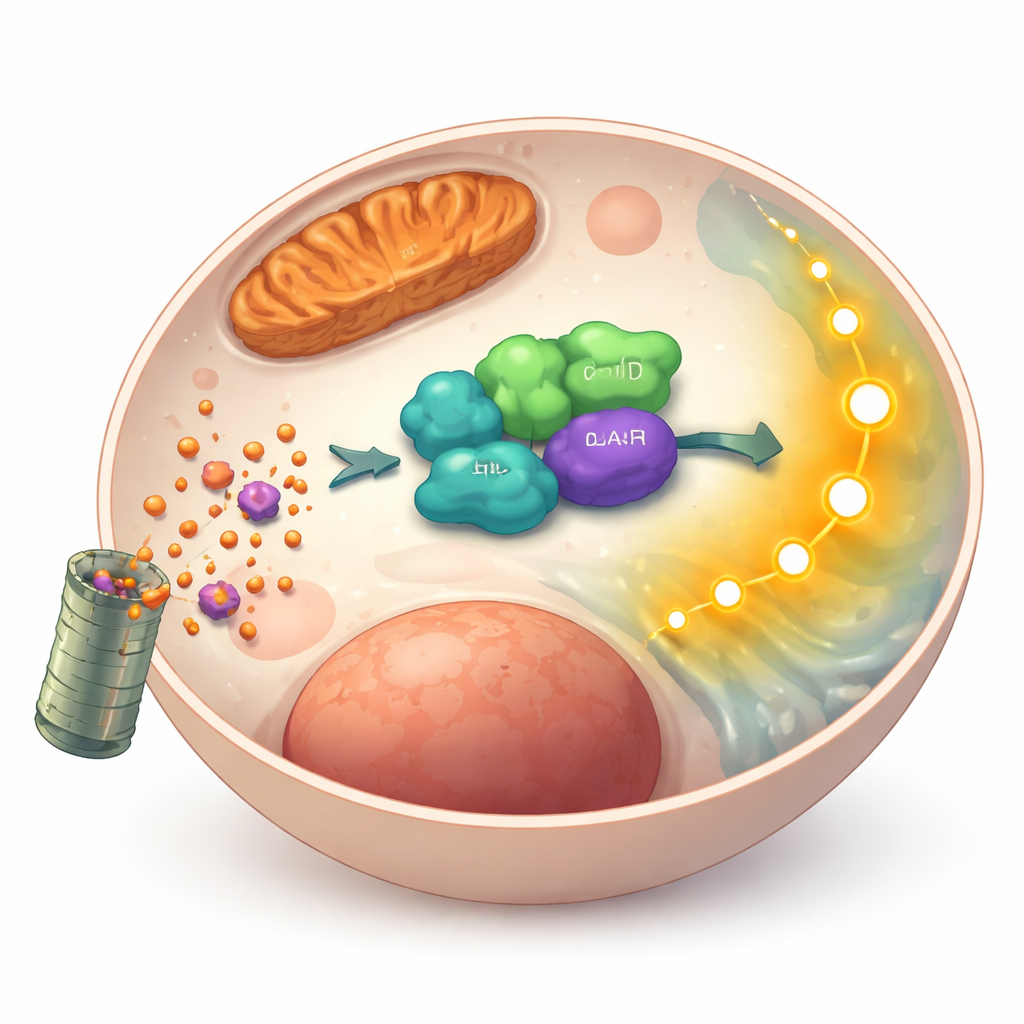
Как GLUD1 защищает ключевой сигнал
Углубляя изучение, команда обнаружила, что GLUD1 действует как «телохранитель», предотвращающий метку и уничтожение ARAF системой утилизации белков клетки. Когда эту систему утилизации химически блокировали, падение ARAF после утраты GLUD1 было обращено. Эксперименты с отслеживанием по времени показали, что ARAF распадался значительно быстрее при отсутствии GLUD1, а биохимические тесты выявили усиленное «маркирование» ARAF для утилизации. Переэкспрессия GLUD1 уменьшала эти метки. В совокупности результаты указывают на то, что GLUD1 стабилизирует ARAF, предотвращая его распад, тем самым сохраняя включённым сигнал выживания в оторванных клетках рака яичников. Любопытно, что хотя GLUD1 известен прежде всего как участник метаболизма глутамина, добавление одного из его метаболитов лишь частично восстанавливало ARAF и его сигнализацию, что предполагает: роль GLUD1 в защите белка как минимум столь же важна, как и его ферментативная активность в данном контексте.
Что это может значить для будущего лечения
Раскрывая, как GLUD1 защищает ARAF и поддерживает активность путей выживания, это исследование выявляет уязвимую точку в жизненном цикле блуждающих клеток рака яичников. Если удастся разработать препараты, ослабляющие стабилизирующее влияние GLUD1 на ARAF — или блокирующие нижележащие сигналы MEK/ERK — это может заставить оторванные клетки пройти аноикис вместо формирования новых опухолей в брюшной полости. Поскольку GLUD1 также играет центральную роль в нормальном клеточном метаболизме, любое такое лечение потребует тщательного взвешивания пользы и побочных эффектов. Тем не менее открытие партнёрства GLUD1–ARAF даёт более ясную карту механизмов распространения рака яичников и выделяет перспективный набор молекулярных мишеней для терапии, направленной на предотвращение укоренения болезни по всему телу.
Цитирование: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Ключевые слова: рак яичников, метастазирование, устойчивость к аноикису, GLUD1, сигналы выживания клеток