Clear Sky Science · pl
GLUD1 wspiera postęp raka jajnika, przeciwdziałając anoikis za pośrednictwem szlaku ARAF/MEK/ERK
Dlaczego to badanie jest ważne
Rak jajnika często bywa wykrywany dopiero wtedy, gdy cicho rozprzestrzenił się po jamie brzusznej, co czyni go jednym z najgroźniejszych nowotworów u kobiet. To rozsiewanie zależy od komórek nowotworowych, które odrywają się od jajnika, unoszą w płynie brzusznym i mimo braku kotwiczenia do otaczających tkanek potrafią przetrwać. Badanie opisane w tym artykule ujawnia kluczowy pomocniczy czynnik, który pozwala tym przemieszczającym się komórkom opierać się śmierci komórkowej i zasiedlać nowe guzy, co wskazuje nowe kierunki, które lekarze mogliby kiedyś wykorzystać, by zatrzymać rozprzestrzenianie się nowotworu.
Jak włóczące się komórki nowotworowe oszukują śmierć
Większość zdrowych komórek musi pozostawać przytwierdzona do miejscowego rusztowania; gdy tracą to podparcie, uruchamiają program samozniszczenia zwany „anoikis”. Komórki raka jajnika w jamie brzusznej grupują się jednak w drobne kuliste agregaty, które przetrwają bez przyczepu i później mogą przylegać do nowych powierzchni. Naukowcy przejrzeli rozległe bazy danych ekspresji genów, koncentrując się na genach powiązanych zarówno z opornością na śmierć komórkową, jak i z wykorzystaniem aminokwasów. Jeden gen, nazwany GLUD1, wyróżniał się wyraźnie: był bardziej aktywny w guzach jajnika niż w tkance prawidłowej, szczególnie w próbkach pobranych z miejsc przerzutowych. Wyższy poziom GLUD1 u pacjentek był silnie skorelowany z krótszym całkowitym przeżyciem i szybszym nawrotem choroby, co sugeruje, że ta cząsteczka wspiera progresję nowotworu. 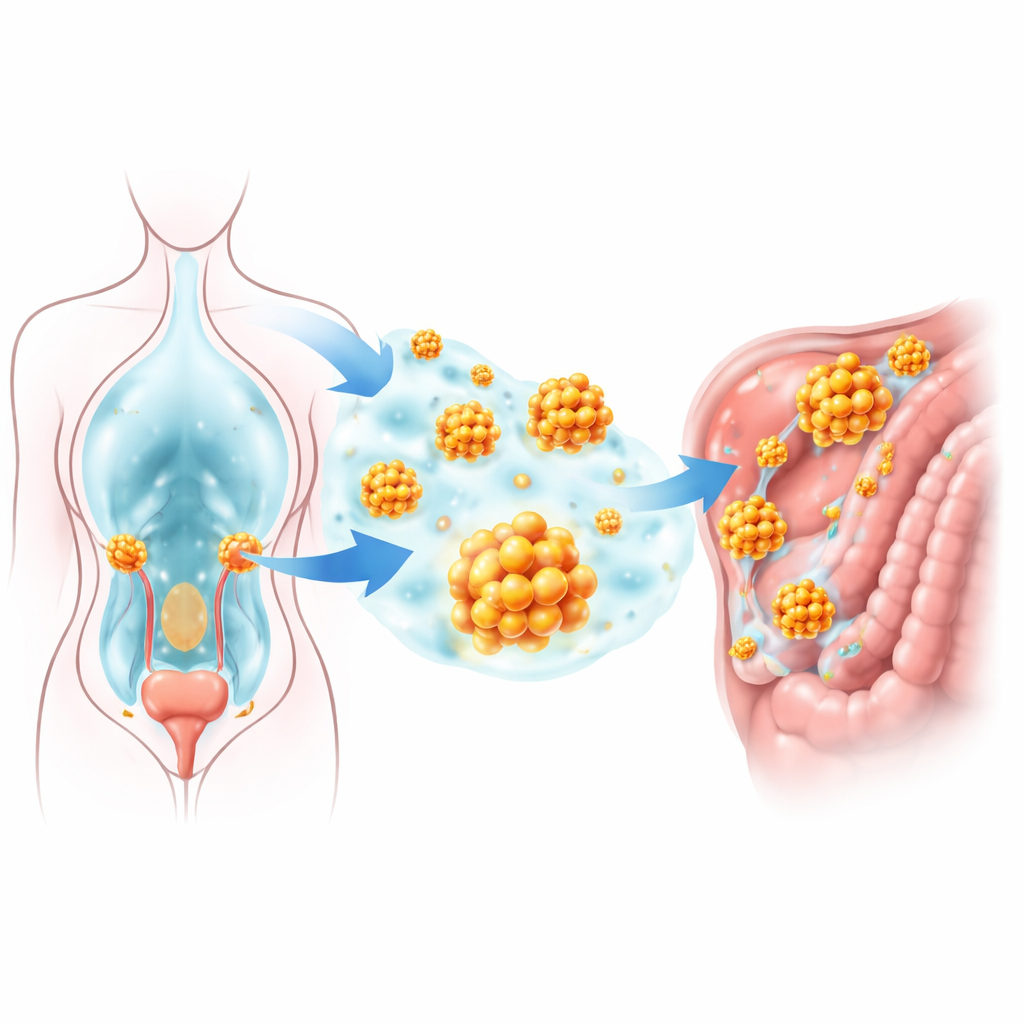
Ukryty wspólnik w rozprzestrzenianiu się guza
Aby wyjść poza związki statystyczne, zespół modyfikował poziomy GLUD1 w liniach komórkowych raka jajnika hodowanych w laboratorium. Gdy obniżono GLUD1, wolno unoszące się skupiska komórek zmniejszały się, komórki nowotworowe łatwiej umierały w zawiesinie, a ich zdolność do migracji w standardowych testach przesiewowych spadła. Po zwiększeniu ekspresji GLUD1 sytuacja była odwrotna: komórki opierały się śmierci i poruszały się bardziej agresywnie. U myszy, którym wstrzyknięto komórki raka jajnika do jamy brzusznej, wyciszenie GLUD1 prowadziło do mniejszej liczby guzków nowotworowych na narządach takich jak śledziona i wątroba, wolniejszego wzrostu guzów i wydłużonego przeżycia. Próbki guzów od tych myszy wykazywały więcej komórek umierających i mniej dzielących się, potwierdzając tezę, że GLUD1 jest kluczowy dla utrzymania przy życiu oderwanych komórek nowotworowych wystarczająco długo, by mogły utworzyć nowe kolonie.
Ochronny układ wewnątrz komórek nowotworowych
Następnie badacze zapytali, w jaki sposób GLUD1 wywiera ten zachowawczy wpływ. Przy użyciu metod poszukiwania białek odkryli, że GLUD1 fizycznie wiąże się z innym białkiem, nazwanym ARAF, będącym częścią dobrze poznanego łańcucha sygnałowego, który napędza przeżycie i wzrost komórek. W komórkach nowotworowych GLUD1 i ARAF współwystępują głównie w cytosolu, a nie w strukturach produkujących energię, co sugeruje rolę w przekazywaniu sygnału. Gdy obniżono GLUD1, poziomy ARAF spadły, natomiast jego bliscy krewni BRAF i CRAF pozostali bez zmian. Utrata ARAF towarzyszyła osłabieniu aktywności szlaku MEK/ERK i przesunięciu w kierunku białek promujących śmierć. Ponowne wprowadzenie ARAF do komórek pozbawionych GLUD1 przywróciło dużą część sygnalizacji przeżyciowej i zmniejszyło śmiertelność komórek, pokazując, że ARAF jest istotnym pośrednikiem łączącym GLUD1 z opornością na anoikis. 
Jak GLUD1 chroni kluczowy sygnał
Dalej zespół ustalił, że GLUD1 działa niczym ochroniarz, zapobiegając znakowaniu ARAF do zniszczenia przez system recyklingu białek w komórce. Gdy ten system recyklingu został chemicznie zablokowany, spadek ARAF obserwowany po utracie GLUD1 został odwrócony. Eksperymenty w czasie wykazały, że ARAF rozpadał się znacznie szybciej, gdy brakowało GLUD1, a testy biochemiczne ujawniły silniejsze „tagowanie” ARAF do utylizacji. Nadekspresja GLUD1 zmniejszała te znaczniki. Razem wyniki wskazują, że GLUD1 stabilizuje ARAF, blokując jego rozkład, tym samym utrzymując aktywny sygnał przeżyciowy w oderwanych komórkach raka jajnika. Co ciekawe, chociaż GLUD1 jest najlepiej znany z udziału w przetwarzaniu aminokwasu glutaminy, uzupełnienie jednego z jego produktów metabolicznych tylko częściowo przywróciło ARAF i jego sygnalizację, co sugeruje, że rola GLUD1 w ochronie białek jest przynajmniej równie ważna jak jego aktywność enzymatyczna w tym kontekście.
Co to może znaczyć dla przyszłego leczenia
Ujawniając, w jaki sposób GLUD1 chroni ARAF i utrzymuje aktywne szlaki przeżycia, to badanie odsłania wrażliwy punkt w cyklu życia przemieszczających się komórek raka jajnika. Jeśli udałoby się opracować leki osłabiające stabilizujący wpływ GLUD1 na ARAF — lub blokujące sygnały MEK/ERK pochodzące dalej w kaskadzie — mogłyby one zmusić oderwane komórki nowotworowe do przejścia w anoikis zamiast tworzenia nowych guzów w jamie brzusznej. Ponieważ GLUD1 odgrywa również istotne role w normalnym metabolizmie komórek, takie leczenie musiałoby starannie wyważyć korzyści i skutki uboczne. Mimo to odkrycie partnerstwa GLUD1–ARAF dostarcza jaśniejszej mapy mechanizmów rozsiewu raka jajnika i wskazuje obiecujący zestaw molekularnych celów terapii ukierunkowanych na zatrzymanie choroby, zanim zdąży się rozsiać po całym organizmie.
Cytowanie: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Słowa kluczowe: rak jajnika, przerzuty, oporność na anoikis, GLUD1, szlaki przeżycia komórki