Clear Sky Science · es
GLUD1 favorece la progresión del cáncer de ovario contrarrestando la anoikis mediante la señalización ARAF/MEK/ERK
Por qué importa esta investigación
El cáncer de ovario suele detectarse solo después de haberse diseminado silenciosamente por toda la cavidad abdominal, lo que lo convierte en uno de los tumores más letales entre las mujeres. Esa diseminación depende de células tumorales que se desprenden del ovario, flotan en el líquido abdominal y logran sobrevivir pese a ya no estar ancladas al tejido circundante. El estudio detrás de este artículo revela una molécula ayudante clave que permite a estas células errantes resistir la muerte celular y sembrar nuevos tumores, lo que abre nuevas ideas sobre cómo los médicos podrían, algún día, impedir la propagación del cáncer.
Cómo las células cancerosas errantes burlan a la muerte
La mayoría de las células sanas deben permanecer adheridas a su estructura de soporte; al perder ese agarre, activan un programa de autodestrucción conocido como “anoikis”. Sin embargo, las células de cáncer de ovario en la cavidad abdominal se agrupan en pequeñas esferas que sobreviven sin adhesión y que más tarde pueden adherirse a nuevas superficies. Los investigadores examinaron grandes bases de datos de expresión génica, centrándose en genes vinculados tanto a la resistencia a la muerte celular como al uso de aminoácidos. Un gen llamado GLUD1 destacó claramente: estaba más activo en tumores ováricos que en tejido normal, sobre todo en muestras tomadas de sitios metastásicos. Niveles más altos de GLUD1 en pacientes se correlacionaron de forma notable con una supervivencia global menor y con recurrencia más rápida de la enfermedad, lo que sugiere que esta molécula ayuda a la progresión tumoral. 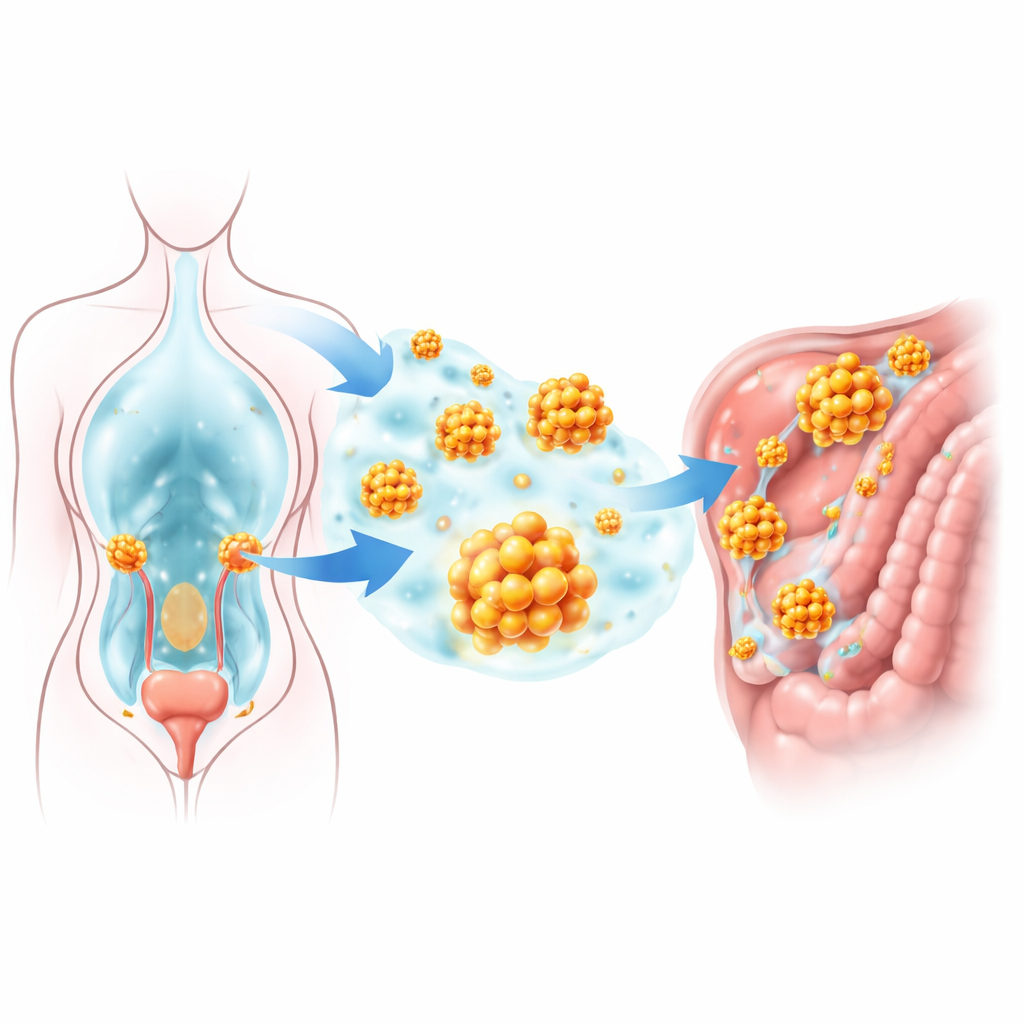
Un cómplice oculto en la diseminación tumoral
Para ir más allá de las asociaciones estadísticas, el equipo moduló los niveles de GLUD1 en líneas celulares de cáncer de ovario cultivadas en el laboratorio. Al reducir GLUD1, los cúmulos celulares suspendidos se hicieron más pequeños, las células tumorales morían con más facilidad en suspensión y disminuía su capacidad de migrar en ensayos estándar. Al aumentar GLUD1, ocurrió lo contrario: las células resistían la muerte y migraban con mayor agresividad. En ratones inyectados con células de cáncer de ovario en la cavidad abdominal, silenciar GLUD1 produjo menos nódulos tumorales en órganos como el bazo y el hígado, un crecimiento tumoral más lento y una supervivencia prolongada. Las muestras tumorales de estos animales mostraron más células moribundas y menos en división, lo que refuerza la idea de que GLUD1 es crucial para mantener con vida a las células desprendidas el tiempo suficiente para formar nuevas colonias.
Una asociación protectora dentro de las células tumorales
Los investigadores preguntaron entonces cómo ejerce GLUD1 esta influencia protectora. Mediante métodos de búsqueda de proteínas, descubrieron que GLUD1 se une físicamente a otra proteína llamada ARAF, parte de una conocida cascada de señales que impulsa la supervivencia y el crecimiento celular. Dentro de las células tumorales, GLUD1 y ARAF se localizan juntos principalmente en el citosol más que en las estructuras productoras de energía, lo que sugiere un papel en la señalización. Cuando GLUD1 se redujo, los niveles de ARAF descendieron, mientras que sus parientes cercanos BRAF y CRAF no cambiaron. Esta pérdida de ARAF se acompañó de una actividad debilitada de la vía MEK/ERK aguas abajo y de un desplazamiento hacia proteínas proapoptóticas. Reintroducir ARAF en células deficientes en GLUD1 restauró gran parte de la señal de supervivencia y redujo la muerte celular, demostrando que ARAF es un intermediario clave que conecta a GLUD1 con la resistencia a la anoikis. 
Cómo GLUD1 protege una señal clave
Indagando más, el equipo encontró que GLUD1 actúa como un guardaespaldas que impide que ARAF sea etiquetado y degradado por el sistema de reciclaje proteico de la célula. Cuando este sistema de reciclaje se bloqueó químicamente, la caída de ARAF observada tras la pérdida de GLUD1 se revirtió. Experimentos temporales mostraron que ARAF se degradaba mucho más rápido cuando faltaba GLUD1, y pruebas bioquímicas revelaron un mayor “marcado” de ARAF para su eliminación. La sobreexpresión de GLUD1 redujo esas marcas. En conjunto, los resultados indican que GLUD1 estabiliza ARAF al bloquear su degradación, manteniendo así la señal de supervivencia activa en células de cáncer de ovario desprendidas. Curiosamente, aunque GLUD1 es mejor conocido por ayudar en el procesamiento del nutriente glutamina, la reposición de uno de sus productos metabólicos solo pudo restaurar de manera parcial a ARAF y su señalización, lo que sugiere que el papel protector de GLUD1 sobre proteínas es al menos tan importante como su actividad enzimática en este contexto.
Qué podría significar esto para tratamientos futuros
Al revelar cómo GLUD1 protege a ARAF y mantiene activas las vías de supervivencia, este estudio expone un punto vulnerable en el ciclo vital de las células de cáncer de ovario errantes. Si se pudieran desarrollar fármacos que atenúen el efecto estabilizador de GLUD1 sobre ARAF —o que bloqueen las señales MEK/ERK aguas abajo—, podrían forzar a las células desprendidas a someterse a la anoikis en lugar de formar nuevos tumores en el abdomen. Dado que GLUD1 también desempeña funciones centrales en el metabolismo normal celular, cualquier tratamiento de este tipo tendría que equilibrar cuidadosamente beneficios y efectos secundarios. Aun así, el descubrimiento de esta asociación GLUD1–ARAF ofrece un mapa más claro de cómo se disemina el cáncer de ovario y destaca un conjunto prometedor de dianas moleculares para terapias destinadas a impedir que la enfermedad se arraigue en todo el cuerpo.
Cita: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Palabras clave: cáncer de ovario, metástasis, resistencia a la anoikis, GLUD1, señalización de supervivencia celular