Clear Sky Science · ja
GLUD1 は ARAF/MEK/ERK シグナルを介して脱着アポトーシスを克服し卵巣がんの進行を促進する
この研究が重要な理由
卵巣がんは腹腔内に静かに広がった後で発見されることが多く、女性に影響を与える最も致命的ながんの一つです。この広がりは、卵巣から離れて腹の液体中を漂いながらも、周囲の組織に接着していないにもかかわらず生き延びることができるがん細胞に依存します。本稿の研究は、こうした浮遊細胞が細胞死に抵抗して新しい腫瘍を播種するのを可能にする重要な補助分子を明らかにしており、がんの播種を止めるための新たな治療の発想を示しています。
漂流するがん細胞はどのように死を逃れるか
ほとんどの正常細胞は局所の支持構造に付着している必要があり、その付着を失うと「脱着アポトーシス(anoikis)」と呼ばれる自己破壊プログラムが作動します。しかし腹腔内の卵巣がん細胞は小さな球状塊を形成して付着せずに生存し、後に新しい表面に付着できます。研究者たちは、大規模な遺伝子発現データベースを精査し、細胞死耐性とアミノ酸利用に関連する遺伝子に着目しました。その中で GLUD1 という遺伝子が際立っていました。GLUD1 は正常組織より卵巣腫瘍でより活性化されており、特に転移部位のサンプルで顕著でした。患者での GLUD1 レベルの高さは全生存期間の短さや再発の早さと強く関連しており、この分子が腫瘍の進展を助けていることを示唆しています。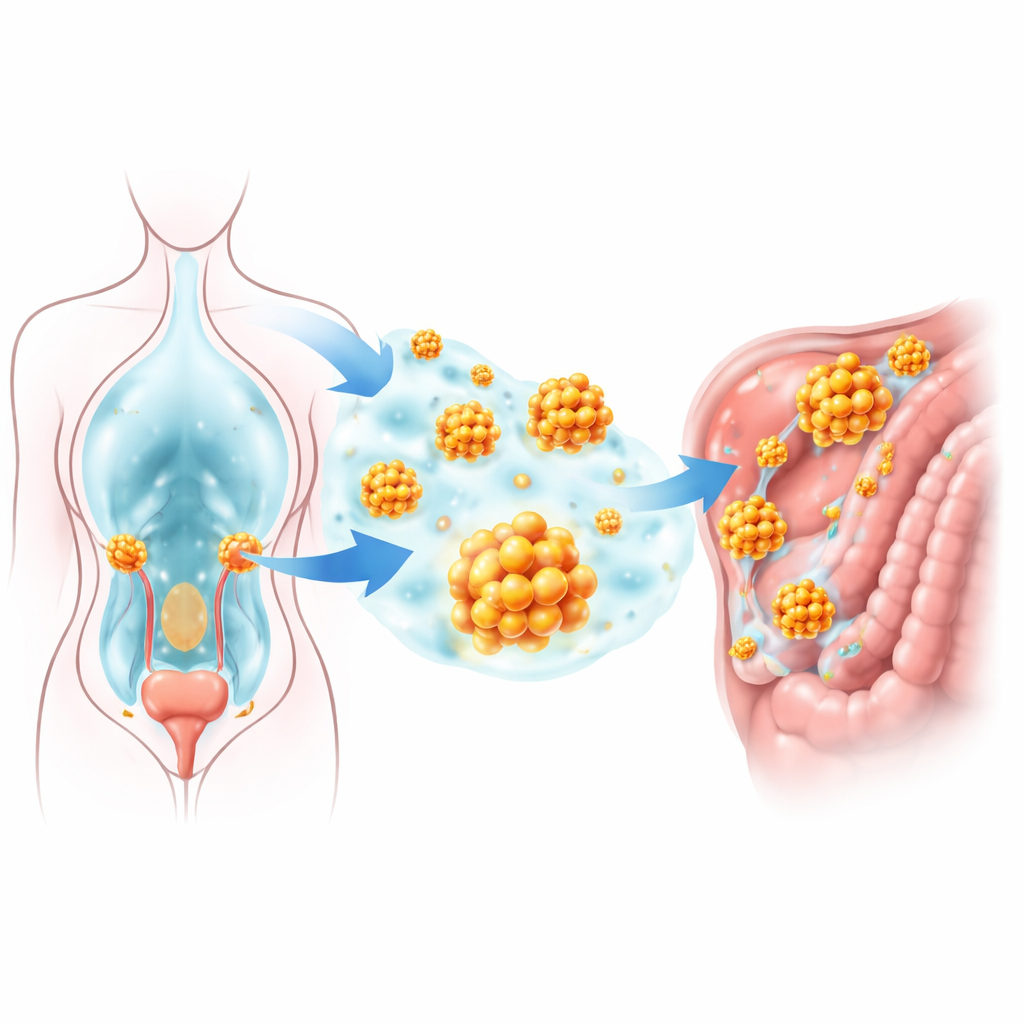
腫瘍播種の隠れた共犯者
統計的関連を超えて因果を探るため、研究チームは培養した卵巣がん細胞株の GLUD1 レベルを操作しました。GLUD1 を低下させると、浮遊する細胞塊は縮小し、懸濁状態での細胞死が増え、標準的な移動試験での遊走能力が低下しました。逆に GLUD1 を増やすと、細胞は死にくくなり、より積極的に移動しました。腹腔内に卵巣がん細胞を注入したマウスでは、GLUD1 をサイレンシングすると脾臓や肝臓などの臓器上の腫瘍結節が減少し、腫瘍成長が遅くなり、寿命が延びました。これらのマウスの腫瘍サンプルは、死滅細胞が増え分裂する細胞が減っており、GLUD1 が接着を失ったがん細胞を新しいコロニーに成長させるのに十分な間、生存させる上で重要であることを裏付けています。
がん細胞内の保護的パートナーシップ
次に研究者たちは GLUD1 がどのようにしてこの生存効果を発揮するのかを調べました。タンパク質探索法により、GLUD1 が ARAF と呼ばれる別のタンパク質に物理的に結合することを発見しました。ARAF は細胞の生存と増殖を駆動するよく知られたシグナル伝達経路の一部です。がん細胞内では GLUD1 と ARAF は主に細胞質に共存しており、エネルギー産生器官ではない部位にいることが示唆され、シグナル伝達での役割が示されました。GLUD1 を減少させると ARAF の量が低下し、BRAF や CRAF といった近縁分子には変化がありませんでした。ARAF 減少は下流の MEK/ERK 経路の活性低下と、細胞死促進タンパク質への傾きと伴っていました。GLUD1 欠損細胞に ARAF を再導入すると生存シグナルの多くが回復し、細胞死が減少したため、ARAF は GLUD1 と脱着アポトーシス耐性を結びつける主要な仲介者であることが示されました。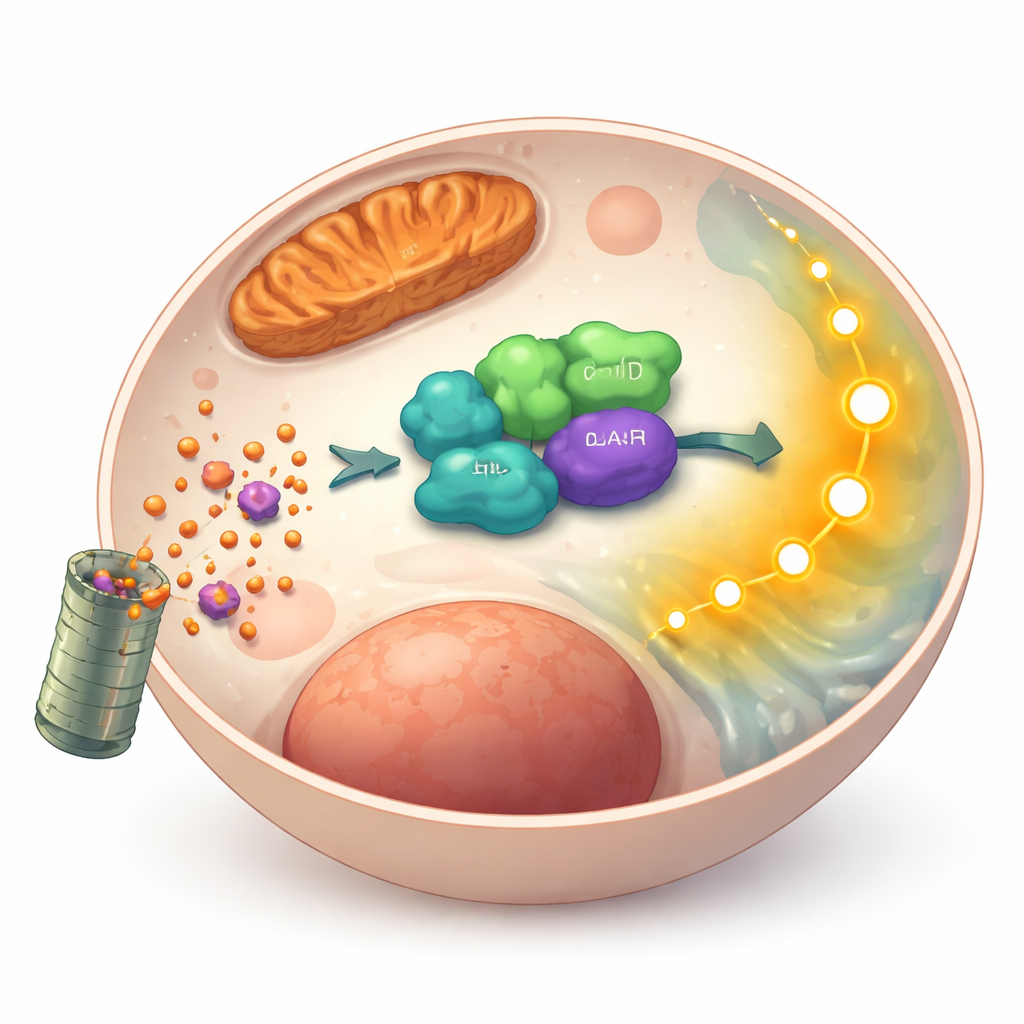
GLUD1 は重要なシグナルをどう守るか
さらに掘り下げると、GLUD1 は ARAF が細胞のタンパク質分解システムによってタグ付けされ分解されるのを阻止する用心棒のように作用することがわかりました。この分解機構を化学的に阻害すると、GLUD1 喪失後に見られた ARAF の低下は逆転しました。時間経過実験では GLUD1 がないと ARAF の分解がはるかに速く進み、生化学的検査では ARAF に対する分解のための「タグ付け」が強まっていることが示されました。GLUD1 を過剰発現させるとこれらのタグは減少しました。これらの結果は、GLUD1 が ARAF の分解を阻止して安定化させることで、遊離した卵巣がん細胞内の生存シグナルを維持していることを示しています。興味深いことに、GLUD1 は主に栄養素グルタミンの代謝に関与する酵素として知られていますが、その代謝産物を補っても ARAF とそのシグナルの回復は一部にとどまり、GLUD1 のタンパク質保護機能が酵素活性と同等以上に重要である可能性が示唆されます。
将来の治療にとっての意味
GLUD1 が ARAF を守り生存経路を活性化し続ける仕組みを明らかにしたことで、浮遊する卵巣がん細胞のライフサイクルにおける脆弱な点が露呈しました。もし GLUD1 の ARAF 安定化作用を弱める薬剤、あるいは下流の MEK/ERK シグナルを遮断する薬剤が開発できれば、剥がれたがん細胞を新たな腹腔内腫瘍を形成する代わりに脱着アポトーシスへ導くことが期待されます。とはいえ GLUD1 は正常細胞の代謝にも中心的役割を果たすため、そうした治療は利益と副作用のバランスを慎重に考慮する必要があります。それでもこの GLUD1–ARAF の結びつきの発見は、卵巣がんがどのように広がるかの地図を明確にし、病変が体内に広がる前に食い止めることを目指す分子標的療法の有望な候補を浮かび上がらせます。
引用: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
キーワード: 卵巣がん, 転移, 脱着耐性, GLUD1, 細胞生存シグナル