Clear Sky Science · pt
GLUD1 sustenta a progressão do câncer de ovário ao contrariar a anoikis via sinalização ARAF/MEK/ERK
Por que esta pesquisa importa
O câncer de ovário frequentemente é detectado apenas depois de ter se espalhado silenciosamente pelo abdome, tornando-se um dos tipos de câncer mais letais entre as mulheres. Essa disseminação depende de células tumorais que se desprendem do ovário, flutuam no líquido abdominal e ainda assim conseguem permanecer vivas apesar de não estarem mais ancoradas ao tecido circundante. O estudo por trás deste artigo revela uma molécula auxiliar-chave que permite a essas células errantes resistir à morte celular e formar novos tumores, apontando ideias novas sobre como médicos, um dia, poderiam impedir a propagação do câncer.
Como células cancerosas errantes driblam a morte
A maioria das células saudáveis precisa permanecer ligada à sua estrutura de suporte local; quando perdem essa ligação, elas ativam um programa de autodestruição conhecido como “anoikis”. Células de câncer de ovário na cavidade abdominal, porém, se agrupam em pequenos esferoides que sobrevivem sem ancoragem e podem mais tarde aderir a novas superfícies. Os pesquisadores vasculharam grandes bancos de dados de expressão gênica, concentrando-se em genes ligados tanto à resistência à morte celular quanto ao uso de aminoácidos. Um gene, chamado GLUD1, destacou-se claramente: estava mais ativo em tumores ovarianos do que em tecido normal, especialmente em amostras de locais metastáticos. Níveis elevados de GLUD1 nos pacientes estavam fortemente associados a sobrevida global mais curta e retorno mais rápido da doença, sugerindo que essa molécula ajuda os tumores a progredirem. 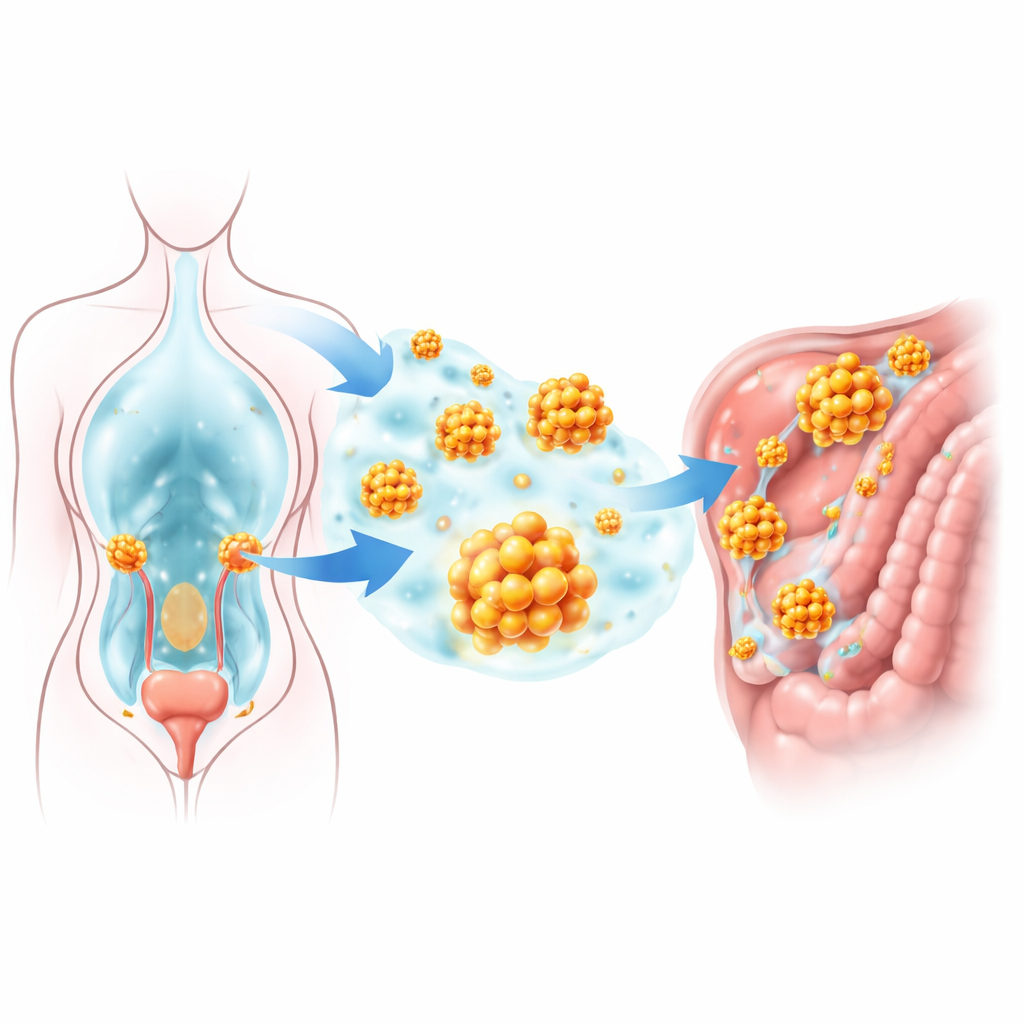
Um cúmplice oculto na disseminação tumoral
Para ir além das associações estatísticas, a equipe manipulou os níveis de GLUD1 em linhagens de células de câncer de ovário cultivadas em laboratório. Quando reduziram o GLUD1, os agregados celulares livres diminuíram, as células tumorais morreram com mais facilidade em suspensão e tornaram-se menos capazes de migrar em testes padrão. Quando aumentaram o GLUD1, ocorreu o oposto: as células resistiram à morte e movimentaram-se de forma mais agressiva. Em camundongos injetados com células de câncer de ovário na cavidade abdominal, o silenciamento de GLUD1 levou a menos nódulos tumorais em órgãos como baço e fígado, crescimento tumoral mais lento e maior sobrevida. Amostras tumorais desses animais mostraram mais células morrendo e menos células em divisão, reforçando a ideia de que GLUD1 é crítico para manter células cancerosas desprendidas vivas tempo suficiente para formar novas colônias.
Uma parceria protetora dentro das células cancerosas
Os investigadores então indagaram como GLUD1 exerce essa influência preservadora da vida. Usando métodos de busca proteica, descobriram que GLUD1 se liga fisicamente a outra proteína chamada ARAF, parte de uma conhecida cascata de sinais que promove sobrevivência e crescimento celular. Dentro das células tumorais, GLUD1 e ARAF ficam juntos principalmente no citosol, e não nas organelas produtoras de energia, sugerindo um papel de sinalização. Quando GLUD1 foi reduzido, os níveis de ARAF caíram, enquanto seus parentes próximos BRAF e CRAF permaneceram inalterados. Essa perda de ARAF foi acompanhada por menor atividade na via MEK/ERK a jusante e por um deslocamento em direção a proteínas pró-morte. Reintroduzir ARAF em células deficientes em GLUD1 restaurou grande parte da sinalização de sobrevivência e reduziu a morte celular, demonstrando que ARAF é um mensageiro central ligando GLUD1 à resistência contra a anoikis. 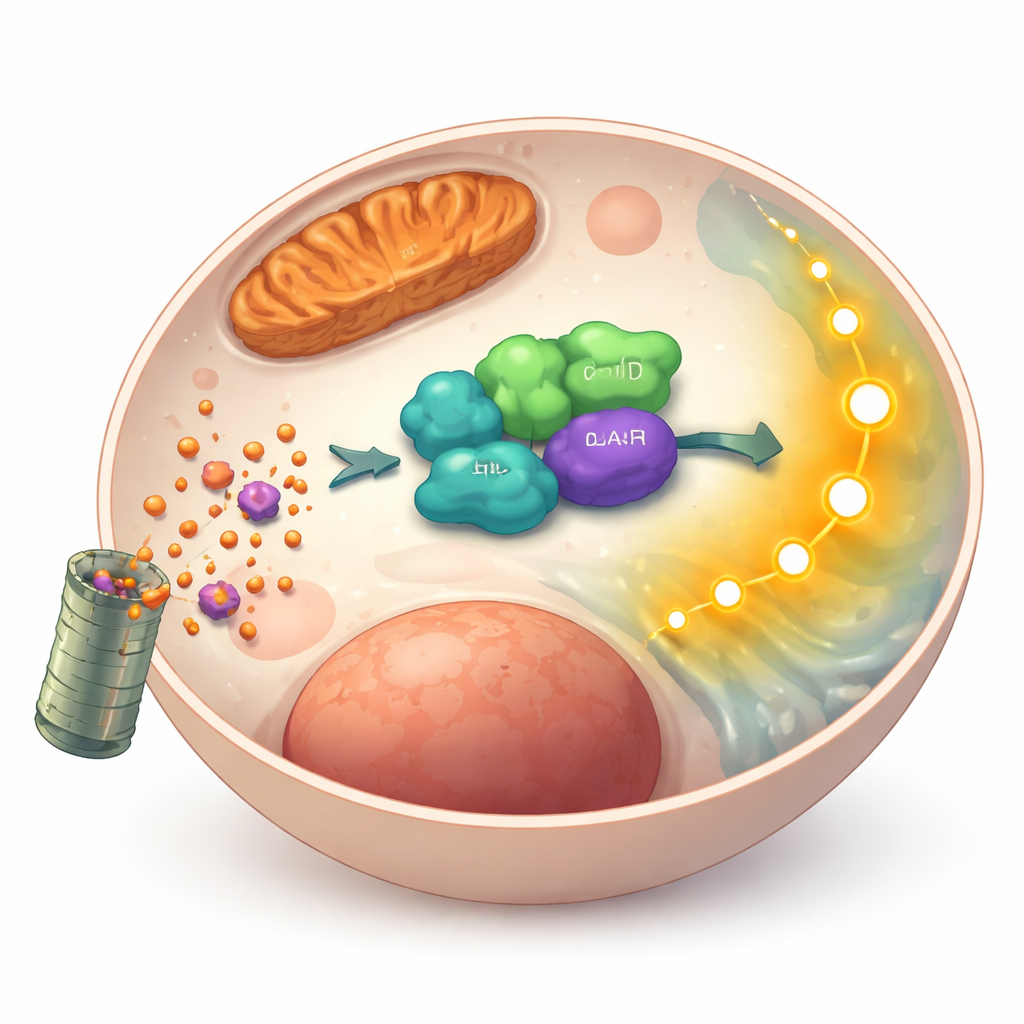
Como GLUD1 protege um sinal crucial
Investigando mais a fundo, a equipe descobriu que GLUD1 atua como um guarda-costas que impede que ARAF seja marcado e destruído pelo sistema de reciclagem de proteínas da célula. Quando essa maquinaria de reciclagem foi bloqueada quimicamente, a queda de ARAF observada após a perda de GLUD1 foi revertida. Experimentos de curso temporal mostraram que ARAF se degradava muito mais rápido na ausência de GLUD1, e testes bioquímicos revelaram marcações mais intensas de ARAF para descarte. A superexpressão de GLUD1 reduziu essas marcações. Juntos, os resultados indicam que GLUD1 estabiliza ARAF bloqueando sua degradação, mantendo assim o sinal de sobrevivência ligado em células de câncer de ovário destacadas. Curiosamente, embora GLUD1 seja mais conhecido por ajudar a processar o nutriente glutamina, a reintrodução de um de seus produtos metabólicos apenas parcialmente restaurou ARAF e sua sinalização, sugerindo que o papel protetor de GLUD1 sobre proteínas é ao menos tão importante quanto sua atividade enzimática nesse contexto.
O que isso pode significar para tratamentos futuros
Ao revelar como GLUD1 protege ARAF e mantém vias de sobrevivência ativas, este estudo expõe um ponto vulnerável no ciclo de vida das células tumorais errantes do ovário. Se fossem desenvolvidas drogas capazes de atenuar o efeito estabilizador de GLUD1 sobre ARAF — ou de bloquear os sinais a jusante MEK/ERK — elas poderiam forçar células tumorais destacadas a sofrer anoikis em vez de formar novos tumores no abdome. Como GLUD1 também desempenha papéis centrais no metabolismo celular normal, qualquer tratamento desse tipo precisaria equilibrar cuidadosamente benefícios e efeitos colaterais. Ainda assim, a descoberta dessa parceria GLUD1–ARAF oferece um mapa mais claro de como o câncer de ovário se espalha e destaca um conjunto promissor de alvos moleculares para terapias destinadas a impedir que a doença se estabeleça por todo o corpo.
Citação: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Palavras-chave: câncer de ovário, metástase, resistência à anoikis, GLUD1, sinalização de sobrevivência celular