Clear Sky Science · sv
GLUD1 stödjer äggstockscancerprogression genom att motverka anoikis via ARAF/MEK/ERK‑signalering
Varför denna forskning är viktig
Äggstockscancer upptäcks ofta först efter att den tyst har spridit sig i buken, vilket gör den till en av de dödligaste cancerformerna som drabbar kvinnor. Denna spridning beror på cancerceller som lossnar från äggstocken, flyter i bukvätska och ändå lyckas hålla sig vid liv trots att de inte längre är förankrade i omgivande vävnad. Studien bakom denna artikel avslöjar en nyckelmolekyl som gör det möjligt för dessa drivande celler att motstå celldöd och anlägga nya tumörer, vilket pekar på nya idéer för hur läkare en dag skulle kunna förhindra att cancern sprider sig.
Hur vandrande cancerceller överlistar döden
De flesta friska celler måste förbli fästa vid sin lokala stödstruktur; när de förlorar det greppet går de in i ett självdestruktivt program som kallas ”anoikis.” Äggstocksceller i bukhålan bildar däremot kluster i små klot som överlever utan fäste och senare kan fästa på nya ytor. Forskarna gick igenom stora genuttrycksdatabaser med fokus på gener kopplade både till motstånd mot celldöd och till användning av aminosyror. En gen, kallad GLUD1, framträdde tydligt: den var mer aktiv i äggstockstumörer än i normal vävnad, särskilt i prover tagna från metastatiska områden. Högre GLUD1‑nivåer hos patienter var starkt kopplade till kortare överlevnad totalt och snabbare återkomst av sjukdomen, vilket tyder på att denna molekyl bidrar till tumörprogression. 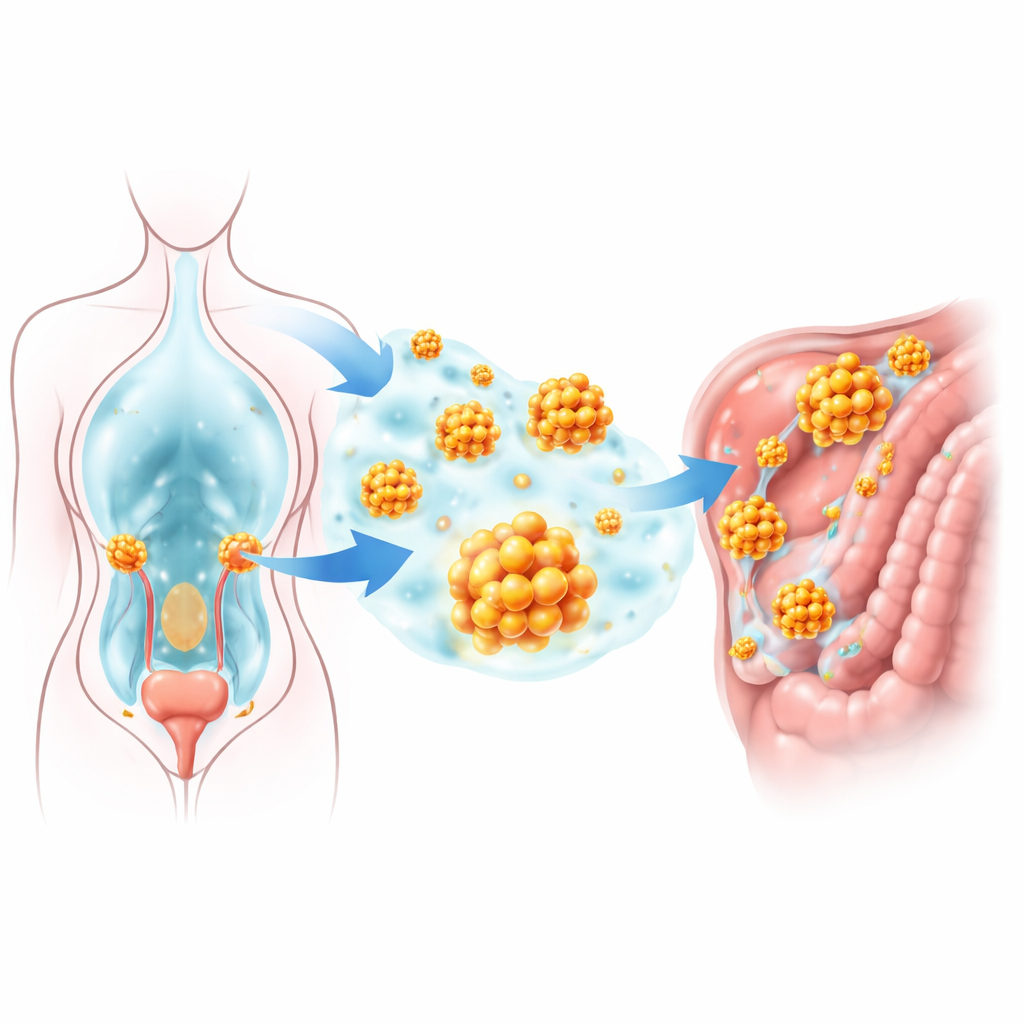
En dold medhjälpare i tumörspridning
För att gå bortom statistiska samband manipulerade teamet GLUD1‑nivåerna i äggstockscellinjer odlade i laboratoriet. När de minskade GLUD1 krympte de fria cellklustren, cancercellerna dog lättare i suspension och cellernas förmåga att migrera i vanliga migrationsprov minskade. När de ökade GLUD1 skedde motsatsen: cellerna motstod död och rörde sig mer aggressivt. I möss som injicerats med äggstocksceller i bukhålan ledde tystnad av GLUD1 till färre tumörnoder på organ som mjälte och lever, långsammare tumörtillväxt och längre överlevnad. Tumörprover från dessa möss visade fler döende celler och färre delande celler, vilket stärker idén att GLUD1 är avgörande för att hålla lossade cancerceller vid liv tillräckligt länge för att bilda nya kolonier.
En skyddande samverkan inne i cancercellen
Forskarna frågade sedan hur GLUD1 utövar detta livsbevarande inflytande. Med hjälp av proteinsökande metoder upptäckte de att GLUD1 fysiskt binder till ett annat protein kallat ARAF, som ingår i en välkänd signalväg som driver cellöverlevnad och tillväxt. Inne i cancerceller sitter GLUD1 och ARAF tillsammans främst i cellvätskan snarare än i energiproducerande strukturer, vilket antyder en signaleringsroll. När GLUD1 minskades sjönk ARAF‑nivåerna, medan dess nära släktingar BRAF och CRAF förblev oförändrade. Denna förlust av ARAF följdes av svagare aktivitet i den nedströms MEK/ERK‑vägen och en förskjutning mot pro‑dödsproteiner. Återinsättning av ARAF i GLUD1‑defekta celler återställde mycket av överlevnadssignaleringen och minskade celldöden, vilket visar att ARAF är en viktig mellanhand som länkar GLUD1 till resistens mot anoikis. 
Hur GLUD1 skyddar en nyckelsignal
Vid vidare undersökningar fann teamet att GLUD1 fungerar som en kroppsgarde som förhindrar att ARAF märks ut och förstörs av cellens proteinåtervinningssystem. När denna återvinningsmaskin kemiskt blockerades vändes minskningen av ARAF som syntes efter GLUD1‑bortfall. Tidsförsök visade att ARAF bröts ner mycket snabbare när GLUD1 saknades, och biokemiska tester avslöjade ökad ”märkning” av ARAF för nedbrytning. Överuttryck av GLUD1 minskade dessa märkningar. Tillsammans indikerar resultaten att GLUD1 stabiliserar ARAF genom att blockera dess nedbrytning, och därigenom håller överlevnadssignalen påslagen i lossade äggstockscancerceller. Intressant nog, även om GLUD1 är mest känd för att hjälpa till i omsättningen av näringsämnet glutamin, kunde tillsats av en av dess metabola produkter bara delvis återställa ARAF och dess signalering, vilket tyder på att GLUD1:s proteinskyddande roll är minst lika viktig som dess enzymatiska aktivitet i detta sammanhang.
Vad detta kan innebära för framtida behandling
Genom att visa hur GLUD1 skyddar ARAF och håller överlevnadsvägar aktiva exponerar denna studie en sårbar punkt i livscykeln för vandrande äggstockscancerceller. Om läkemedel kan utvecklas för att dämpa GLUD1:s stabiliserande effekt på ARAF—eller för att blockera de nedströms MEK/ERK‑signalerna—kan de tvinga lossade cancerceller att genomgå anoikis istället för att bilda nya tumörer i buken. Eftersom GLUD1 också spelar centrala roller i normal cellmetabolism skulle en sådan behandling behöva balansera nytta och biverkningar noggrant. Ändå erbjuder upptäckten av detta GLUD1–ARAF‑partnerskap en tydligare karta över hur äggstockscancer sprider sig och lyfter fram en lovande uppsättning molekylära mål för terapier som syftar till att stoppa sjukdomen innan den kan slå rot i hela kroppen.
Citering: Feng, H., Chen, Y., Wu, G. et al. GLUD1 supports ovarian cancer progression by counteracting anoikis via ARAF/MEK/ERK signaling. npj Precis. Onc. 10, 151 (2026). https://doi.org/10.1038/s41698-026-01349-6
Nyckelord: äggstockscancer, metastasering, resistens mot anoikis, GLUD1, cellsignalering för överlevnad