Clear Sky Science · zh
一种通过二氧化硅纳米颗粒递送、靶向CXCR4的肽可消除胰腺导管腺癌中迁移的癌症干细胞
这项研究为何重要
胰腺癌是最致命的癌症之一,因为它早期扩散且几乎对所有治疗手段都具抵抗性。一个主要罪魁祸首是体内一小群具有移动能力的“种子”肿瘤细胞,它们在体内迁移并在他处重新启动癌症。该研究探讨了这些流动种子如何被其周围环境滋养,并提出了一种新的、高度靶向的实验性疗法——通过微小的二氧化硅纳米颗粒递送——旨在追踪并解除它们的危险性,防止其造成进一步伤害。
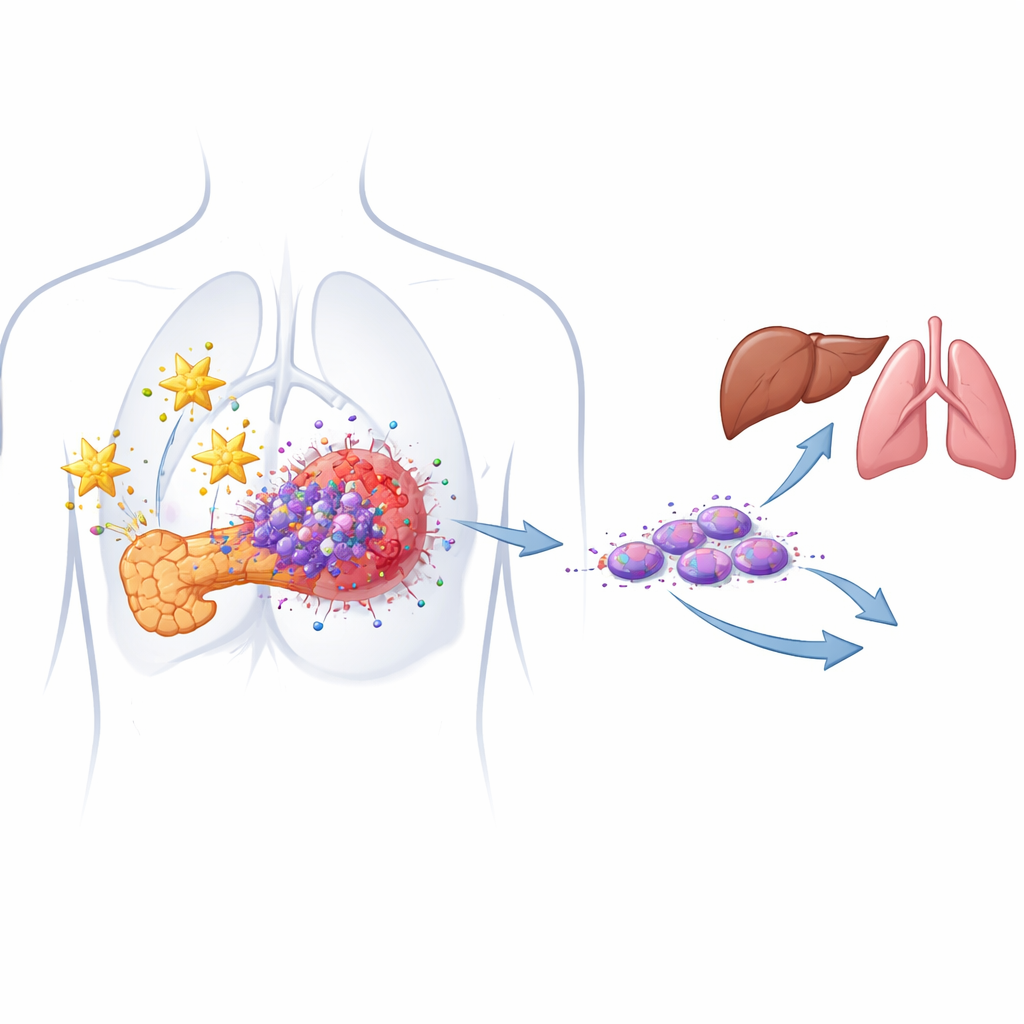
驱动复发的隐匿癌症种子
大多数胰腺肿瘤由外观普通的癌细胞构成,但其中含有一小部分所谓的癌症干细胞。这些细胞能自我更新、耐受化疗并在治疗后再生肿瘤。作者此前鉴定出一类尤其危险的亚群,称为迁移性癌症干细胞,它们表面带有两种标志(CD133 和 CXCR4),并且与转移密切相关。在源自患者的细胞模型中,研究者现在证实与正常组织相比,胰腺肿瘤中这两种标志物都有过度表达,且这些细胞水平更高与疾病更具侵袭性相关联。
肿瘤周边细胞如何助长蔓延
胰腺癌生长在一种致密、瘢痕样的组织中,充斥着被称为胰腺星状细胞的支持细胞。星状细胞并非被动支架,而是积极地“指导”邻近癌细胞。团队通过将来源于患者的肿瘤细胞与星状细胞共同培养或暴露于星状细胞条件培养基来在实验室中重建这种相互作用。他们发现星状细胞释放一种名为 CXCL12 的信号分子,该分子与癌症干细胞表面的 CXCR4 受体结合。此类细胞间对话增强了干性特征,促使细胞由紧凑的上皮形态向更具流动性的间质形态转变,并提高其成球与迁移能力——这些都是与转移和耐药相关的特征。
癌症种子内的关键分子开关
深入研究 CXCR4 下游的信号网络后,研究人员将一个名为 BMI1 的蛋白鉴定为中心控制节点。BMI1 已知有助于正常干细胞维持自我更新。在本研究中,当科学家使用基因工具减少转移性胰腺癌细胞中的 CXCR4 或 BMI1 表达时,细胞失去了许多干性和迁移特征。它们形成的球体减少、向 CXCL12 的迁移减少,并表现出向更有序的上皮状态的回转。在分子层面,阻断该通路减弱了促存活和应激反应回路,并降低了通常促进侵袭和治疗抵抗的通路的激活。
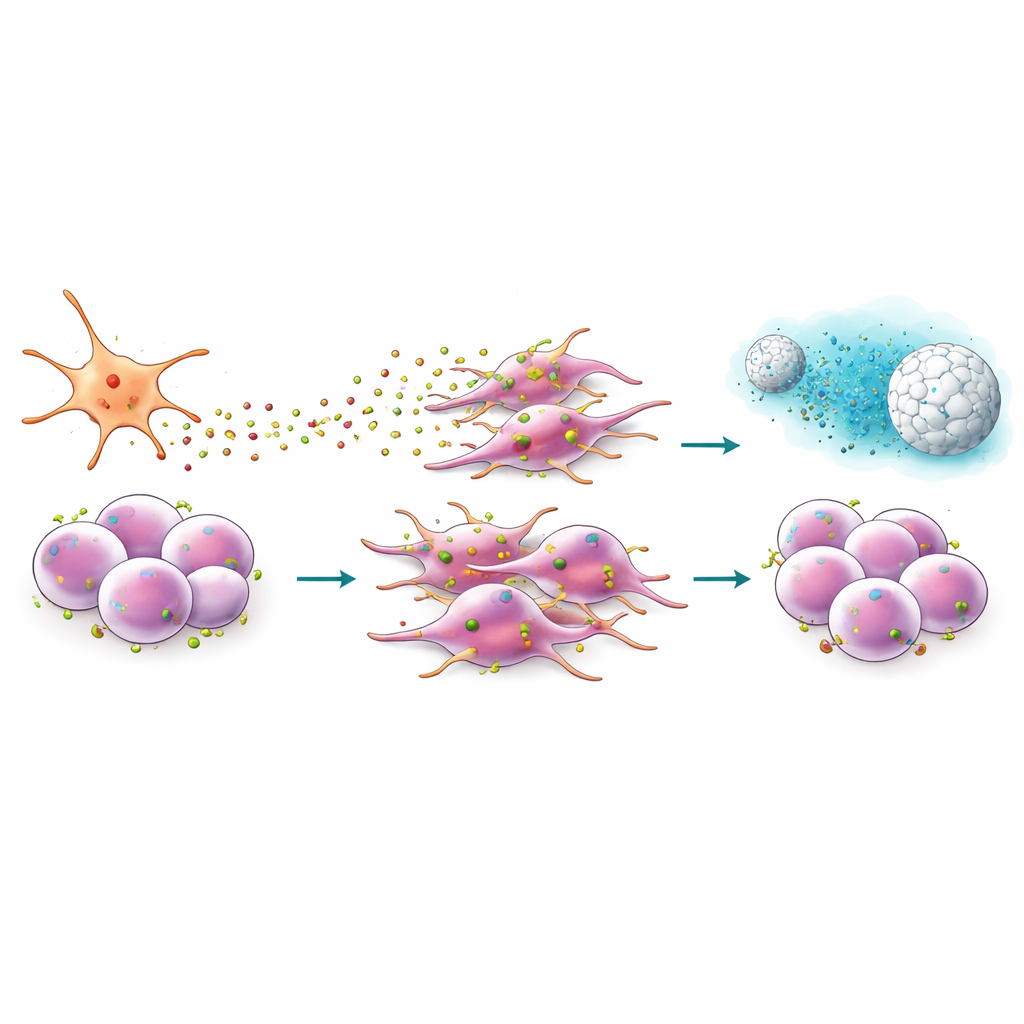
设计肽药物与纳米颗粒以切断信号
由于 CXCR4 位于细胞表面,它为药物提供了一个有吸引力的停靠位点。团队研究了 EPI‑X4 ——一种天然存在的人源肽,可阻断 CXCR4——以及一种经过工程改造、更高效的变体 JM#21。在迁移实验中,这些肽显著降低了癌细胞向 CXCL12 的移动能力,并减弱了与侵袭相关的细胞形态变化。它们还降低了与干性、上皮-间质转化以及肿瘤常常劫持的发育程序(例如 Hedgehog 信号)相关基因的活性。当与常规化疗药物如吉西他滨或紫杉醇联合使用时,JM#21 使先前耐药的细胞显著更易受损,治疗后幸存的癌症干细胞池明显缩小。
用二氧化硅纳米颗粒偷运脆弱药物
肽类药物的一个障碍是它们在血液和常规培养基中会迅速被降解。为克服这一点,研究者将 JM#21 装载到微孔二氧化硅球——介孔二氧化硅纳米颗粒中,这些颗粒像保护性海绵一样缓慢释放肽,同时屏蔽其免受降解。在通常会使游离 JM#21 失活的血清条件下,纳米颗粒结合形式仍然有效:它仍能阻断 CXCL12 驱动的迁移,并在肿瘤与星状细胞的共培养中减少危险的迁移性癌症干细胞比例。基因层面的分析显示,纳米颗粒递送的 JM#21 还降低了耐药标志、抗氧化防御和 BMI1 本身的表达,同时推动细胞回归到较不具侵袭性的状态。
这对患者意味着什么
对非专业读者而言,这项工作的要点在于:胰腺癌中最危险的细胞依赖于与其周围环境的对话以及一组特定的分子开关来保持移动性、干性和耐药性。通过用特制肽中断 CXCL12–CXCR4–BMI1 轴,并将该肽装入二氧化硅纳米颗粒以保持其稳定,研究者展示了在实验室模型中削弱这些转移性“种子”并提高化疗效果的可行性。尽管仍需进一步的动物和临床研究,但这一方法为不仅仅缩小肿瘤体积,而是靶向驱动扩散与复发的根源细胞的治疗提供了有希望的蓝图。
引用: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
关键词: 胰腺癌, 癌症干细胞, 肿瘤微环境, CXCR4抑制剂, 纳米颗粒药物递送