Clear Sky Science · ru
Пептид, нацеленный на CXCR4, доставляемый кремнезёмными наночастицами, уничтожает мигрирующие раковые стволовые клетки при протоковой аденокарциноме поджелудочной железы
Почему это исследование важно
Рак поджелудочной железы — один из самых смертоносных видов рака, потому что он рано дает метастазы и почти не поддаётся большинству применяемых врачами методов лечения. Главным виновником является небольшая подвижная группа «зернообразных» клеток опухоли, которые перемещаются по организму и заново запускают развитие рака в других участках. В этом исследовании изучают, как эти блуждающие «семена» подпитываются окружающей средой, и предлагают новую, высокоизбирательную экспериментальную терапию — доставляемую с помощью крошечных кремнезёмных наночастиц — целью которой является выследить и обезвредить их до того, как они вызовут новое распространение болезни.
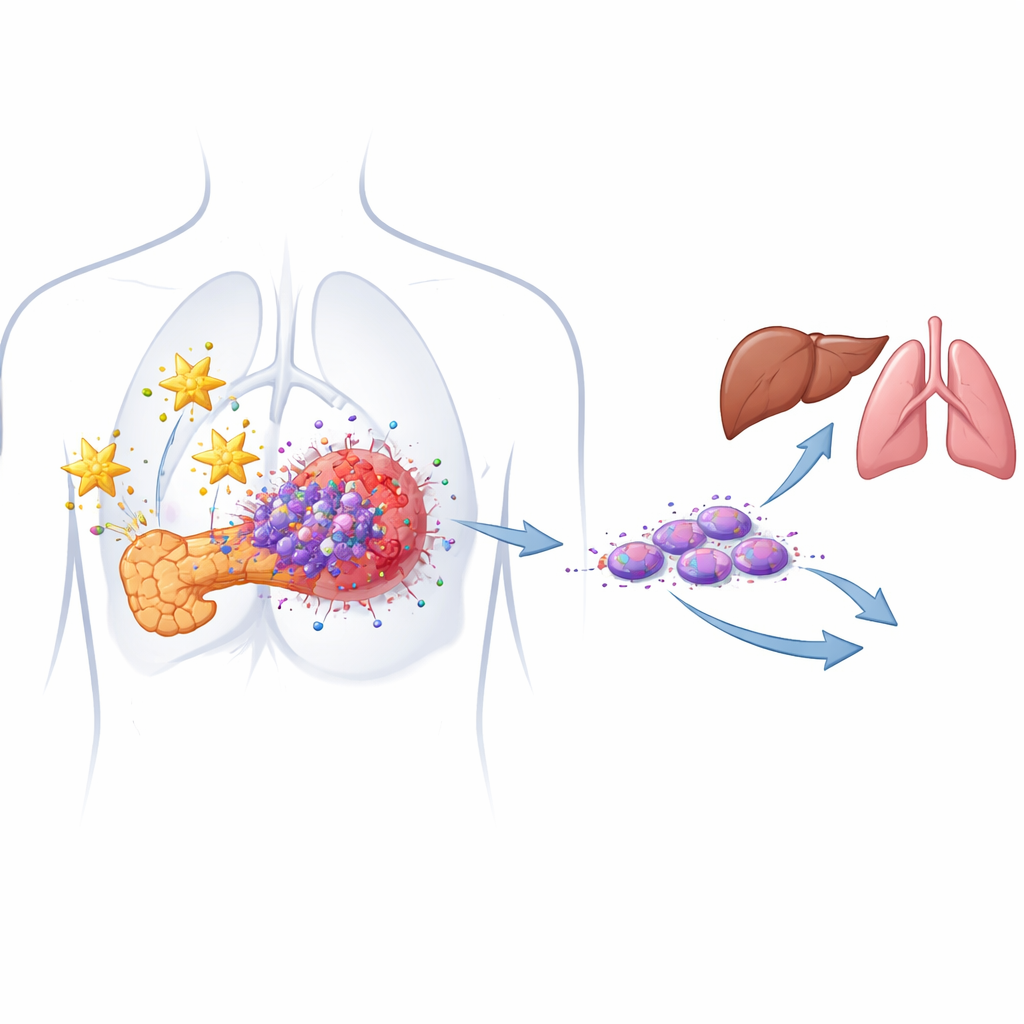
Скрытые раковые «семена», приводящие к рецидиву
Большинство опухолей поджелудочной железы состоит из клеток, похожих на обычные раковые клетки, но внутри них укрывается меньшинство — так называемые раковые стволовые клетки. Эти клетки способны к самоподдержанию, выживают после химиотерапии и способны восстановить опухоль после лечения. Авторы ранее выделили особенно опасный подтип — мигрирующие раковые стволовые клетки, которые несут два поверхностных маркера (CD133 и CXCR4) и тесно связаны с метастазированием. В моделях, полученных от пациентов, они подтвердили, что оба маркера сверхэкспрессированы в опухолях поджелудочной железы по сравнению с нормальной тканью, и что более высокий уровень этих клеток коррелирует с более агрессивным течением болезни.
Как соседи опухоли раздувают пламя
Рак поджелудочной железы развивается в плотной рубцовой ткани, насыщенной поддерживающими клетками — звездчатыми клетками поджелудочной железы. Эти клетки, далёкие от пассивного «каркаса», активно «наставляют» соседние раковые клетки. Команда воспроизвела это взаимодействие в лаборатории, со- культивируя опухолевые клетки, полученные от пациентов, со звездчатыми клетками или подвергая их действию кондиционированной среды от звездчатых клеток. Они обнаружили, что звездчатые клетки выделяют сигнальную молекулу CXCL12, которая связывается с рецептором CXCR4 на раковых стволовых клетках. Этот диалог усиливает стволоподобные свойства, побуждает клетки переходить от компактной эпителиальной формы к более подвижной мезенхимальной, и повышает их способность образовывать сферы и мигрировать — признаки, связанные с метастазированием и устойчивостью к лечению.
Ключевой молекулярный переключатель в раковых «семенах»
Углубляясь в сигнальную сеть, располагающуюся ниже по каскаду CXCR4, исследователи выявили белок BMI1 как центральный узел управления. BMI1 известен тем, что помогает нормальным стволовым клеткам поддерживать способность к самоподновлению. В этой работе, когда учёные использовали генетические инструменты для снижения уровня CXCR4 или BMI1 в метастатических клетках рака поджелудочной железы, клетки теряли многие стволоподобные и миграционные свойства. Они образовывали меньше сфер, слабее двигались в направлении CXCL12 и демонстрировали сдвиг обратно к более упорядоченному эпителиальному состоянию. На молекулярном уровне блокирование этого пути притупляло про-выживаемые и стресс-ответные цепочки и снижало активацию путей, которые обычно подпитывают инвазию и устойчивость к терапии.
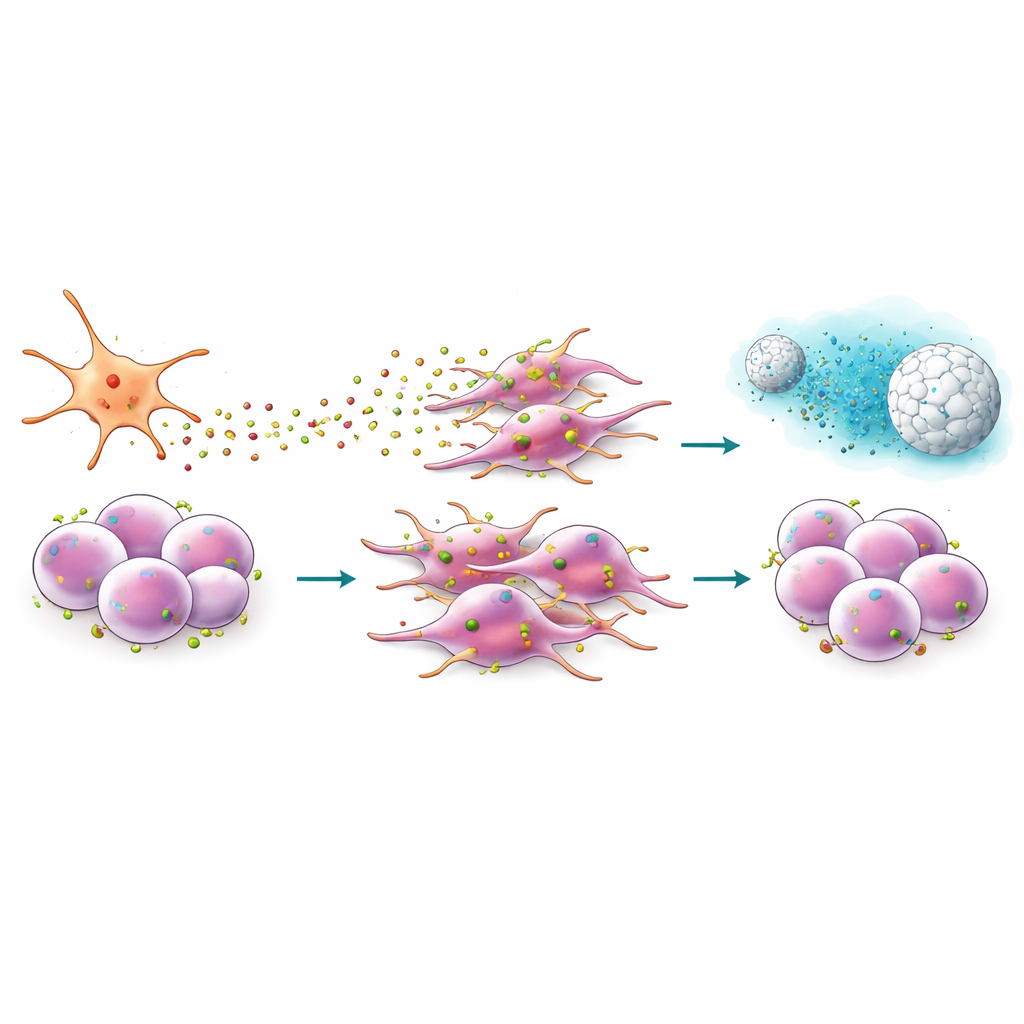
Разработка пептида и наночастицы для разрыва сигнала
Поскольку CXCR4 располагается на поверхности клетки, он представляет привлекательную мишень для препаратов. Команда изучала EPI‑X4, естественный человеческий пептид, блокирующий CXCR4, и инженерную, более мощную версию JM#21. В экспериментах на миграцию эти пептиды резко снижали способность раковых клеток двигаться в направлении CXCL12 и смягчали изменения формы клеток, связанные с инвазией. Они также понижали активность генов, связанных со стволовостью, эпителиально‑мезенхимальным переходом и сигнальным путём развития (Hedgehog), который часто перехватывают опухоли. В сочетании с стандартными химиотерапиями, такими как гемцитабин или паклитаксел, JM#21 делал ранее устойчивые клетки значительно более уязвимыми, сокращая пул выживших раковых стволовых клеток после лечения.
Перевозка хрупких препаратов в кремнезёмных наночастицах
Одна из проблем использования пептидов как лекарств в том, что они быстро разрушаются в крови и в обычных культуральных средах. Чтобы обойти это, исследователи загрузили JM#21 в крошечные пористые кремнезёмные сферы — мезопористые кремнезёмные наночастицы — которые работают как защитные губки, медленно высвобождая пептид и предохраняя его от разложения. В сыворотсодержащих условиях, которые обычно инактивируют свободный JM#21, форма, связанная с наночастицами, сохраняла функциональность: она по‑прежнему блокировала миграцию, вызванную CXCL12, и снижала долю опасных мигрирующих раковых стволовых клеток в со-культурах опухолевых и звездчатых клеток. Анализы на уровне генов показали, что доставляемый наночастицами JM#21 также ослаблял маркеры лекарственной устойчивости, антиоксидантные защиты и сам BMI1, одновременно подталкивая клетки к менее агрессивному состоянию.
Что это может означать для пациентов
Для непрофессионала суть этой работы в том, что наиболее опасные клетки рака поджелудочной железы зависят от взаимодействия с окружающей средой и от конкретного молекулярного переключателя, чтобы оставаться подвижными, стволоподобными и устойчивыми к лекарствам. Прерывая ось CXCL12–CXCR4–BMI1 с помощью специально подобранного пептида и упаковывая этот пептид в кремнезёмные наночастицы для сохранения его стабильности, исследователи показывают, что можно ослабить эти метастатические «семена» и сделать химиотерапию более эффективной в лабораторных моделях. Хотя необходимы дополнительные исследования на животных и клинические испытания, этот подход предлагает перспективную схему терапии, направленную не только на уменьшение размеров опухолей, но и на корневые клетки, которые приводят к распространению и рецидиву.
Цитирование: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Ключевые слова: рак поджелудочной железы, раковые стволовые клетки, опухолевый микросреда, ингибиторы CXCR4, наночастичная доставка препаратов