Clear Sky Science · sv
Ett CXCR4‑inriktat peptid levererat av kiselnanopartiklar eliminerar migrerande cancerceller med stamcellsegenskaper i pankreasslemhinnekörtelcancer
Varför denna forskning är viktig
Bukspottkörtelcancer är en av de dödligaste cancerformerna eftersom den sprider sig tidigt och motstår nästan alla behandlingar som sätts in. En viktig bov är en liten, rörlig grupp av tumör"frö"celler som färdas genom kroppen och återstartar cancer på andra platser. Denna studie undersöker hur dessa vandrande frön stöds av sin omgivning och introducerar en ny, mycket riktad experimentell terapi—levererad med små kiselnanopartiklar—som syftar till att spåra upp och oskadliggöra dem innan de kan orsaka mer skada.
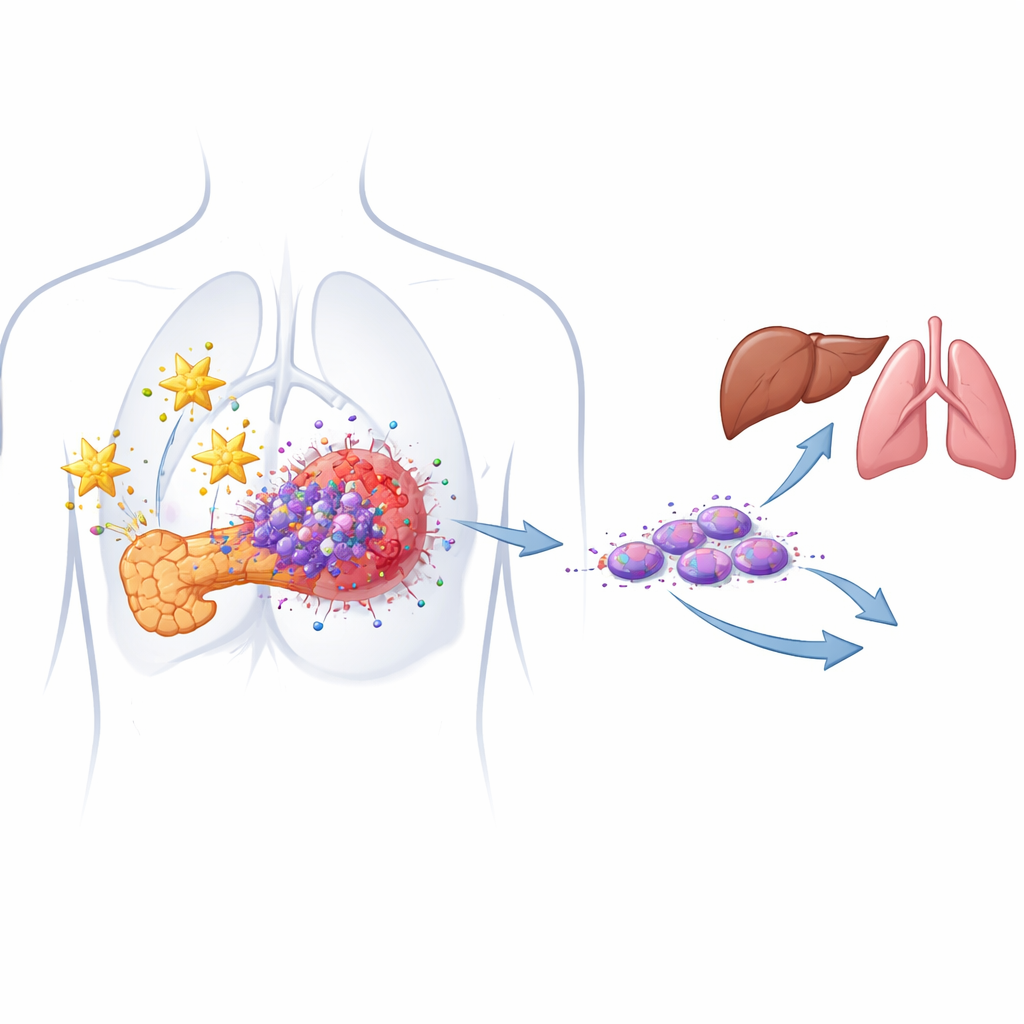
De dolda cancerväxterna som driver återfall
De flesta pankreastumörer består av vanligt utseende cancerceller, men inbäddat i dem finns en minoritet av så kallade cancerceller med stamcellsegenskaper. Dessa celler kan självförnya sig, överleva kemoterapi och återbilda en tumör efter behandling. Författarna identifierade tidigare en särskilt farlig undergrupp kallad migrerande cancerceller med stamcellsegenskaper, som bär två ytmarkörer (CD133 och CXCR4) och är starkt kopplade till metastasering. I patient‑härledda cellmodeller bekräftar de nu att båda markörerna överproduceras i pankreastumörer jämfört med normalt vävnad och att högre nivåer av dessa celler korrelerar med en mer aggressiv sjukdom.
Hur tumörens grannar eldar på
Pankreascancer växer i en tät, ärrlik vävnad som är fylld av stödjeceller kallade pankreatiska stellatceller. Långt ifrån att vara passiv stomme, "coachar" dessa stellatceller aktivt närliggande cancerceller. Teamet återskapade denna interaktion i laboratoriet genom att samodla patient‑härledda tumörceller med stellatceller eller genom att utsätta dem för medium betingat av stellatceller. De fann att stellatceller frisätter ett signalsubstans kallat CXCL12, som binder till CXCR4‑receptorn på cancerceller med stamcellsegenskaper. Denna korsprat förstärker stamcellsliknande egenskaper, uppmuntrar celler att gå från en kompakt, epitelial form till en mer mobil, mesenkymal form, och gör dem bättre på att bilda sfärer och migrera—egenskaper som förknippas med metastasering och läkemedelsresistens.
En nyckelswitch i de maligna fröna
När forskarna grävde djupare i det signalnätverk som följer efter CXCR4 identifierade de ett protein kallat BMI1 som en central kontrollpunkt. BMI1 är känt för att hjälpa normala stamceller att bevara sin självförnyelse. Här, när forskarna använde genetiska verktyg för att minska antingen CXCR4 eller BMI1 i metastatiska pankreascancerceller, förlorade cellerna många av sina stamcellsliknande och migratoriska egenskaper. De bildade färre sfärer, rörde sig mindre mot CXCL12 och visade en återgång mot ett mer ordnat, epitelialt tillstånd. På molekylär nivå dämpade blockering av denna bana överlevnads‑ och stressresponssystem och minskade aktiveringen av vägar som normalt driver invasion och terapiresistens.
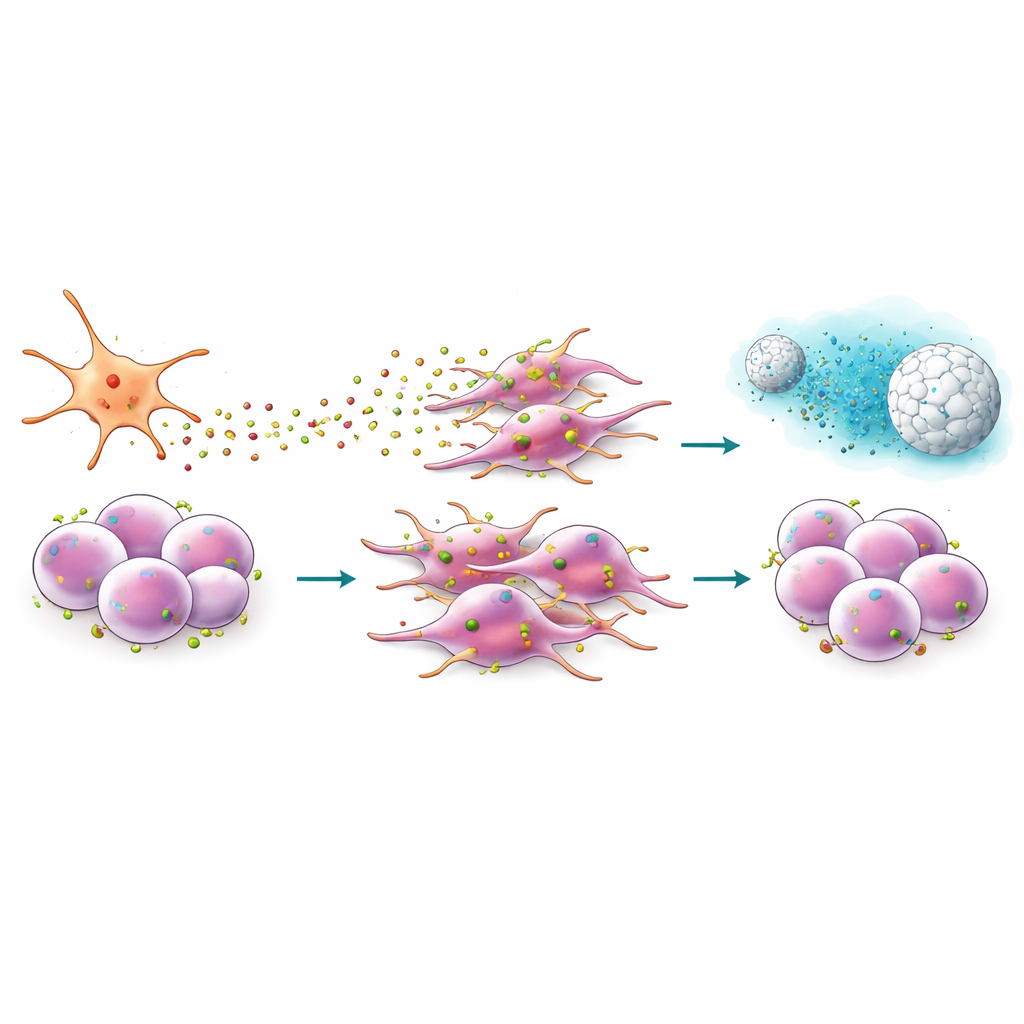
Design av ett peptid och en nanopartikel för att kapa signalen
Eftersom CXCR4 sitter på cellens yta erbjuder den en attraktiv plats för läkemedel att fästa vid. Teamet studerade EPI‑X4, ett naturligt förekommande mänskligt peptid som blockerar CXCR4, och en konstruerad, mer potent version kallad JM#21. I migrationsförsök minskade dessa peptider kraftigt cancercellernas förmåga att röra sig mot CXCL12 och dämpade de formförändringar som är förknippade med invasion. De sänkte också aktiviteten hos gener kopplade till stamcellsegenskaper, epitel‑till‑mesenkymal övergång och ett utvecklingsprogram (Hedgehog‑signalering) som ofta utnyttjas av tumörer. När JM#21 kombinerades med standardkemoterapier som gemcitabin eller paklitaxel blev tidigare resistenta celler mycket mer sårbara, vilket krympte poolen av överlevande cancerceller med stamcellsegenskaper efter behandling.
Smuggling av bräckliga läkemedel med kiselnanopartiklar
Ett hinder för att använda peptider som läkemedel är att de snabbt bryts ner i blod och i konventionella odlingsmedium. För att övervinna detta lastade forskarna JM#21 i små, porösa kiselsfärer—mesoporösa kiselnanopartiklar—som fungerar som skyddande svampar och långsamt frigör peptiden samtidigt som de skyddar den från nedbrytning. I seruminnehållande förhållanden som normalt inaktiverar fri JM#21 förblev nanopartikelbunden form funktionell: den blockerade fortfarande CXCL12‑driven migration och minskade andelen farliga migrerande cancerceller med stamcellsegenskaper i samodlingar av tumör‑ och stellatceller. Genanalyser visade att nanopartikel‑levererad JM#21 också dämpade markörer för läkemedelsresistens, antioxidantförsvar och BMI1 självt, samtidigt som den knuffade cellerna tillbaka mot ett mindre aggressivt tillstånd.
Vad detta kan betyda för patienter
För en lekman är budskapet i detta arbete att bukspottkörtelns farligaste celler är beroende av en dialog med sin omgivning och av en specifik molekylär switch för att förbli mobila, stamcellsliknande och läkemedelsresistenta. Genom att avbryta CXCL12–CXCR4–BMI1‑axeln med ett skräddarsytt peptid, och genom att paketera det peptidet i kiselnanopartiklar för att hålla det stabilt, visar forskarna att det är möjligt att försvaga dessa metastatiska frön och göra kemoterapi mer effektiv i laboratoriemodeller. Medan vidare djur‑ och kliniska studier krävs erbjuder detta angreppssätt en lovande ritning för terapier som inte bara krymper tumörer, utan också riktar sig mot de rotceller som driver spridning och återfall.
Citering: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Nyckelord: bukspottkörtelcancer, cancerceller med stamcellsegenskaper, tumörmikromiljö, CXCR4‑hämmare, nanopartikelleverans av läkemedel