Clear Sky Science · fr
Un peptide ciblant CXCR4 délivré par des nanoparticules de silice élimine les cellules souches cancéreuses migrantes dans l’adénocarcinome canalaire pancréatique
Pourquoi cette recherche est importante
Le cancer du pancréas est l’un des plus meurtriers parce qu’il se propage tôt et résiste à presque tous les traitements disponibles. Un responsable majeur est un petit groupe mobile de cellules « graines » tumorales qui voyagent dans l’organisme et réenclenchent la maladie ailleurs. Cette étude examine comment ces graines errantes sont soutenues par leur environnement et présente une nouvelle thérapie expérimentale très ciblée — délivrée par de minuscules nanoparticules de silice — visant à les localiser et à les neutraliser avant qu’elles ne provoquent d’autres dégâts.
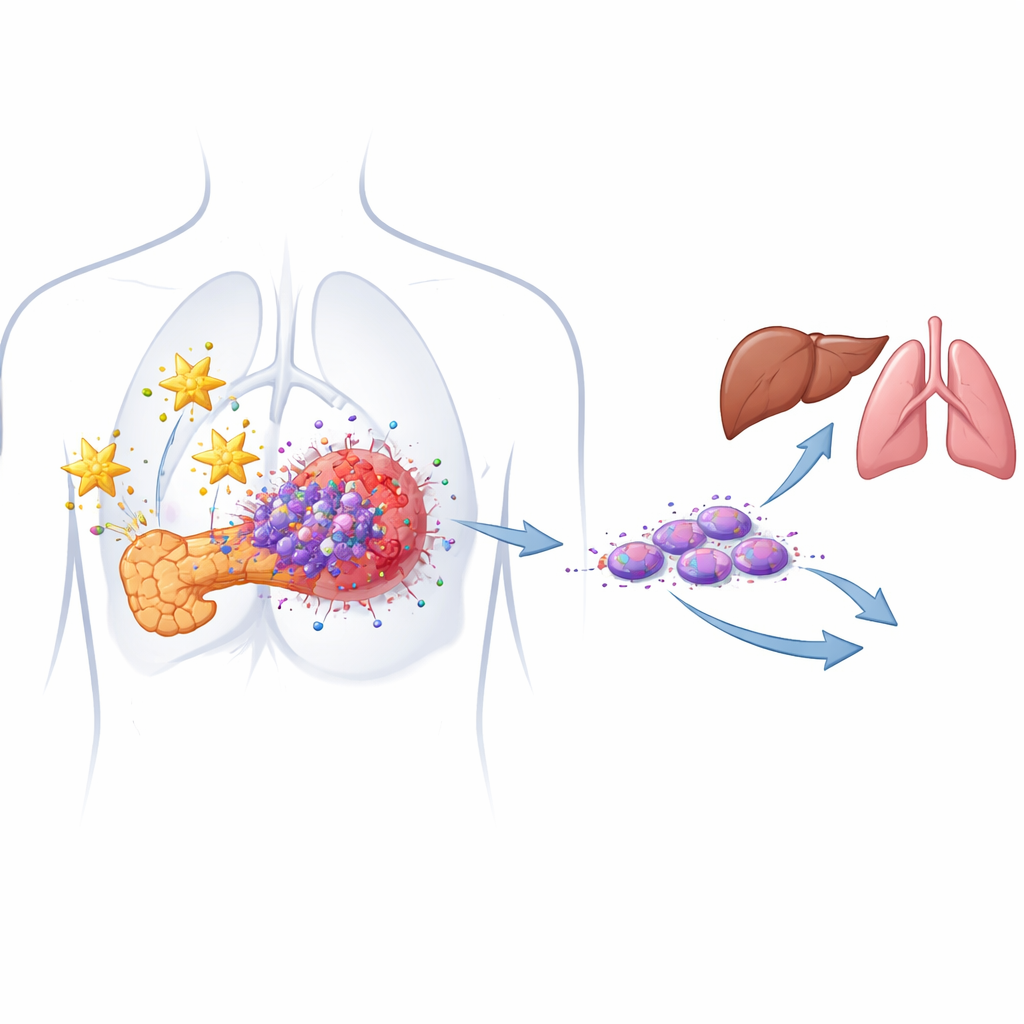
Les graines cancéreuses cachées qui provoquent la récidive
La plupart des tumeurs pancréatiques sont composées de cellules cancéreuses d’apparence ordinaire, mais nichée en leur sein se trouve une minorité de cellules dites souches cancéreuses. Ces cellules peuvent s’auto-renouveler, survivre à la chimiothérapie et régénérer une tumeur après le traitement. Les auteurs avaient précédemment identifié un sous‑ensemble particulièrement dangereux appelé cellules souches cancéreuses migrantes, qui portent deux marqueurs de surface (CD133 et CXCR4) et sont fortement associés aux métastases. Dans des modèles cellulaires dérivés de patients, ils confirment maintenant que ces deux marqueurs sont surproduits dans les tumeurs pancréatiques par rapport au tissu normal et que des niveaux plus élevés de ces cellules corrèlent avec une maladie plus agressive.
Comment les voisins de la tumeur attisent l’agressivité
Les cancers du pancréas se développent dans un tissu dense, semblable à une cicatrice, rempli de cellules de soutien appelées cellules étoilées pancréatiques. Loin d’être un simple échafaudage, ces cellules étoilées « coachent » activement les cellules cancéreuses voisines. L’équipe a recréé cette interaction en laboratoire en co‑cultivant des cellules tumorales dérivées de patients avec des cellules étoilées ou en les exposant au milieu conditionné par ces cellules. Ils ont constaté que les cellules étoilées libèrent une molécule de signalisation appelée CXCL12, qui se lie au récepteur CXCR4 sur les cellules souches cancéreuses. Cette communication renforce les traits de type souche, favorise la transition d’une forme épithéliale compacte vers une forme mésenchymateuse plus mobile, et augmente la capacité des cellules à former des sphères et à migrer — des caractéristiques associées aux métastases et à la résistance aux médicaments.
Un commutateur moléculaire clé à l’intérieur des graines cancéreuses
En approfondissant le réseau de signalisation en aval de CXCR4, les chercheurs ont identifié une protéine appelée BMI1 comme un nœud de contrôle central. BMI1 est connue pour aider les cellules souches normales à maintenir leur auto‑renouvellement. Ici, lorsque les scientifiques ont utilisé des outils génétiques pour réduire soit CXCR4 soit BMI1 dans des cellules de cancer pancréatique métastatique, les cellules ont perdu une grande partie de leurs caractéristiques de type souche et migratoires. Elles ont formé moins de sphères, migré moins vers le CXCL12 et ont montré une réversion vers un état plus épithélial et ordonné. Au niveau moléculaire, le blocage de cette voie a atténué les circuits pro‑survie et de réponse au stress et réduit l’activation des voies qui alimentent normalement l’invasion et la résistance thérapeutique.
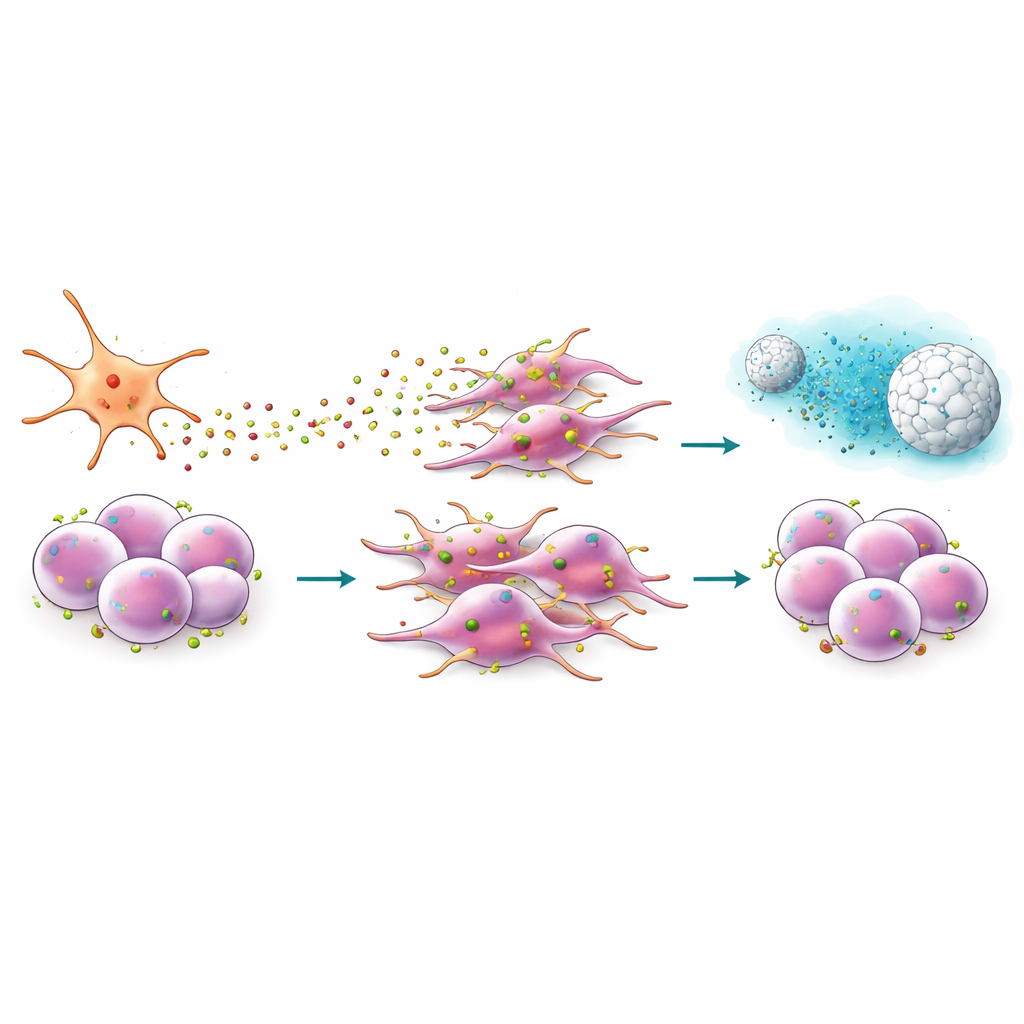
Conception d’un peptide et d’une nanoparticule pour interrompre le signal
Parce que CXCR4 se trouve à la surface cellulaire, il offre un site d’ancrage attractif pour les médicaments. L’équipe a étudié l’EPI‑X4, un peptide humain naturel qui bloque CXCR4, ainsi qu’une version modifiée et plus puissante appelée JM#21. Dans des expériences de migration, ces peptides ont fortement réduit la capacité des cellules cancéreuses à se déplacer vers le CXCL12 et ont atténué les changements de forme cellulaire associés à l’invasion. Ils ont également abaissé l’activité des gènes liés à la « stemness », à la transition épithélio‑mésenchymateuse et à un programme de développement (signalisation Hedgehog) souvent détourné par les tumeurs. Associé à des chimiothérapies standards comme la gemcitabine ou le paclitaxel, JM#21 a rendu des cellules auparavant résistantes beaucoup plus vulnérables, réduisant le pool de cellules souches cancéreuses survivantes après traitement.
Faire entrer des médicaments fragiles dans des nanoparticules de silice
Un obstacle à l’utilisation des peptides comme médicaments est qu’ils sont rapidement dégradés dans le sang et dans les milieux de culture classiques. Pour contourner ce problème, les chercheurs ont chargé JM#21 dans de minuscules sphères de silice poreuse — des nanoparticules de silice mésoporeuse — qui agissent comme des éponges protectrices, libérant lentement le peptide tout en le protégeant de la dégradation. Dans des conditions contenant du sérum qui inactivent normalement JM#21 libre, la forme liée aux nanoparticules est restée fonctionnelle : elle bloquait toujours la migration induite par CXCL12 et réduisait la fraction des dangereuses cellules souches cancéreuses migrantes dans des co‑cultures de cellules tumorales et de cellules étoilées. Des analyses au niveau des gènes ont montré que JM#21 délivré par nanoparticules diminuait également les marqueurs de résistance aux médicaments, les défenses antioxydantes et BMI1 lui‑même, tout en poussant les cellules vers un état moins agressif.
Ce que cela pourrait signifier pour les patients
Pour un non‑spécialiste, le message de ce travail est que les cellules les plus dangereuses du cancer du pancréas dépendent d’un dialogue avec leur environnement et d’un commutateur moléculaire spécifique pour rester mobiles, de type souche et résistantes aux traitements. En interrompant l’axe CXCL12–CXCR4–BMI1 avec un peptide conçu pour cet effet, et en encapsulant ce peptide dans des nanoparticules de silice pour le stabiliser, les chercheurs montrent qu’il est possible d’affaiblir ces graines métastatiques et de rendre la chimiothérapie plus efficace dans des modèles de laboratoire. Bien que des études animales et cliniques complémentaires soient nécessaires, cette approche offre un plan prometteur pour des thérapies qui ne se contentent pas de réduire la taille des tumeurs, mais ciblent aussi les cellules à l’origine de la dissémination et de la récidive.
Citation: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Mots-clés: cancer du pancréas, cellules souches cancéreuses, microenvironnement tumoral, inhibiteurs de CXCR4, nanoparticules pour l’administration de médicaments