Clear Sky Science · es
Un péptido dirigido a CXCR4 entregado por nanopartículas de sílice elimina células madre cancerosas migrantes en adenocarcinoma ductal pancreático
Por qué esta investigación importa
El cáncer de páncreas es uno de los más letales porque se disemina pronto y resiste casi todos los tratamientos disponibles. Un factor clave es un pequeño grupo móvil de células “semilla” tumorales que viajan por el cuerpo y reactivan el cáncer en otros órganos. Este estudio examina cómo el entorno tumoral alimenta a esas semillas errantes e introduce una nueva terapia experimental muy dirigida —entregada mediante diminutas nanopartículas de sílice— que pretende localizar y desactivar esas células antes de que causen más daño.
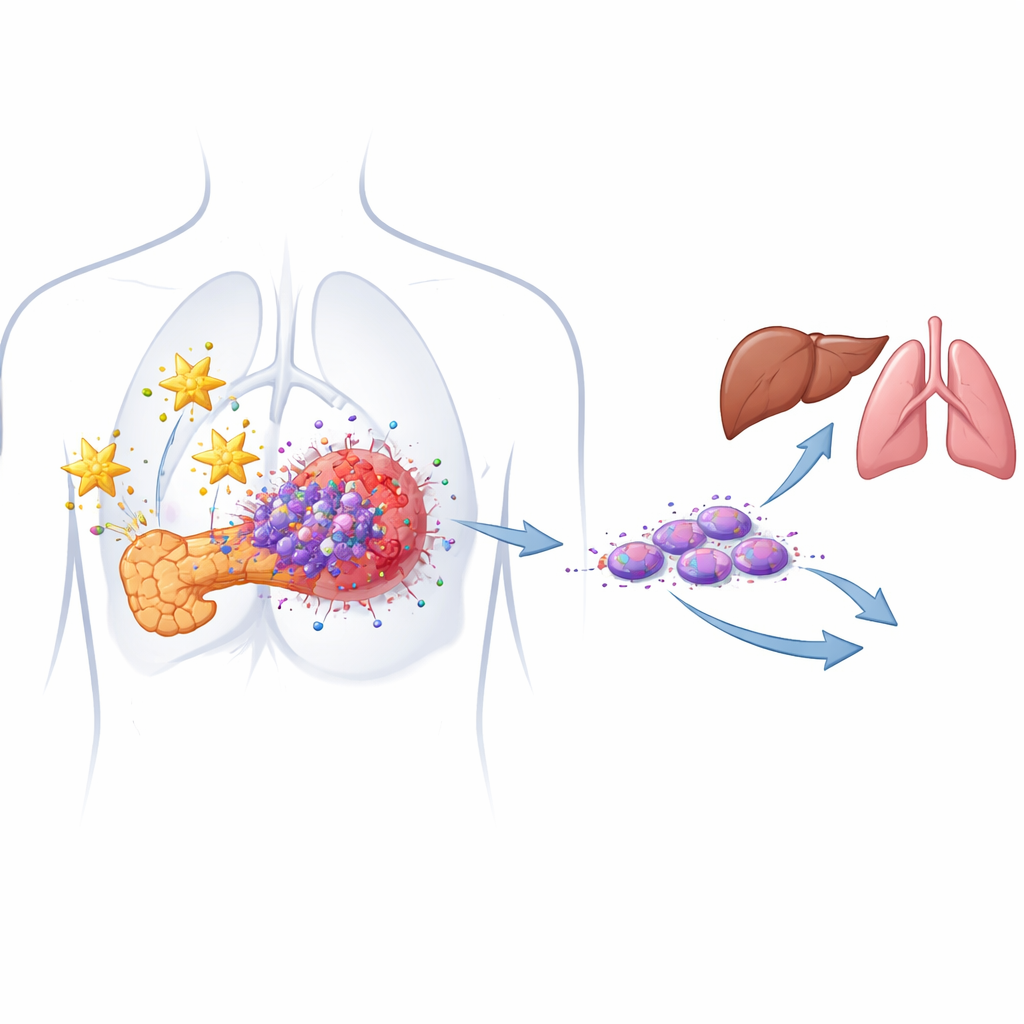
Las semillas ocultas del cáncer que impulsan la recaída
La mayoría de los tumores pancreáticos están compuestos por células cancerosas de aspecto convencional, pero en su interior existe una minoría conocida como células madre cancerosas. Estas células pueden autorrenovarse, sobrevivir a la quimioterapia y regenerar un tumor tras el tratamiento. Los autores identificaron previamente un subconjunto especialmente peligroso llamado células madre cancerosas migrantes, que expresan dos marcadores de superficie (CD133 y CXCR4) y se asocian fuertemente con la metástasis. En modelos celulares derivados de pacientes, confirman ahora que ambos marcadores están sobrerrepresentados en tumores pancreáticos respecto al tejido normal y que niveles más altos de estas células se correlacionan con una enfermedad más agresiva.
Cómo los vecinos del tumor avivan las llamas
Los cánceres pancreáticos crecen en un tejido denso, similar a una cicatriz, lleno de células de soporte llamadas células estrelladas pancreáticas. Lejos de ser un andamiaje pasivo, estas células estrelladas “asesoran” activamente a las células cancerosas cercanas. El equipo recreó esta interacción en el laboratorio co‑cultivando células tumorales derivadas de pacientes con células estrelladas o exponiéndolas a un medio condicionado por células estrelladas. Hallaron que las estrelladas liberan una molécula señal llamada CXCL12, que se une al receptor CXCR4 en las células madre cancerosas. Este diálogo potencia rasgos de tipo madre, fomenta que las células cambien de una forma compacta y epitelial a una más móvil y mesenquimal, y aumenta su capacidad de formar esferas y migrar —características asociadas a metástasis y resistencia a fármacos.
Un interruptor molecular clave dentro de las semillas cancerosas
Profundizando en la red de señalización aguas abajo de CXCR4, los investigadores identificaron a la proteína BMI1 como un nodo central de control. Se sabe que BMI1 ayuda a las células madre normales a mantener su autorrenovación. Aquí, cuando los científicos utilizaron herramientas genéticas para reducir CXCR4 o BMI1 en células pancreáticas metastásicas, las células perdieron muchos de sus rasgos de tipo madre y migratorios. Formaron menos esferas, se movieron menos hacia CXCL12 y mostraron un retorno hacia un estado más ordenado y epitelial. A nivel molecular, bloquear esta vía atenuó circuitos de supervivencia y respuesta al estrés y redujo la activación de rutas que normalmente alimentan la invasión y la resistencia a la terapia.
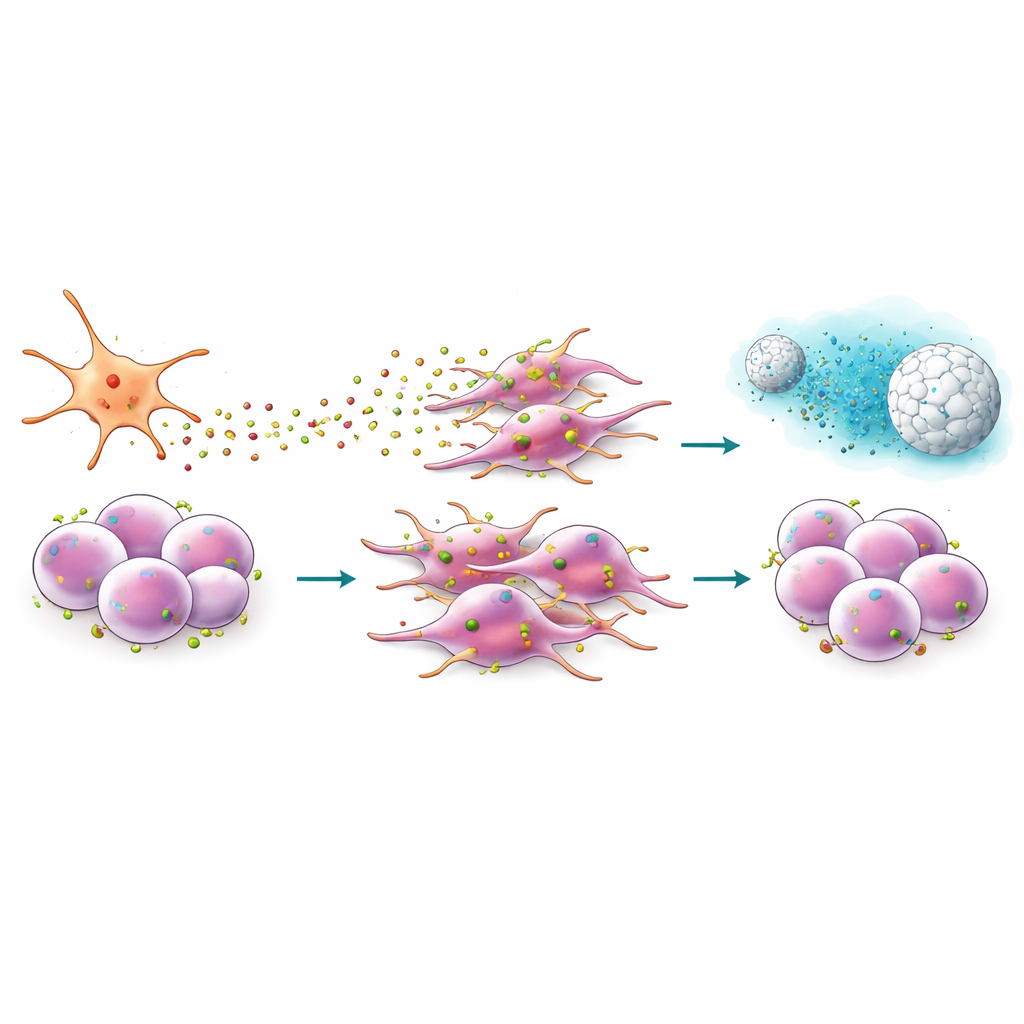
Diseñar un péptido y una nanopartícula para cortar la señal
Dado que CXCR4 se encuentra en la superficie celular, ofrece un punto de anclaje atractivo para fármacos. El equipo estudió EPI‑X4, un péptido humano de origen natural que bloquea CXCR4, y una versión diseñada, más potente, llamada JM#21. En experimentos de migración, estos péptidos redujeron drásticamente la capacidad de las células cancerosas de moverse hacia CXCL12 y mitigaron los cambios morfológicos asociados a la invasión. También disminuyeron la actividad de genes relacionados con la pluripotencia, la transición epitelio‑mesenquimal y un programa de desarrollo (señalización Hedgehog) que los tumores suelen secuestrar. Cuando se combinaron con quimioterapias estándar como gemcitabina o paclitaxel, JM#21 volvió mucho más vulnerables a células previamente resistentes, reduciendo la reserva de células madre cancerosas supervivientes tras el tratamiento.
Contrabandear fármacos frágiles con nanopartículas de sílice
Un obstáculo para usar péptidos como fármacos es que se degradan rápidamente en sangre y en los medios de cultivo convencionales. Para sortear esto, los investigadores cargaron JM#21 en pequeñas esferas porosas de sílice —nanopartículas de sílice mesoporosa— que actúan como esponjas protectoras, liberando el péptido de forma sostenida mientras lo protegen de la degradación. En condiciones con suero que normalmente inactivan el JM#21 libre, la forma ligada a nanopartículas permaneció funcional: seguía bloqueando la migración impulsada por CXCL12 y reduciendo la fracción de peligrosas células madre cancerosas migrantes en co‑cultivos de tumor y células estrelladas. Los análisis a nivel génico mostraron que JM#21 administrado por nanopartículas también atenuó marcadores de resistencia a fármacos, defensas antioxidantes y la propia BMI1, al tiempo que empujó a las células hacia un estado menos agresivo.
Qué podría significar esto para los pacientes
Para un lector no especializado, la conclusión es que las células más peligrosas del cáncer de páncreas dependen de una conversación con su entorno y de un interruptor molecular específico para mantener su movilidad, características de madre y resistencia a fármacos. Al interrumpir el eje CXCL12–CXCR4–BMI1 con un péptido diseñado, y empaquetando ese péptido en nanopartículas de sílice para mantener su estabilidad, los investigadores muestran que es posible debilitar estas semillas metastásicas y aumentar la eficacia de la quimioterapia en modelos de laboratorio. Aunque hacen falta más estudios en animales y ensayos clínicos, este enfoque ofrece un plano prometedor para terapias que no solo reducen tumores, sino que también atacan las células raíz que impulsan la diseminación y la recaída.
Cita: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Palabras clave: cáncer de páncreas, células madre cancerosas, microambiente tumoral, inhibidores de CXCR4, liberación de fármacos con nanopartículas