Clear Sky Science · de
Ein auf CXCR4 zielendes Peptid, das mittels Silika-Nanopartikeln geliefert wird, eliminiert migrierende Krebsstammzellen beim duktalen pankreatischen Adenokarzinom
Warum diese Forschung wichtig ist
Pankreaskrebs gehört zu den tödlichsten Krebsarten, weil er früh metastasiert und fast jeder Therapie widersteht. Ein wesentlicher Verursacher ist eine kleine, mobile Gruppe von Tumor‑„Samen“zellen, die durch den Körper wandern und an anderen Stellen den Krebs neu starten. Diese Studie untersucht, wie diese wandernden Samen von ihrer Umgebung gefördert werden, und stellt eine neue, hochgradig zielgerichtete experimentelle Therapie vor – geliefert von winzigen Silika‑Nanopartikeln –, die darauf abzielt, sie aufzuspüren und zu deaktivieren, bevor sie weiteren Schaden anrichten können.
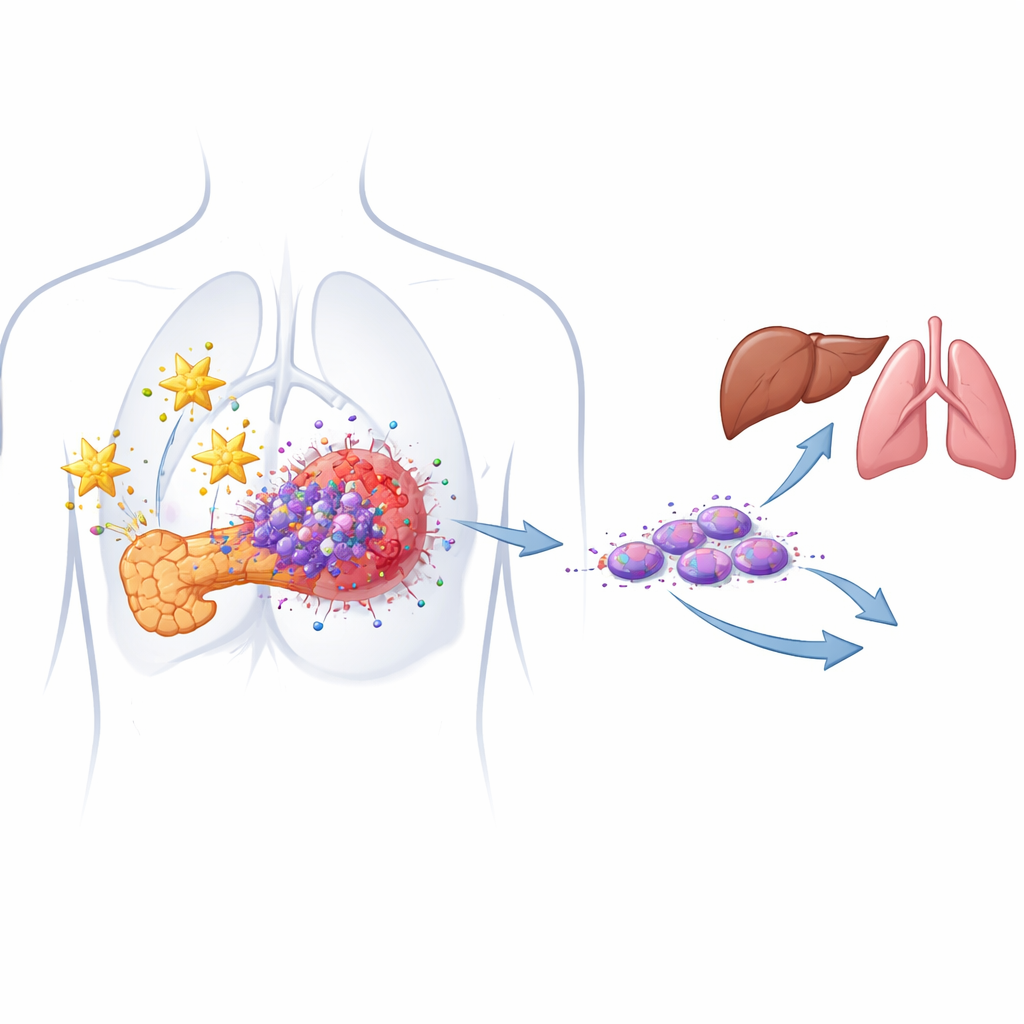
Die verborgenen Krebs‑Samen, die Rückfälle antreiben
Die meisten Pankreastumoren bestehen aus normal aussehenden Krebszellen, doch eingebettet in ihnen befindet sich eine Minderheitspopulation sogenannter Krebsstammzellen. Diese Zellen können sich selbst erneuern, Chemotherapie überleben und nach der Behandlung einen Tumor regenerieren. Die Autor:innen identifizierten zuvor eine besonders gefährliche Untergruppe, die migrierenden Krebsstammzellen, die zwei Oberflächenmarker (CD133 und CXCR4) tragen und stark mit Metastasen assoziiert sind. In patientenabgeleiteten Zellmodellen bestätigen sie jetzt, dass beide Marker in Pankreastumoren im Vergleich zu normalem Gewebe überproduziert werden und dass höhere Anteile dieser Zellen mit aggressiverer Erkrankung korrelieren.
Wie die Nachbarzellen des Tumors das Feuer anfachen
Pankreaskarzinome wachsen in einem dichten, narbenähnlichen Gewebe, das mit Stütz- und Hilfszellen gefüllt ist, den pankreatischen Sternzellen. Diese Sternzellen sind keineswegs passives Gerüst, sondern coachen die benachbarten Krebszellen aktiv. Das Team rekonstruierte diese Interaktion im Labor, indem es patientenabgeleitete Tumorzellen mit Sternzellen ko-kultivierte oder sie dem konditionierten Medium der Sternzellen aussetzte. Sie fanden heraus, dass Sternzellen ein Signalmolekül namens CXCL12 freisetzen, das an den CXCR4‑Rezeptor auf Krebsstammzellen bindet. Dieser Austausch verstärkt stammesähnliche Eigenschaften, fördert die Umwandlung von einer kompakten, epithelialen Gestalt zu einer mobileren, mesenchymalen Form und erhöht ihre Fähigkeit, Sphären zu bilden und zu migrieren – Merkmale, die mit Metastasierung und Therapieresistenz verbunden sind.
Ein wichtiger molekularer Schalter in den Krebs‑Samen
Tiefer gehend in das Signalisierungsnetzwerk downstream von CXCR4 identifizierten die Forschenden ein Protein namens BMI1 als zentrales Steuerungszentrum. BMI1 ist bekannt dafür, normalen Stammzellen bei der Erhaltung ihrer Selbst‑Erneuerung zu helfen. Hier verloren metastatische Pankreaskrebszellen, bei denen die Wissenschaftler:innen genetische Werkzeuge einsetzten, um entweder CXCR4 oder BMI1 zu reduzieren, viele ihrer stammesähnlichen und migrativen Eigenschaften. Sie bildeten weniger Sphären, bewegten sich weniger in Richtung CXCL12 und zeigten eine Rückkehr zu einem geordneteren, epithelialen Zustand. Auf molekularer Ebene dämpfte die Blockade dieses Pfads pro‑überlebens‑ und Stress‑Antwort‑Schaltkreise und verringerte die Aktivierung von Wegen, die normalerweise Invasion und Therapie‑Resistenz antreiben.
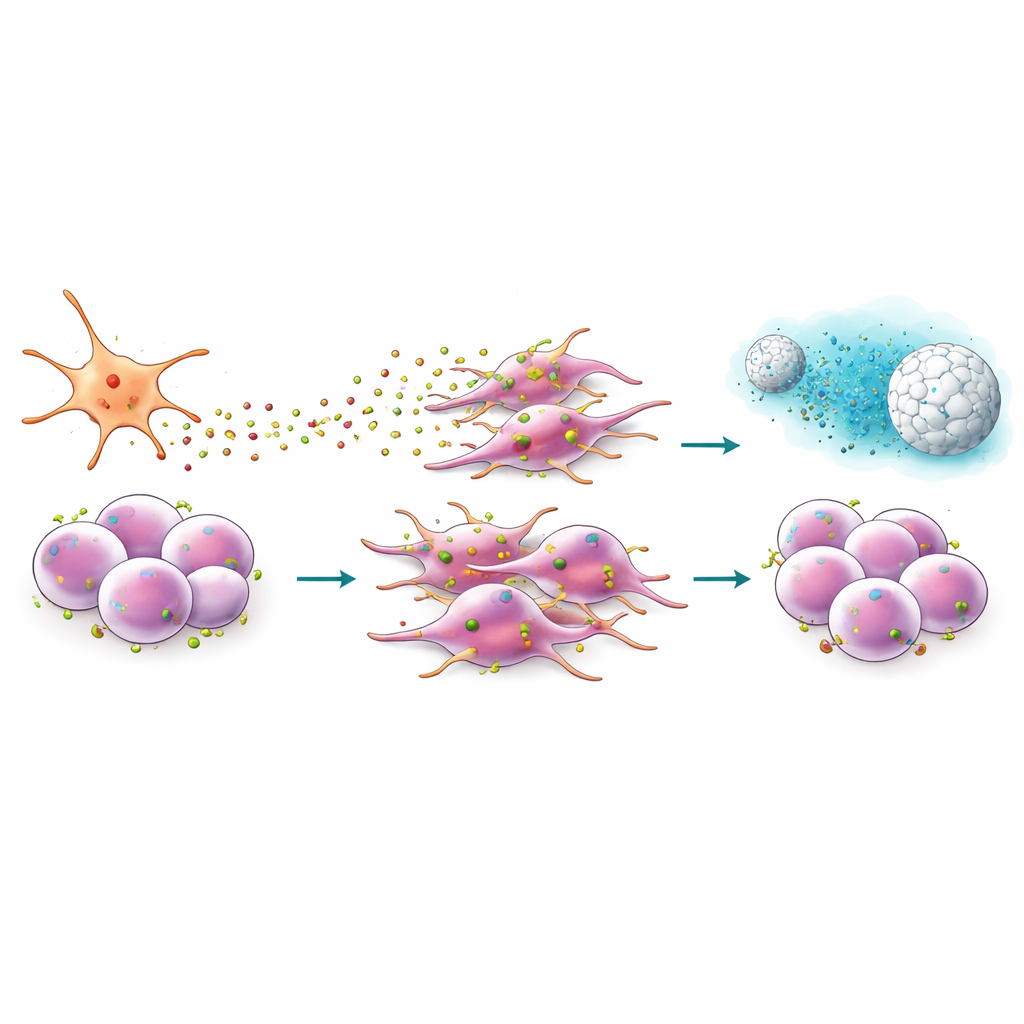
Entwurf eines Peptids und eines Nanopartikels, um das Signal zu durchtrennen
Da CXCR4 an der Zelloberfläche sitzt, bietet es eine attraktive Andockstelle für Medikamente. Das Team untersuchte EPI‑X4, ein natürlich vorkommendes menschliches Peptid, das CXCR4 blockiert, und eine gentechnisch veränderte, wirksamere Version namens JM#21. In Migrationsversuchen reduzierten diese Peptide stark die Fähigkeit der Krebszellen, sich in Richtung CXCL12 zu bewegen, und milderten Formänderungen, die mit Invasion einhergehen. Sie senkten zudem die Aktivität von Genen, die mit Stammhaftigkeit, epithelial‑zu‑mesenchymalem Übergang und einem oft von Tumoren gekaperten Entwicklungsprogramm (Hedgehog‑Signalgebung) verknüpft sind. In Kombination mit Standardchemotherapeutika wie Gemcitabin oder Paclitaxel machten JM#21 zuvor resistente Zellen deutlich verwundbarer und verkleinerten den Anteil überlebender Krebsstammzellen nach der Behandlung.
Schmuggeln fragiler Wirkstoffe mit Silika‑Nanopartikeln
Ein Hindernis für den Einsatz von Peptiden als Medikamente ist, dass sie im Blut und in konventionellen Kulturmedien schnell abgebaut werden. Um dem entgegenzuwirken, luden die Forschenden JM#21 in winzige, poröse Silika‑Kugeln – mesoporöse Silika‑Nanopartikel –, die wie schützende Schwämme wirken, das Peptid langsam freisetzen und es vor Abbau abschirmen. Unter serumhaltigen Bedingungen, die freies JM#21 normalerweise inaktivieren, blieb die nanopartikelgebundene Form funktionsfähig: Sie blockierte weiterhin CXCL12‑getriebene Migration und reduzierte den Anteil gefährlicher migrierender Krebsstammzellen in Ko‑Kulturen von Tumor‑ und Sternzellen. Genexpressionsanalysen zeigten, dass nanopartikelvermitteltes JM#21 auch Markern der Therapieresistenz, antioxidativen Abwehrmechanismen und BMI1 selbst entgegenwirkte und die Zellen in einen weniger aggressiven Zustand zurückführte.
Was das für Patient:innen bedeuten könnte
Für Laien lautet die Botschaft dieser Arbeit, dass die gefährlichsten Zellen des Pankreaskrebses auf ein Gespräch mit ihrer Umgebung und auf einen spezifischen molekularen Schalter angewiesen sind, um mobil, stammesähnlich und therapieresistent zu bleiben. Indem man die CXCL12–CXCR4–BMI1‑Achse mit einem maßgeschneiderten Peptid unterbricht und dieses Peptid in Silika‑Nanopartikeln verpackt, um es stabil zu halten, zeigen die Forschenden, dass es möglich ist, diese metastatischen Samen zu schwächen und die Chemotherapie in Labor‑Modellen wirksamer zu machen. Während weitere Tier‑ und klinische Studien nötig sind, bietet dieser Ansatz eine vielversprechende Blaupause für Therapien, die nicht nur Tumoren verkleinern, sondern auch die ursächlichen Zellen angreifen, die Ausbreitung und Rückfälle antreiben.
Zitation: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Schlüsselwörter: Pankreaskrebs, Krebsstammzellen, Tumormikroumgebung, CXCR4-Inhibitoren, Nanopartikel-Arzneimittelabgabe