Clear Sky Science · pl
Peptyd celujący w CXCR4 podany za pomocą nanocząstek krzemionkowych eliminuje migrujące komórki macierzyste raka w gruczolakoraku przewodowym trzustki
Dlaczego to badanie ma znaczenie
Rak trzustki jest jednym z najgroźniejszych nowotworów, ponieważ wcześnie się rozsiewa i opiera niemal każdemu zastosowanemu leczeniu. Głównym sprawcą są niewielkie, mobilne „nasiona” guza — komórki, które przemieszczają się po organizmie i odtwarzają nowotwór w innych miejscach. W niniejszym badaniu zbadano, jak te wędrujące komórki są wspierane przez ich otoczenie, i przedstawiono nową, wysoko ukierunkowaną eksperymentalną terapię — dostarczaną za pomocą maleńkich nanocząstek krzemionkowych — której celem jest odnalezienie i unieszkodliwienie tych komórek, zanim wyrządzą dalsze szkody.
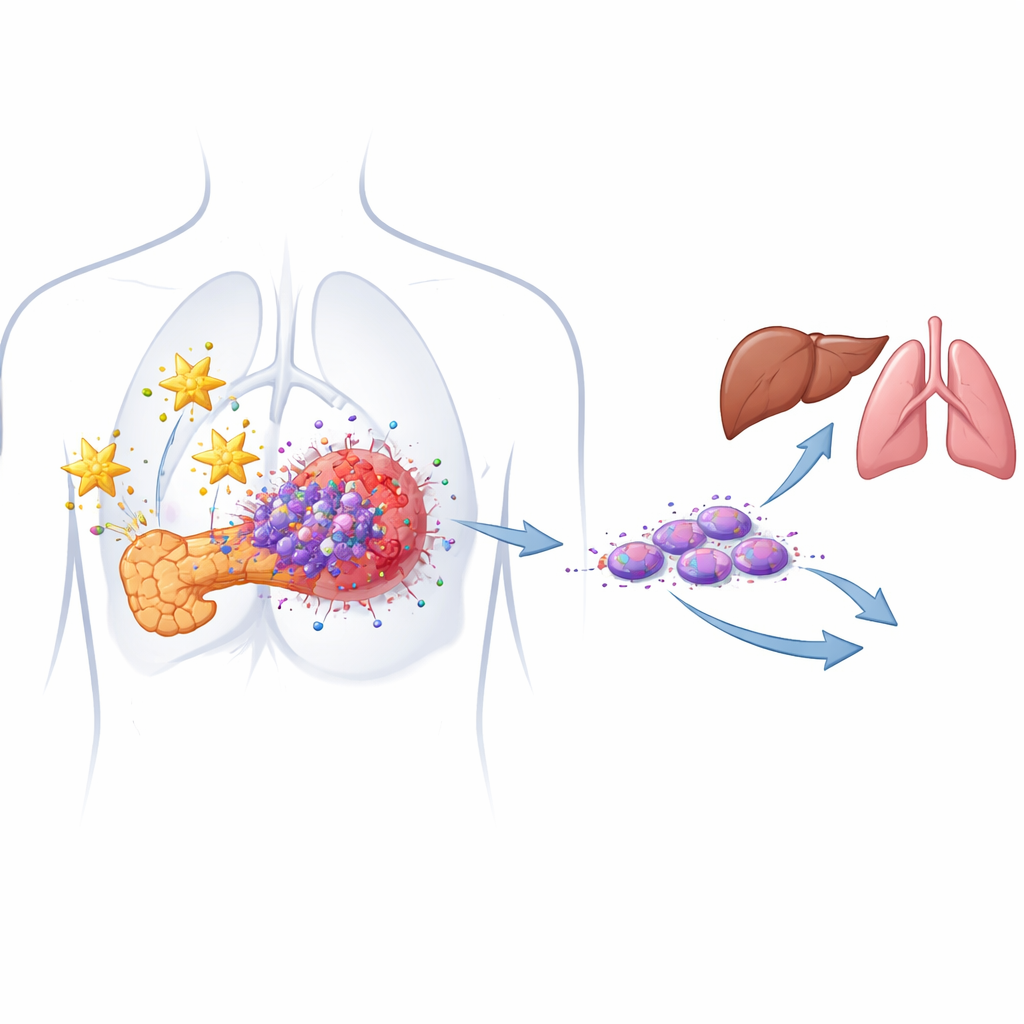
Ukryte nasiona nowotworu, które napędzają nawrót
Większość guzów trzustki składa się z komórek nowotworowych o zwykłym wyglądzie, lecz w ich wnętrzu znajduje się mniejszość tzw. komórek macierzystych nowotworu. Komórki te potrafią samoodnawiać się, przetrwać chemioterapię i zregenerować guz po leczeniu. Autorzy wcześniej zidentyfikowali szczególnie niebezpieczny podtyp — migrujące komórki macierzyste nowotworu, które wykazują dwa markery powierzchniowe (CD133 i CXCR4) i są silnie powiązane z przerzutami. W modelach komórek pochodzących od pacjentów potwierdzili teraz, że oba markery są nadmiernie eksprymowane w guzach trzustki w porównaniu z tkanką zdrową i że wyższe poziomy tych komórek korelują z bardziej agresywnym przebiegiem choroby.
Jak sąsiedzi guza podsycają rozwój
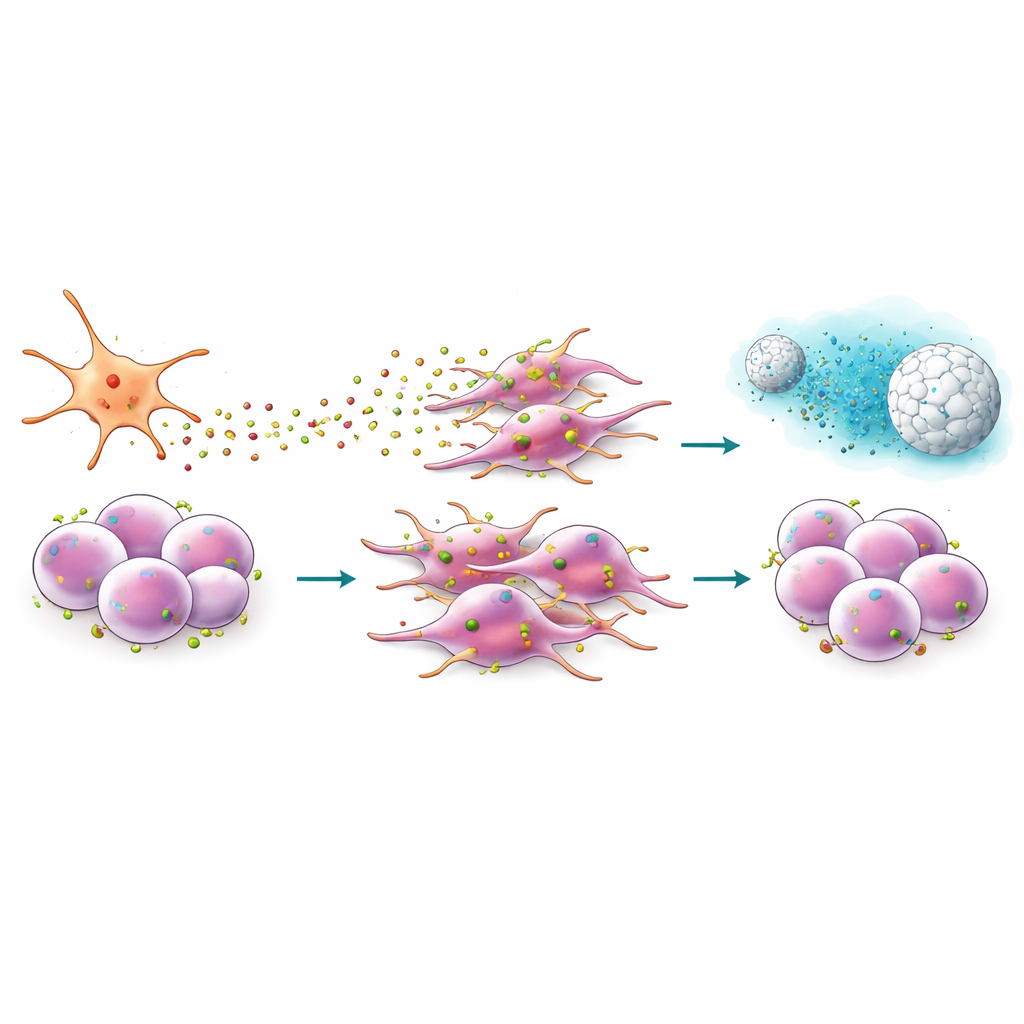
Raki trzustki rozwijają się w gęstej, przypominającej bliznę tkance, wypełnionej komórkami wspierającymi zwanymi komórkami gwiaździstymi trzustki. Zamiast być biernym rusztowaniem, komórki te aktywnie „trenują” pobliskie komórki nowotworowe. Zespół odtworzył tę interakcję w laboratorium, ko‑hodując komórki guza pochodzące od pacjentów z komórkami gwiaździstymi lub eksponując je na medium warunkowane przez komórki gwiaździste. Stwierdzono, że komórki gwiaździste wydzielają cząsteczkę sygnałową o nazwie CXCL12, która wiąże się z receptorem CXCR4 na komórkach macierzystych nowotworu. Ta komunikacja wzmacnia cechy zbliżone do komórek macierzystych, sprzyja przejściu komórek z zwartego, nabłonkowego kształtu do bardziej ruchomej, mezenchymalnej formy oraz zwiększa ich zdolność do tworzenia sfer i migracji — cechy związane z przerzutami i opornością na leki.
Kluczowy molekularny przełącznik wewnątrz nasion nowotworu
Pogłębiając analizę sieci sygnałowej po CXCR4, badacze wskazali białko o nazwie BMI1 jako centralny węzeł kontrolny. BMI1 jest znane z roli w utrzymaniu samoodnawiania normalnych komórek macierzystych. Tutaj, gdy naukowcy zastosowali narzędzia genetyczne do obniżenia ekspresji CXCR4 lub BMI1 w przerzutowych komórkach raka trzustki, komórki te straciły wiele cech związanych z „stemness” i migracją. Tworzyły mniej sfer, słabiej migrowały w kierunku CXCL12 i wykazywały przesunięcie z powrotem w kierunku bardziej uporządkowanego, nabłonkowego stanu. Na poziomie molekularnym zablokowanie tej ścieżki osłabiało obwody pro‑przeżyciowe i odpowiedzi na stres oraz zmniejszało aktywację szlaków zwykle napędzających inwazję i oporność na terapie.
Projektowanie peptydu i nanocząstki do przerwania sygnału
Ponieważ CXCR4 znajduje się na powierzchni komórki, stanowi atrakcyjne miejsce docelowe dla leków. Zespół badał EPI‑X4, naturalnie występujący peptyd ludzki blokujący CXCR4, oraz jego zmodyfikowaną, silniejszą wersję nazwaną JM#21. W eksperymentach migracyjnych te peptydy wyraźnie zmniejszały zdolność komórek nowotworowych do przemieszczania się w kierunku CXCL12 i łagodziły zmiany kształtu komórek związane z inwazją. Obniżały też aktywność genów powiązanych z cechami komórek macierzystych, przejściem nabłonkowo‑mezenchymalnym i programem rozwojowym (szlak Hedgehog), często przejmowanym przez guzy. W połączeniu ze standardowymi chemioterapiami, takimi jak gemcytabina czy paklitaksel, JM#21 uczynił wcześniej oporne komórki znacznie bardziej podatnymi, zmniejszając pulę przeżywających komórek macierzystych po leczeniu.
Przemyt delikatnych leków za pomocą nanocząstek krzemionkowych
Jednym z problemów stosowania peptydów jako leków jest ich szybkie rozkładanie we krwi i w konwencjonalnych mediach hodowlanych. Aby temu zaradzić, badacze załadowali JM#21 do drobnych, porowatych kulek krzemionkowych — mezoporowatych nanocząstek krzemionkowych — które działają jak ochronne gąbki, powoli uwalniając peptyd i chroniąc go przed degradacją. W warunkach zawierających surowicę, które normalnie inaktywują wolny JM#21, forma związana z nanocząstkami pozostała funkcjonalna: nadal blokowała migrację napędzaną przez CXCL12 i zmniejszała odsetek niebezpiecznych migrujących komórek macierzystych nowotworu w ko‑hodowlach komórek guza i komórek gwiaździstych. Analizy na poziomie genowym wykazały, że JM#21 dostarczony za pomocą nanocząstek również osłabiał markery oporności na leki, systemy obronne przeciwutleniaczy oraz samą ekspresję BMI1, jednocześnie skłaniając komórki ku mniej agresywnemu fenotypowi.
Co to może oznaczać dla pacjentów
Dla laika przesłanie tej pracy jest takie, że najbardziej niebezpieczne komórki raka trzustki polegają na rozmowie z otoczeniem i na określonym molekularnym przełączniku, aby zachować mobilność, cechy komórek macierzystych i oporność na leki. Przerywając oś CXCL12–CXCR4–BMI1 za pomocą dopasowanego peptydu i pakując ten peptyd w nanocząstki krzemionkowe w celu zapewnienia stabilności, badacze pokazują, że można osłabić te przerzutowe nasiona i zwiększyć skuteczność chemioterapii w modelach laboratoryjnych. Choć potrzebne są dalsze badania na zwierzętach i kliniczne, podejście to stanowi obiecujący schemat terapii, które nie tylko zmniejszają rozmiar guzów, lecz także celują w komórki źródłowe napędzające rozsiew i nawrót.
Cytowanie: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Słowa kluczowe: rak trzustki, komórki macierzyste nowotworu, mikrośrodowisko guza, inhibitory CXCR4, dostarczanie leków za pomocą nanocząstek