Clear Sky Science · it
Un peptide che prende di mira CXCR4 veicolato da nanoparticelle di silice elimina le cellule staminali tumorali migranti nell’adenocarcinoma duttale pancreatico
Perché questa ricerca è importante
Il cancro pancreatico è uno dei tumori più letali perché si diffonde precocemente e resiste praticamente a ogni trattamento disponibile. Un colpevole principale è una piccola popolazione mobile di cellule “seme” tumorali che viaggiano attraverso il corpo e rilanciano il tumore altrove. Questo studio esplora come questi semi erranti siano nutriti dal loro microambiente e presenta una nuova terapia sperimentale altamente mirata — veicolata da minuscole nanoparticelle di silice — che punta a rintracciarli e disarmarli prima che provochino ulteriori danni.
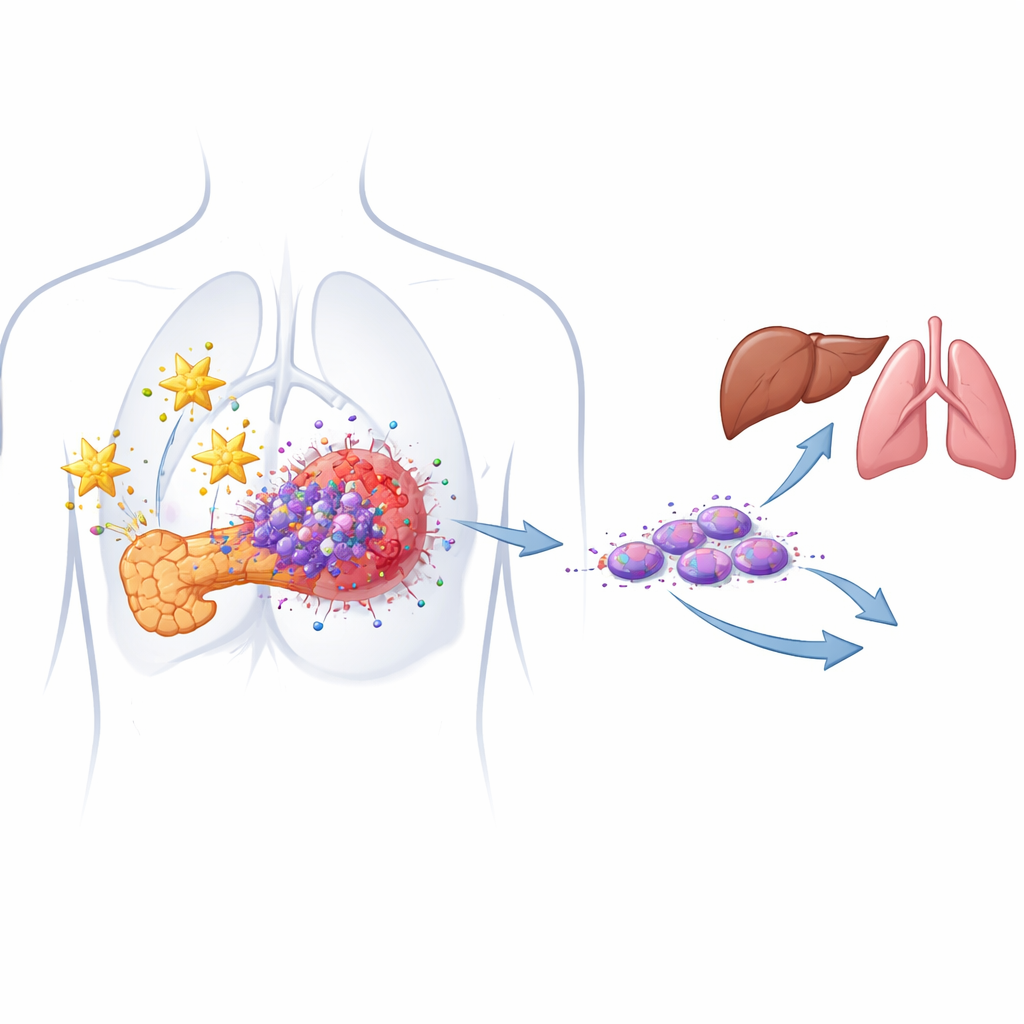
I semi tumorali nascosti che guidano le recidive
La maggior parte dei tumori pancreatici è composta da cellule cancerose dall’aspetto ordinario, ma al loro interno si trova una popolazione minoritaria di cosiddette cellule staminali tumorali. Queste cellule possono autorinnovarsi, sopravvivere alla chemioterapia e rigenerare un tumore dopo il trattamento. Gli autori avevano in precedenza identificato un sottogruppo particolarmente pericoloso chiamato cellule staminali tumorali migranti, che esprimono due marcatori di superficie (CD133 e CXCR4) ed sono fortemente correlate con la metastasi. In modelli cellulari derivati da pazienti, confermano ora che entrambi i marcatori sono sovraespressi nei tumori pancreatici rispetto al tessuto normale e che livelli più elevati di queste cellule correlano con una malattia più aggressiva.
Come i vicini del tumore alimentano il problema
I tumori pancreatici crescono in un tessuto denso, simile a una cicatrice, ricco di cellule di supporto chiamate cellule stellate pancreatiche. Lungi dall’essere un semplice impalcatura, queste cellule stellate «istruiscono» attivamente le cellule tumorali adiacenti. Il gruppo ha ricreato questa interazione in laboratorio co‑coltivando cellule tumorali derivate da pazienti con cellule stellate oppure esponendole a mezzi condizionati dalle stellate. Hanno scoperto che le cellule stellate rilasciano una molecola di segnalazione chiamata CXCL12, che si lega al recettore CXCR4 sulle cellule staminali tumorali. Questo dialogo potenzia i tratti stem‑like, favorisce il passaggio da una forma compatta ed epiteliale a una più mobile e mesenchimale, e rende le cellule più abili a formare sfere e a migrare — caratteristiche associate a metastasi e resistenza ai farmaci.
Un interruttore molecolare chiave nelle cellule staminali tumorali
Approfondendo la rete di segnalazione a valle di CXCR4, i ricercatori hanno individuato una proteina chiamata BMI1 come nodo di controllo centrale. Si sa che BMI1 aiuta le cellule staminali normali a mantenere il loro autorinnovamento. Qui, quando gli scienziati hanno usato strumenti genetici per ridurre l’espressione di CXCR4 o di BMI1 in cellule metastatiche del pancreas, le cellule hanno perso molte delle caratteristiche staminali e migratorie. Hanno formato meno sfere, migrato meno verso CXCL12 e mostrato un ritorno a uno stato più ordinato ed epiteliale. A livello molecolare, il blocco di questa via ha attenuato circuiti pro‑sopravvivenza e di risposta allo stress e ha ridotto l’attivazione di vie che normalmente alimentano invasione e resistenza alle terapie.
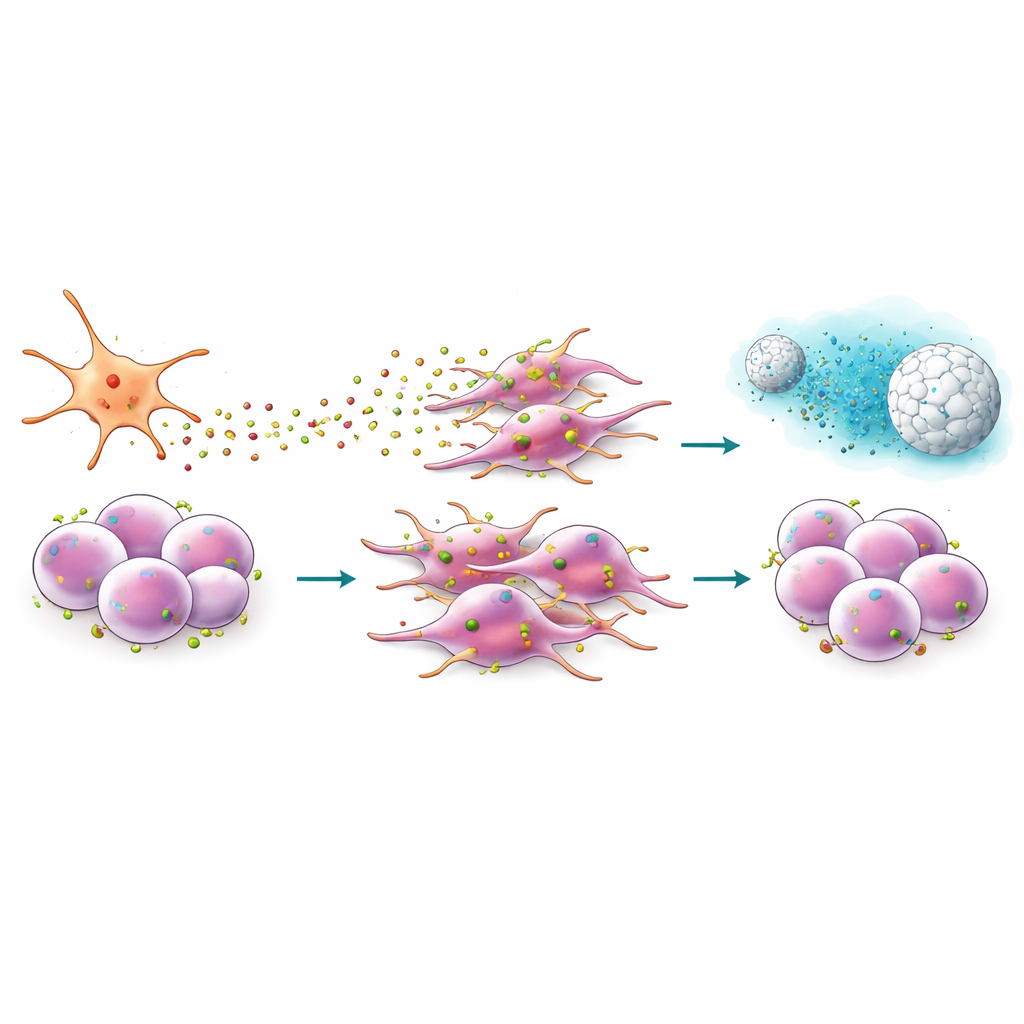
Progettare un peptide e una nanoparticella per interrompere il segnale
Poiché CXCR4 è esposto sulla superficie cellulare, rappresenta un sito di ancoraggio attraente per i farmaci. Il gruppo ha studiato EPI‑X4, un peptide umano naturale che blocca CXCR4, e una versione ingegnerizzata e più potente chiamata JM#21. Nei test di migrazione, questi peptidi hanno ridotto nettamente la capacità delle cellule tumorali di muoversi verso CXCL12 e hanno attenuato i cambiamenti morfologici associati all’invasione. Hanno inoltre abbassato l’attività di geni legati alla stemness, alla transizione epitelio‑mesenchimale e a un programma di sviluppo (via Hedgehog) spesso dirottato dai tumori. In combinazione con chemioterapie standard come gemcitabina o paclitaxel, JM#21 ha reso cellule precedentemente resistenti molto più vulnerabili, riducendo il pool di cellule staminali tumorali sopravvissute dopo il trattamento.
Trasportare farmaci fragili con nanoparticelle di silice
Un ostacolo all’uso dei peptidi come farmaci è che vengono rapidamente degradati nel sangue e nei medi di coltura convenzionali. Per superare questo problema, i ricercatori hanno caricato JM#21 in minuscole sfere porose di silice — nanoparticelle di silice mesoporosa — che agiscono come spugne protettive, rilasciando lentamente il peptide e proteggendolo dalla degradazione. In condizioni con siero che normalmente inattivano JM#21 libero, la forma legata alla nanoparticella è rimasta funzionale: ha continuato a bloccare la migrazione indotta da CXCL12 e ha ridotto la frazione di pericolose cellule staminali tumorali migranti nelle co‑colture di tumore e cellule stellate. Analisi a livello genico hanno mostrato che JM#21 veicolato dalle nanoparticelle ha anche attenuato marcatori di resistenza ai farmaci, difese antiossidanti e lo stesso BMI1, spingendo le cellule verso uno stato meno aggressivo.
Cosa potrebbe significare per i pazienti
Per un non addetto ai lavori, il messaggio di questo lavoro è che le cellule più pericolose del cancro pancreatico dipendono da una conversazione con il loro microambiente e da un interruttore molecolare specifico per rimanere mobili, staminali e resistenti ai farmaci. Interrompendo l’asse CXCL12–CXCR4–BMI1 con un peptide su misura, e racchiudendo quel peptide in nanoparticelle di silice per mantenerlo stabile, i ricercatori dimostrano che è possibile indebolire questi semi metastatici e rendere la chemioterapia più efficace nei modelli di laboratorio. Pur richiedendo ulteriori studi su animali e sperimentazioni cliniche, questo approccio offre una promettente mappa di riferimento per terapie che non si limitano a ridurre i tumori, ma colpiscono anche le cellule radice che guidano la diffusione e le recidive.
Citazione: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Parole chiave: cancro del pancreas, cellule staminali tumorali, microambiente tumorale, inibitori di CXCR4, consegna di farmaci con nanoparticelle