Clear Sky Science · nl
Een CXCR4‑gerichte peptide afgeleverd door silica‑nanodeeltjes elimineert migrerende kankerstamcellen bij pancreatisch ductaal adenocarcinoom
Waarom dit onderzoek ertoe doet
Alvleesklierkanker is een van de dodelijkste vormen van kanker omdat ze vroeg uitzaait en vrijwel elke behandeling weet te weerstaan. Een belangrijke boosdoener is een kleine, mobiele groep tumor‑“zaad”cellen die door het lichaam reizen en de kanker elders opnieuw kunnen starten. Deze studie onderzoekt hoe deze zwervende zaadcellen door hun omgeving worden gevoed en introduceert een nieuwe, zeer gerichte experimentele therapie—afgeleverd door piepkleine silica‑nanodeeltjes—die erop gericht is deze cellen op te sporen en uit te schakelen voordat ze verdere schade kunnen aanrichten.
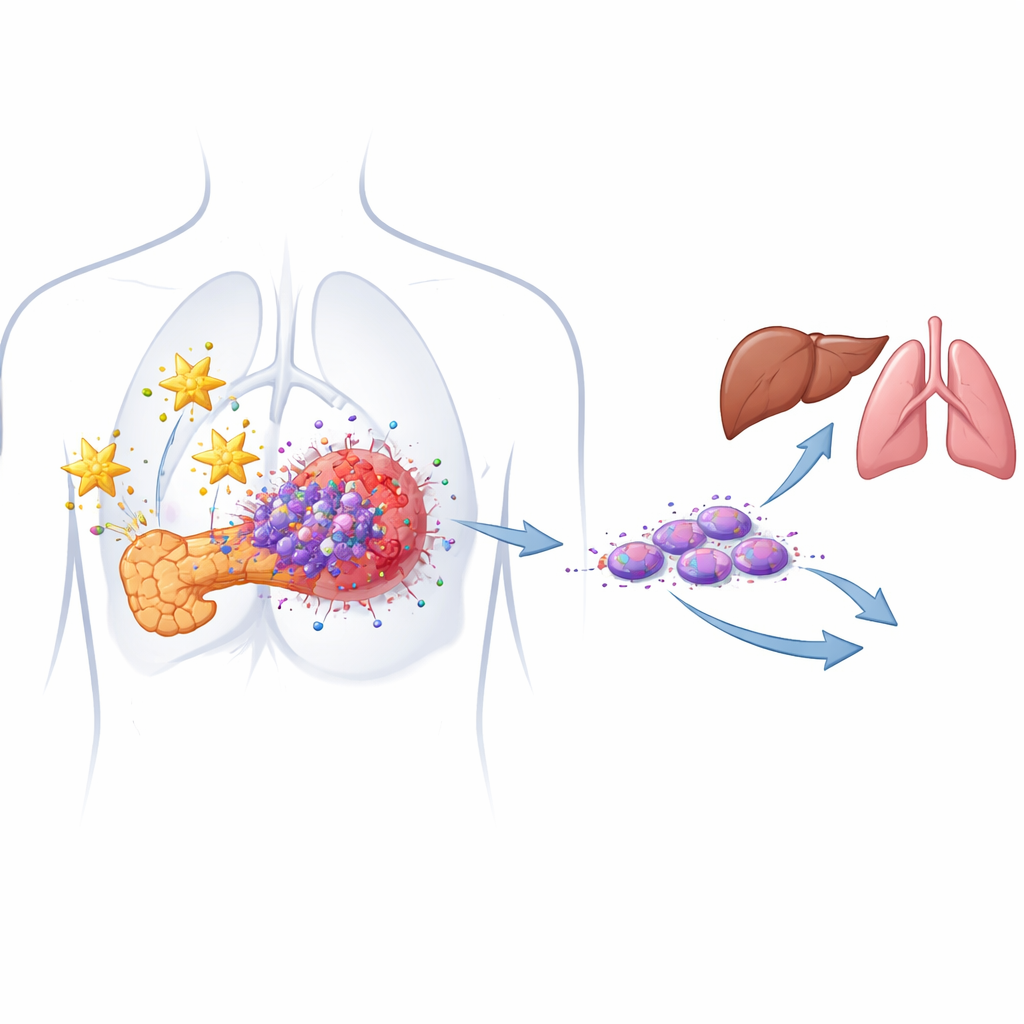
De verborgen kankerzaden die terugval aandrijven
De meeste alvleeskliertumoren bestaan uit gewone‑uitziende kankercellen, maar daarin verscholen bevindt zich een minderheid van zogeheten kankerstamcellen. Deze cellen kunnen zichzelf vernieuwen, chemotherapie overleven en na behandeling een tumor regenereren. De auteurs identificeerden eerder een bijzonder gevaarlijke subgroep, de migrerende kankerstamcellen, die twee oppervlaktemarkers (CD133 en CXCR4) dragen en sterk geassocieerd zijn met uitzaaiing. In patiëntafgeleide celmodellen bevestigen ze nu dat beide markers in alvleeskliertumoren meer worden geproduceerd vergeleken met normaal weefsel en dat hogere aantallen van deze cellen correleren met agressievere ziekte.
Hoe de buren van de tumor het vuur aanwakkeren
Alvleesklierkankers groeien in dicht, littekenachtig weefsel dat vol zit met steunende cellen, de pancreatische stercellen. Lang niet passief als een geraamte, coachen deze stercellen actief nabije kankercellen. Het team herbouwde deze interactie in het laboratorium door patiëntafgeleide tumorcellen samen te kweken met stercellen of ze bloot te stellen aan medium geconditioneerd door stercellen. Ze vonden dat stercellen een signaalmolecuul genaamd CXCL12 afgeven, dat bindt aan de CXCR4‑receptor op kankerstamcellen. Deze kruisgesprekken versterken stam‑achtige eigenschappen, moedigen cellen aan over te schakelen van een compacte, epitheliale vorm naar een mobielere mesenchymale vorm, en maken ze beter in staat bolletjes te vormen en te migreren—kenmerken die samenhangen met uitzaaiing en medicijnresistentie.
Een belangrijke moleculaire schakel binnen de kankerzaden
Dieper gravend in het signaalnetwerk stroomafwaarts van CXCR4, pinpointten de onderzoekers een eiwit genaamd BMI1 als een centraal regelpunt. BMI1 staat bekend om normale stamcellen te helpen hun zelfvernieuwingsvermogen te behouden. Hier, wanneer de wetenschappers genetische middelen gebruikten om ofwel CXCR4 of BMI1 in metastatische alvleesklierkankercellen te verminderen, verloren de cellen veel van hun stam‑achtige en migratoire eigenschappen. Ze vormden minder bolletjes, bewogen minder richting CXCL12 en keerden op cellulair niveau terug naar een meer geordende, epitheliale staat. Op moleculair niveau dempte het blokkeren van deze route pro‑overlevings‑ en stressresponscircuits en verminderde de activatie van paden die normaal invasie en therapie‑resistentie aanwakkeren.
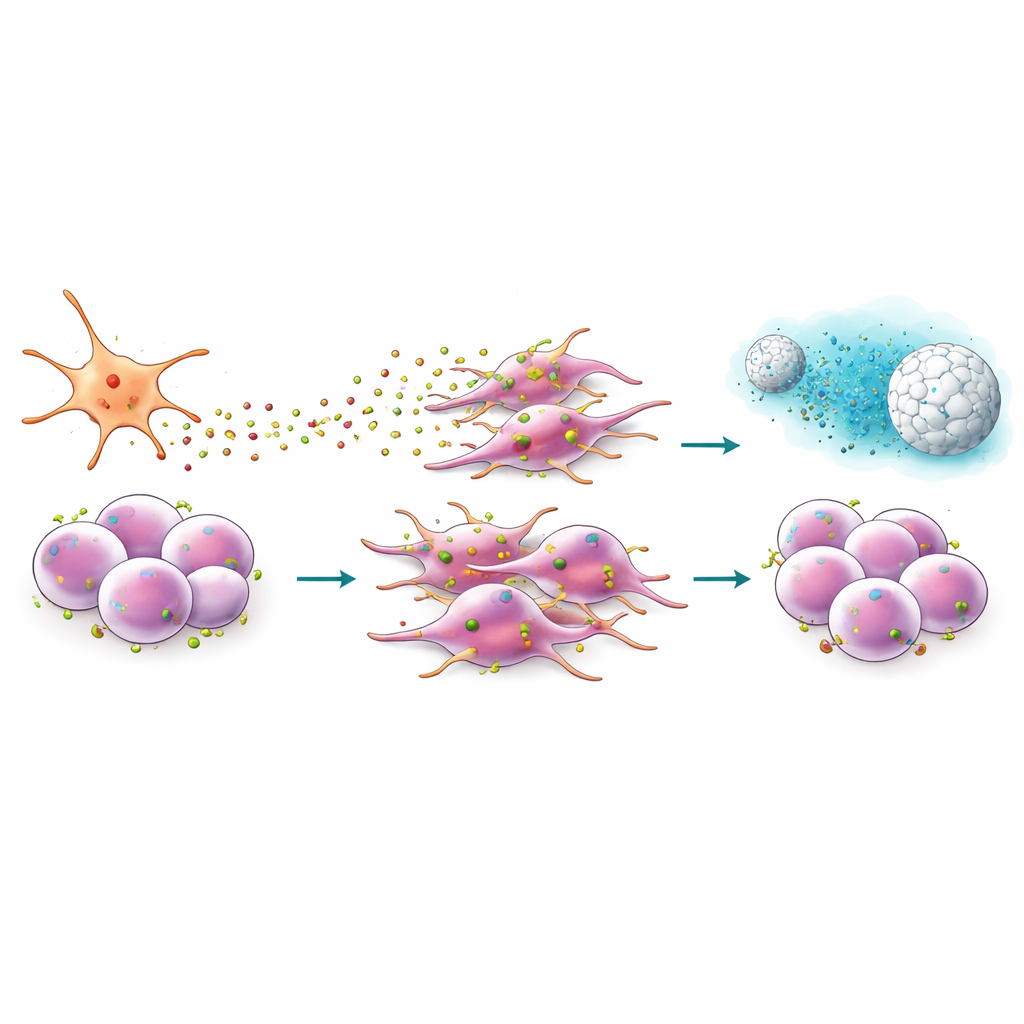
Ontwerp van een peptide en een nanodeeltje om het signaal te doorbreken
Omdat CXCR4 zich op het celoppervlak bevindt, biedt het een aantrekkelijk aanlegpunt voor geneesmiddelen. Het team onderzocht EPI‑X4, een van nature voorkomend humaan peptide dat CXCR4 blokkeert, en een ontworpen, krachtigere variant genaamd JM#21. In migratie‑experimenten verminderden deze peptiden sterk het vermogen van kankercellen om naar CXCL12 te bewegen en dempten ze veranderingen in celvorm die met invasie geassocieerd worden. Ze verlaagden ook de activiteit van genen die gelinkt zijn aan stam‑eigenschappen, epitheel‑naar‑mesenchymale transitie en een ontwikkelingsprogramma (Hedgehog‑signaleringspad) dat vaak door tumoren wordt gekaapt. In combinatie met standaardchemotherapieën zoals gemcitabine of paclitaxel maakte JM#21 eerder resistente cellen veel kwetsbaarder, waardoor de populatie overlevende kankerstamcellen na behandeling aanzienlijk kromp.
Vervoeren van fragiele middelen met silica‑nanodeeltjes
Een obstakel bij het gebruik van peptiden als geneesmiddelen is dat ze snel worden afgebroken in bloed en in conventioneel kweekmedium. Om dit te omzeilen laadden de onderzoekers JM#21 in piepkleine, poreuze silica‑bolletjes—mesoporeuze silica‑nanodeeltjes—die werken als beschermende sponzen en het peptide langzaam vrijgeven terwijl ze het tegen afbraak afschermen. Onder serumhoudende condities die normaal vrij JM#21 inactiveren, bleef de nanoparticlegebonden vorm functioneel: het blokkeerde nog steeds CXCL12‑gedreven migratie en verminderde het aandeel gevaarlijke migrerende kankerstamcellen in co‑kweken van tumor‑ en stercellen. Genexpressieanalyses toonden aan dat door nanodeeltjes afgeleverd JM#21 ook markers van medicijnresistentie, antioxidantverdedigingen en BMI1 zelf verminderde, terwijl het cellen terugduwde naar een minder agressieve staat.
Wat dit voor patiënten zou kunnen betekenen
Voor leken is de kernboodschap van dit werk dat de gevaarlijkste cellen van alvleesklierkanker afhankelijk zijn van een gesprek met hun omgeving en van een specifiek moleculair schakelpunt om mobiel, stam‑achtig en medicijnresistent te blijven. Door de CXCL12–CXCR4–BMI1‑as te onderbreken met een op maat gemaakt peptide, en dat peptide in silica‑nanodeeltjes te verpakken zodat het stabiel blijft, laten de onderzoekers zien dat het mogelijk is deze metastatische zaden te verzwakken en chemotherapie effectiever te maken in laboratoriummodellen. Hoewel verder onderzoek in diermodellen en klinische studies nodig is, biedt deze benadering een veelbelovend blauwdruk voor therapieën die niet alleen tumoren laten krimpen, maar ook de wortelcellen aanpakken die uitzaaiing en terugkeer aandrijven.
Bronvermelding: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Trefwoorden: alvleesklierkanker, kankerstamcellen, tumormicro‑omgeving, CXCR4‑remmers, nanodeeltje‑medicijnafgifte