Clear Sky Science · pt
Um peptídeo direcionado ao CXCR4 entregue por nanopartículas de sílica elimina células‑tronco cancerígenas migrantes no adenocarcinoma ductal pancreático
Por que esta pesquisa importa
O câncer de pâncreas é um dos mais letais porque se espalha cedo e resiste a quase todos os tratamentos disponíveis. Um grande culpado é um pequeno grupo móvel de células‑“sementes” do tumor que viajam pelo corpo e reiniciam o câncer em outros locais. Este estudo investiga como essas sementes errantes são nutridas pelo seu entorno e apresenta uma nova terapia experimental altamente direcionada — entregue por minúsculas nanopartículas de sílica — que pretende localizar e desarmar essas células antes que causem mais danos.
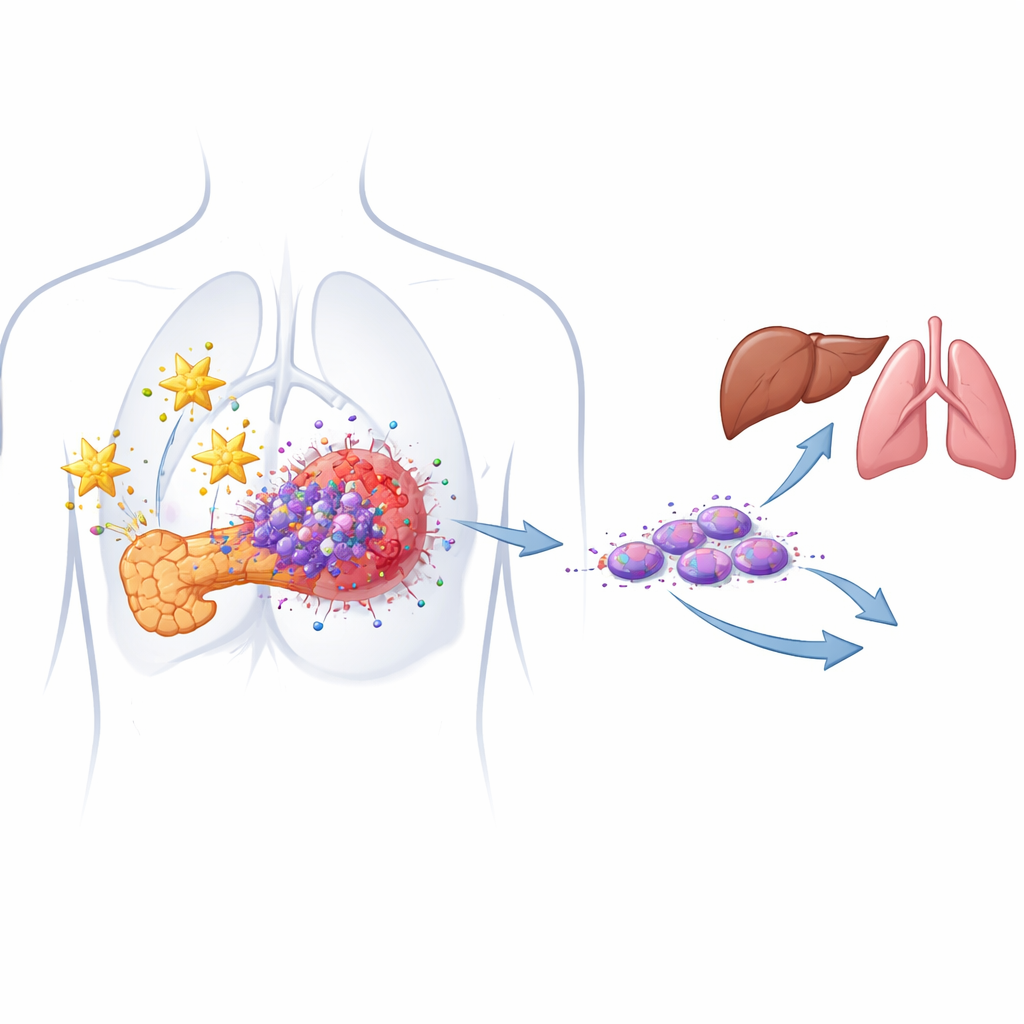
As sementes cancerígenas ocultas que impulsionam a recidiva
A maioria dos tumores pancreáticos é composta por células cancerígenas de aparência comum, mas abrigam uma população minoritária chamada células‑tronco cancerígenas. Essas células podem se autorrenovar, sobreviver à quimioterapia e regenerar um tumor após o tratamento. Os autores identificaram anteriormente um subconjunto especialmente perigoso chamado células‑tronco cancerígenas migrantes, que expressam dois marcadores de superfície (CD133 e CXCR4) e estão fortemente associados à metástase. Em modelos celulares derivados de pacientes, eles agora confirmam que ambos os marcadores são superexpressos em tumores pancreáticos em comparação com tecido normal e que níveis mais altos dessas células correlacionam com uma doença mais agressiva.
Como os vizinhos do tumor atiçam as chamas
Os cânceres de pâncreas crescem em um tecido denso, semelhante a uma cicatriz, repleto de células de suporte chamadas células estreladas pancreáticas. Longe de ser um arcabouço passivo, essas células estreladas atuam como “treinadoras” das células cancerígenas próximas. A equipe recriou essa interação no laboratório co‑cultivando células tumorais derivadas de pacientes com células estreladas ou expondo‑as a meio condicionado por células estreladas. Eles descobriram que as células estreladas liberam uma molécula sinalizadora chamada CXCL12, que se liga ao receptor CXCR4 nas células‑tronco cancerígenas. Essa comunicação aumenta traços de tipo‑tronco, estimula a mudança de uma forma compacta e epitelial para uma forma mais móvel e mesenquimal, e as torna mais capazes de formar esferas e migrar — características associadas à metástase e à resistência a medicamentos.
Um interruptor molecular chave dentro das sementes cancerígenas
Ao aprofundar a rede de sinalização a montante de CXCR4, os pesquisadores identificaram uma proteína chamada BMI1 como um nó central de controle. Sabe‑se que BMI1 ajuda células‑tronco normais a manterem sua autorrenovação. Aqui, quando os cientistas usaram ferramentas genéticas para reduzir tanto CXCR4 quanto BMI1 em células metastáticas de câncer pancreático, as células perderam muitas de suas características de tipo‑tronco e migratórias. Formaram menos esferas, migraram menos em direção ao CXCL12 e mostraram um retorno a um estado mais ordenado e epitelial. Ao nível molecular, o bloqueio dessa via reduziu circuitos pró‑sobrevivência e de resposta ao estresse e diminuiu a ativação de caminhos que normalmente alimentam a invasão e a resistência terapêutica.
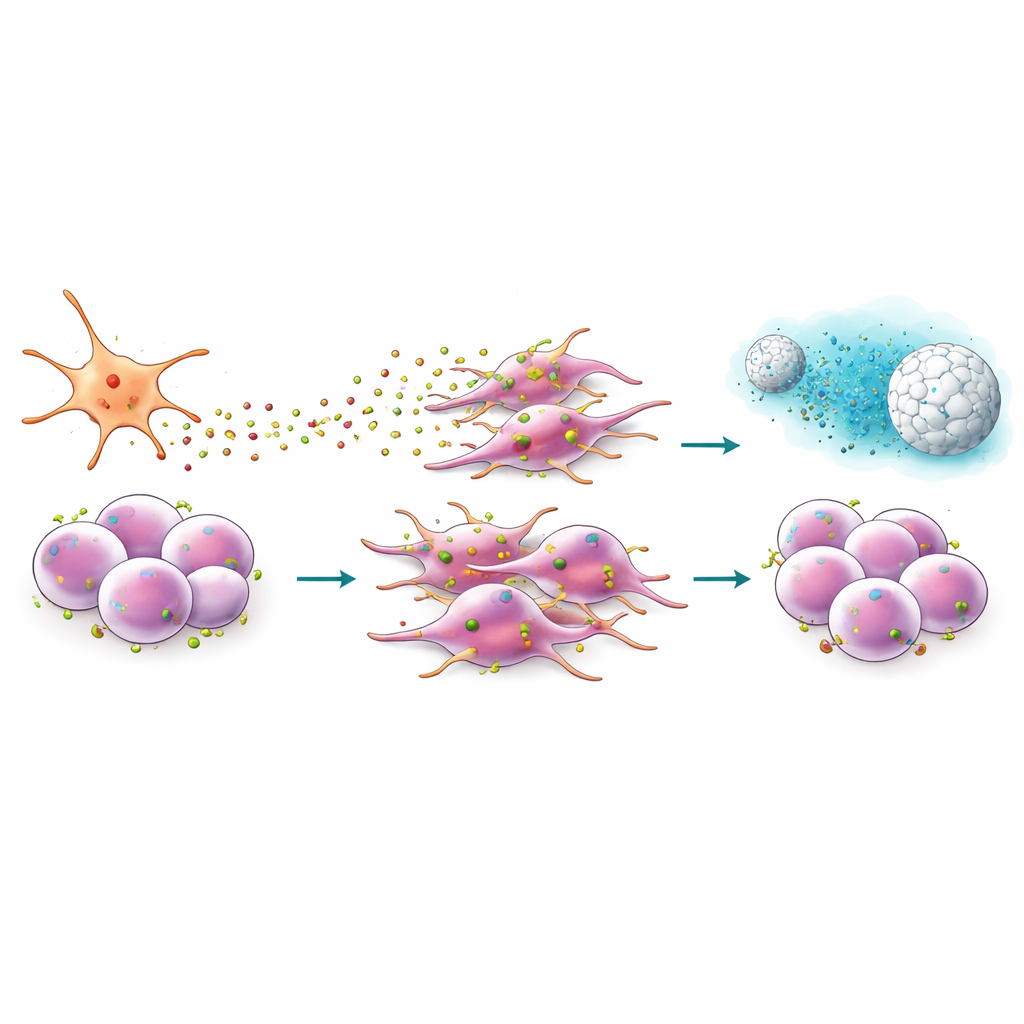
Projetando um peptídeo e uma nanopartícula para interromper o sinal
Como CXCR4 está na superfície celular, ele oferece um sítio de ancoragem atraente para fármacos. A equipe estudou EPI‑X4, um peptídeo humano natural que bloqueia CXCR4, e uma versão modificada e mais potente chamada JM#21. Em experimentos de migração, esses peptídeos reduziram acentuadamente a capacidade das células cancerígenas de se mover em direção ao CXCL12 e atenuaram as mudanças de forma celular associadas à invasão. Também diminuíram a atividade de genes ligados à pluripotência, à transição epitélio‑mesênquima e a um programa de desenvolvimento (sinalização Hedgehog) frequentemente capturado por tumores. Quando combinado com quimioterapias padrão, como gemcitabina ou paclitaxel, o JM#21 tornou células previamente resistentes muito mais vulneráveis, reduzindo o pool de células‑tronco cancerígenas sobreviventes após o tratamento.
Contrabandeando fármacos frágeis com nanopartículas de sílica
Um obstáculo ao uso de peptídeos como fármacos é que eles são rapidamente degradados no sangue e em meios de cultura convencionais. Para contornar isso, os pesquisadores carregaram JM#21 em minúsculas esferas porosas de sílica — nanopartículas de sílica mesoporosa — que funcionam como esponjas protetoras, liberando lentamente o peptídeo enquanto o protegem da degradação. Em condições com soro que normalmente inativam o JM#21 livre, a forma ligada à nanopartícula permaneceu funcional: ainda bloqueou a migração induzida por CXCL12 e reduziu a fração das perigosas células‑tronco cancerígenas migrantes em co‑culturas de tumor e células estreladas. Análises ao nível gênico mostraram que o JM#21 entregue por nanopartículas também reduziu marcadores de resistência a drogas, defesas antioxidantes e o próprio BMI1, ao mesmo tempo que guiou as células de volta a um estado menos agressivo.
O que isso pode significar para os pacientes
Para um leigo, a mensagem deste trabalho é que as células mais perigosas do câncer de pâncreas dependem de uma conversa com seu entorno e de um interruptor molecular específico para se manterem móveis, com características de tronco e resistentes a medicamentos. Ao interromper o eixo CXCL12–CXCR4–BMI1 com um peptídeo sob medida, e ao embalar esse peptídeo em nanopartículas de sílica para mantê‑lo estável, os pesquisadores mostram ser possível enfraquecer essas sementes metastáticas e tornar a quimioterapia mais eficaz em modelos laboratoriais. Embora sejam necessários estudos animais e clínicos adicionais, essa abordagem oferece um roteiro promissor para terapias que não apenas reduzem tumores, mas também atacam as células‑raízes que impulsionam a disseminação e a recidiva.
Citação: Tiwary, K., Lahusen, A., Inaas, S. et al. A CXCR4 targeting peptide delivered by silica nanoparticles eliminates migrating cancer stem cells in pancreatic ductal adenocarcinoma. Sci Rep 16, 12588 (2026). https://doi.org/10.1038/s41598-026-48584-2
Palavras-chave: câncer pancreático, células‑tronco cancerígenas, microambiente tumoral, inibidores de CXCR4, liberação de fármacos por nanopartículas