Clear Sky Science · zh
循环肿瘤细胞的综合电学建模以增强介电泳捕获与电穿孔效果
为何对血细胞施加微小电击很重要
在肿瘤可通过影像检测到之前很久,癌症就可能向血流中脱落少量流浪的细胞。循环肿瘤细胞为早期诊断和个性化治疗提供了重要线索,但它们极为稀少且难以在不伤及其他血细胞的情况下处理。本文探讨了如何在微型“实验室芯片”中通过精心设计的电场,温和地捕获这些游走的癌细胞,在其膜上短暂打开微小通道,然后让其恢复——同时尽量不损伤健康血细胞。
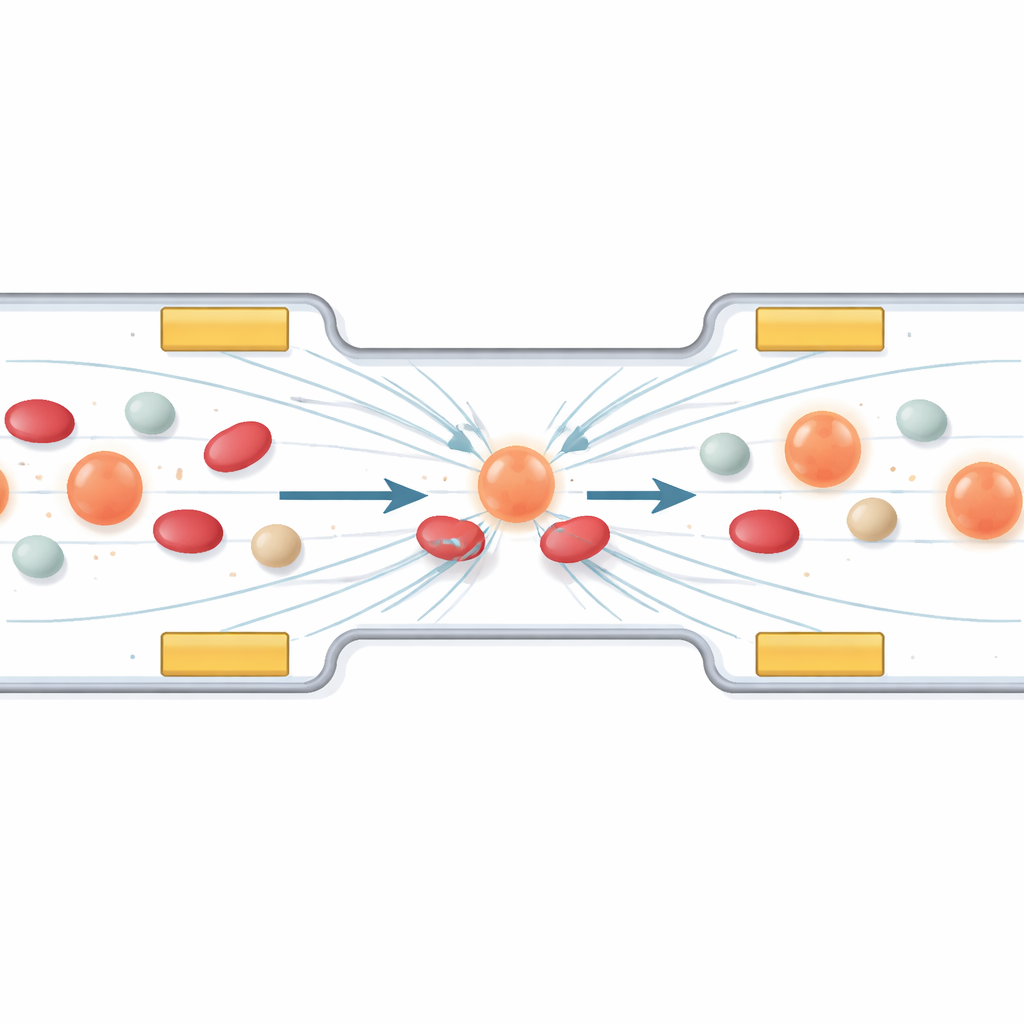
用看不见的力捕捉游走的癌细胞
工作第一部分研究如何利用称为介电泳的现象来操控并收集特定细胞。简单来说,当交变电场施加于微通道时,细胞会受到取决于其尺寸和电学特性的微小推拉力。作者设计了一组微电极,使循环肿瘤细胞在它们之间漂移到一个稳定的“停靠通道”,而更小或极化性较低的血液成分则通过。计算机模拟展示了改变电压和频率如何塑造电场,引导细胞远离高场区并将它们排列到用于处理的合适位置。电极表面的保护层可防止细胞与电极直接接触而受损。
在细胞膜上打开并关闭微观之门
当细胞被固定在位后,装置发出超短电脉冲,在外膜上短暂打出纳米级孔洞。该研究为血液中的三类关键细胞(循环肿瘤细胞、白细胞和血小板)建立了详细的数学模型,追踪每种细胞膜电压如何上升、何时首次出现孔洞、孔洞的大小与数量如何变化以及膜如何以及多快重新封闭。通过同时调整场强和脉冲时长,团队找到了使膜足够渗透以引入药物或遗传物质但随后愈合且不致死的“甜点”参数。对于肿瘤细胞和白细胞,有效场强在约1–4千伏/厘米,而体积小得多的血小板需要大约十倍的场强才能达到相同效果。
不同血细胞,不同的“甜点”参数
建模显示细胞尺寸和电学性质如何改变每种细胞的响应方式。较大的循环肿瘤细胞和白细胞充电较慢,在脉冲约两微秒时达到膜电压峰值;其孔洞在几十微秒到秒的时间尺度上生长然后关闭。相比之下,微小的血小板几乎即时响应,孔洞形成与封闭更快。在所有细胞类型中,最强的作用出现在面向入射场的“超极化”一侧,这里力的集中更大。这意味着通过为特定细胞大小选择合适的场强,可以优先在肿瘤细胞上打开孔洞,同时将对健康邻近细胞的损伤降到最低,为高度选择性的处理奠定基础。
在芯片上用真实细胞检验该想法
为检验模拟与现实是否一致,作者构建了一个将捕获电极与中央检测区结合的微流体芯片。他们将一种模型白细胞系(THP‑1细胞)注入通道,并在固定间隙上施加逐步增大的电压。他们没有直接观察孔洞,而是测量混悬液对交变电流的通导性。随着电场增大,细胞混合物的整体阻抗下降,其电容特性减弱,这些迹象表明膜变得更具导电性、不再像完整的绝缘体。在最高测试场强下,电学响应由通过开放孔洞的电导主导,与计算模型预测的趋势高度一致。
这对未来癌症护理意味着什么
简而言之,这项研究表明,一个紧凑的芯片既能从血液中分离稀有的癌细胞,又能以高度可控的方式温和打开其细胞膜。通过针对每类细胞调整脉冲强度和时序,该方法既可以保持细胞存活以供详细分析和药物测试,也可以将其推向不可逆损伤以实现靶向破坏,同时最小化加热并减少对健康细胞的伤害。对于普通读者,关键是:借助合适的“电学编排”,我们可以将微小电流变成早期癌症检测、精准药物递送以及可能更安全、更集中的癌症疗法的有力工具。
引用: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
关键词: 循环肿瘤细胞, 微流体电穿孔, 介电泳, 癌症诊断, 芯片实验室