Clear Sky Science · fr
Modélisation électrique intégrée des cellules tumorales circulantes pour un piégeage diélectrophorétique et une électroporation améliorés
Pourquoi de petites décharges électriques aux cellules sanguines comptent
Un cancer peut libérer quelques cellules dissidentes dans le sang bien avant qu’une tumeur n’apparaisse à l’imagerie. Ces cellules tumorales circulantes sont des indices précieux pour un diagnostic précoce et des traitements sur mesure, mais elles sont rares et difficiles à manipuler sans nuire au reste du sang. Cet article explore comment des champs électriques soigneusement façonnés à l’intérieur d’un petit dispositif lab‑on‑a‑chip peuvent capturer en douceur ces cellules cancéreuses errantes, ouvrir de minuscules portes temporaires dans leurs membranes, puis les laisser se régénérer — tout en épargnant largement les cellules sanguines saines.
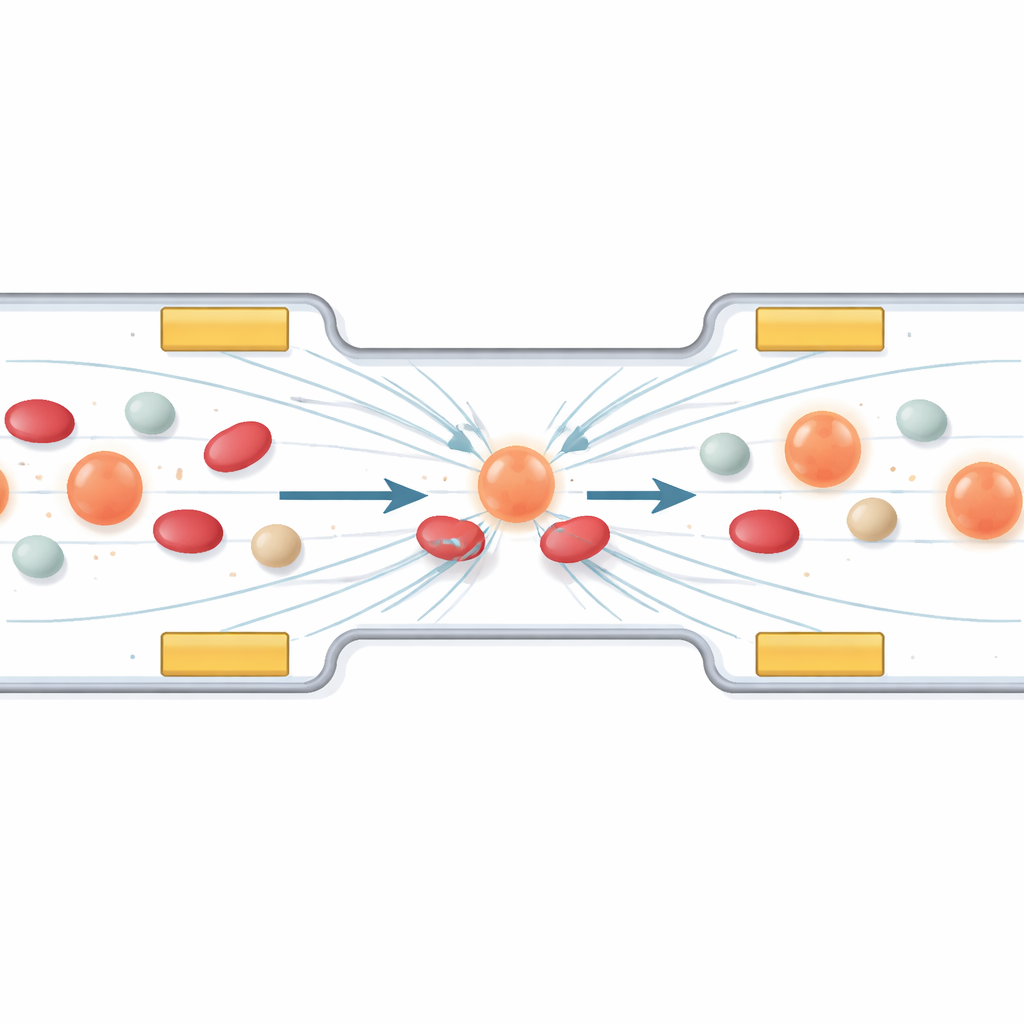
Utiliser des forces invisibles pour piéger les cellules cancéreuses errantes
La première partie du travail examine comment diriger et collecter des cellules spécifiques en utilisant un phénomène appelé diélectrophorèse. En termes simples, lorsqu’un champ électrique alternatif est appliqué à travers un microcanal, les cellules subissent de petites poussées qui dépendent de leur taille et de leur constitution électrique. Les auteurs conçoivent un agencement d’électrodes miniatures de sorte que les cellules tumorales circulantes dérivent vers une « voie de stationnement » stable entre elles, tandis que les composants sanguins plus petits ou moins polarisables passent. Des simulations informatiques montrent comment modifier la tension et la fréquence façonne le champ, guidant les cellules loin des zones de champ intense et les alignant dans la région adéquate pour le traitement. Une couche protectrice sur les électrodes empêche les cellules d’être endommagées par contact direct.
Ouvrir et fermer des portes microscopiques dans la peau des cellules
Une fois les cellules maintenues en place, le dispositif délivre des impulsions électriques ultracourtes qui percent brièvement des pores de l’ordre du nanomètre dans la membrane externe. L’étude construit un modèle mathématique détaillé de ce processus pour trois acteurs clés du sang : les cellules tumorales circulantes, les globules blancs et les plaquettes. Il suit comment la tension à travers chaque membrane cellulaire augmente, quand les pores apparaissent pour la première fois, quelle taille et quelle abondance ils atteignent, et la rapidité avec laquelle la membrane se referme. En réglant à la fois l’intensité du champ et la durée des impulsions, l’équipe identifie des plages optimales où la membrane devient suffisamment perméable pour faire entrer des médicaments ou du matériel génétique, puis se répare sans tuer la cellule. Pour les cellules tumorales et les globules blancs, les champs efficaces se situent entre 1 et 4 kilovolts par centimètre, tandis que les plaquettes, beaucoup plus petites, nécessitent environ dix fois plus de champ pour obtenir le même effet.
Différentes cellules sanguines, différents points optimaux
La modélisation révèle comment la taille des cellules et leurs propriétés électriques modulent la réponse de chaque type cellulaire. Les grandes cellules tumorales circulantes et les globules blancs se chargent plus lentement et atteignent une tension membranaire maximale autour de deux microsecondes après le début de l’impulsion ; leurs pores croissent puis se referment sur des échelles de temps allant de dizaines de microsecondes à plusieurs secondes. Les petites plaquettes, en revanche, réagissent presque instantanément, avec une formation et une fermeture de pores plus rapides. Pour tous les types cellulaires, l’action la plus intense se produit du côté « hyperpolarisé » de la cellule faisant face au champ arrivant, où les forces se concentrent. Cela signifie qu’en choisissant l’intensité de champ adaptée à une taille cellulaire donnée, il est possible de favoriser l’ouverture de pores dans les cellules tumorales tout en limitant les dommages aux voisines saines, posant les bases de traitements hautement sélectifs.
Tester l’idée avec de vraies cellules sur une puce
Pour vérifier si les simulations reflètent la réalité, les auteurs ont construit une puce microfluidique qui combine des électrodes de piégeage et une zone centrale de détection. Ils ont fait circuler une lignée de globules blancs modèles (cellules THP‑1) dans le canal et appliqué des tensions croissantes à travers un écart fixe. Plutôt que d’observer directement les pores, ils ont mesuré la facilité avec laquelle un courant alternatif traversait la suspension. À mesure que le champ électrique augmentait, la résistance globale du mélange cellulaire diminuait et son comportement capacitif s’atténuait, des signatures indiquant que les membranes étaient devenues plus conductrices et moins isolantes. Aux champs les plus élevés testés, la réponse électrique était dominée par la conduction à travers des pores ouverts, reflétant de près les tendances prédites par le modèle informatique.
Ce que cela pourrait signifier pour les soins du cancer à venir
En termes simples, cette étude montre qu’une puce compacte peut à la fois trier des cellules tumorales rares du sang et ouvrir leurs membranes de manière contrôlée et douce. En adaptant l’intensité et le timing des impulsions à chaque type cellulaire, l’approche peut soit préserver les cellules vivantes pour des analyses détaillées et des tests médicamenteux, soit les orienter vers des dommages irréversibles pour une destruction ciblée, tout en minimisant le chauffage et les effets indésirables sur les cellules saines. Pour un public non spécialiste, le message clé est qu’avec la bonne « chorégraphie électrique », de très faibles courants peuvent devenir des outils puissants pour la détection précoce du cancer, l’administration précise de médicaments et, potentiellement, des thérapies anticancéreuses plus sûres et plus ciblées.
Citation: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Mots-clés: cellules tumorales circulantes, électroporation microfluidique, diélectrophorèse, diagnostic du cancer, lab-on-a-chip