Clear Sky Science · es
Modelado eléctrico integrado de células tumorales circulantes para mejorar el atrapamiento dielectroforético y la electroporación
Por qué importan las pequeñas sacudidas eléctricas a las células sanguíneas
El cáncer puede desprender unas pocas células rebeldes en el torrente sanguíneo mucho antes de que un tumor sea detectable en una exploración. Estas células tumorales circulantes son pistas valiosas para el diagnóstico precoz y tratamientos personalizados, pero son escasas y difíciles de manejar sin dañar el resto de la sangre. Este trabajo explora cómo campos eléctricos cuidadosamente diseñados dentro de un pequeño dispositivo lab‑on‑a‑chip pueden atrapar suavemente estas células cancerosas errantes, abrir pequeñas puertas temporales en sus membranas y permitirles recuperarse —todo ello dejando en gran medida indemnes a las células sanguíneas sanas.
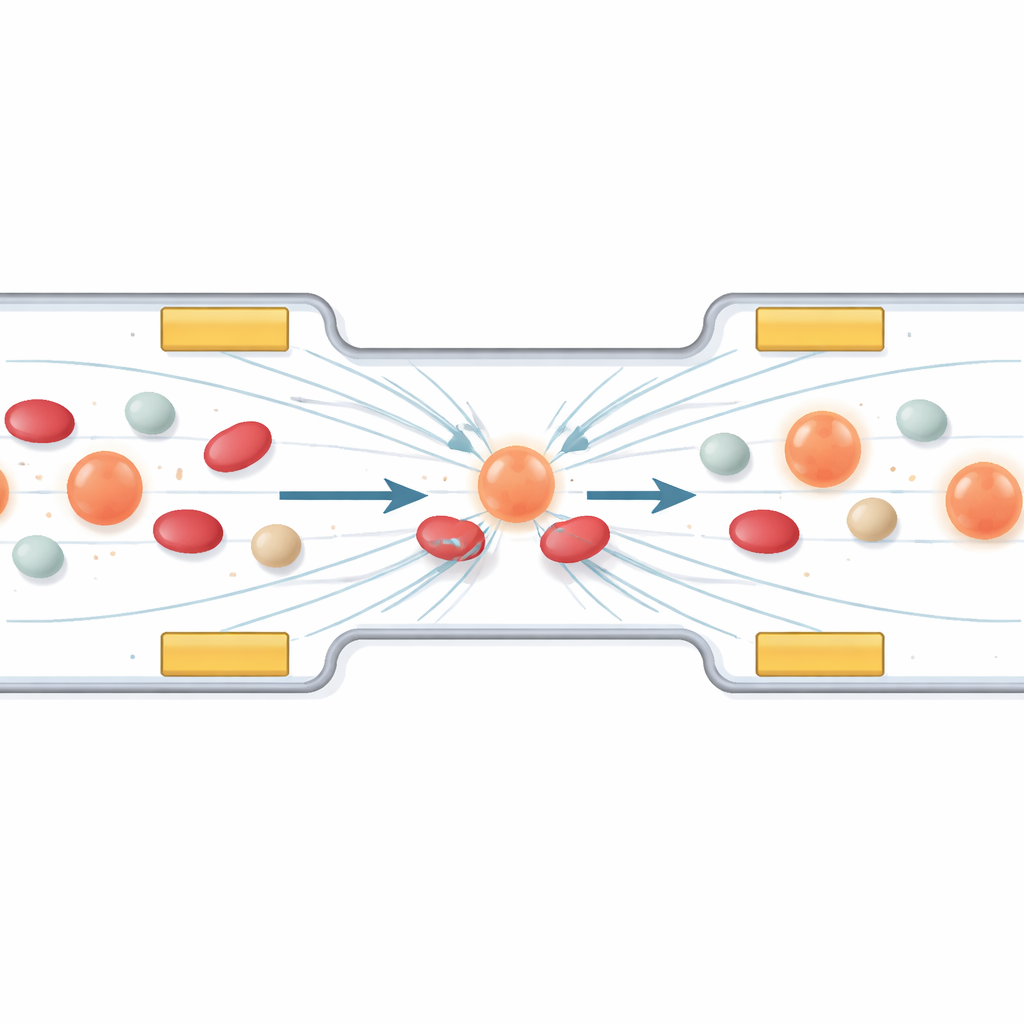
Usar fuerzas invisibles para capturar células cancerosas errantes
La primera parte del estudio analiza cómo guiar y colectar células específicas mediante un fenómeno llamado dielectroforesis. En términos sencillos, cuando se aplica un campo eléctrico alterno a través de un microcanal, las células experimentan pequeñas fuerzas de empuje y atracción que dependen de su tamaño y composición eléctrica. Los autores diseñan una disposición de electrodos en miniatura de modo que las células tumorales circulantes se desplacen hacia un “carril de estacionamiento” estable entre ellos, mientras que componentes sanguíneos más pequeños o menos polarizables pasan de largo. Las simulaciones por ordenador muestran cómo al cambiar el voltaje y la frecuencia se moldea el campo, guiando a las células fuera de zonas de campo intenso y alineándolas en la región adecuada para el tratamiento. Una capa protectora sobre los electrodos evita que las células sufran daño por contacto directo.
Abrir y cerrar puertas microscópicas en las membranas celulares
Una vez que las células quedan inmovilizadas, el dispositivo aplica pulsos eléctricos ultracortos que perforan temporalmente poros de escala nanométrica en la membrana externa. El estudio construye un modelo matemático detallado de este proceso para tres protagonistas clave en la sangre: células tumorales circulantes, leucocitos y plaquetas. Sigue cómo aumenta el voltaje a través de cada membrana celular, cuándo aparecen los poros por primera vez, cuánto y cuántos crecen, y con qué rapidez se reseca la membrana. Al ajustar tanto la intensidad del campo como la duración del pulso, el equipo identifica puntos óptimos donde la membrana se vuelve lo bastante permeable para admitir fármacos o material genético y luego se cura sin matar la célula. Para células tumorales y leucocitos, los campos efectivos están en el rango de 1–4 kilovoltios por centímetro, mientras que las mucho más pequeñas plaquetas necesitan campos aproximadamente diez veces más fuertes para alcanzar el mismo efecto.
Diferentes células sanguíneas, diferentes puntos óptimos
El modelado revela cómo el tamaño celular y las propiedades eléctricas modifican la respuesta de cada célula. Las células tumorales circulantes más grandes y los leucocitos se cargan más lentamente y alcanzan el voltaje máximo de membrana alrededor de los dos microsegundos del pulso; sus poros crecen y luego se cierran en escalas que van de decenas de microsegundos a segundos. Las diminutas plaquetas, en contraste, responden casi de inmediato, con una formación y resección de poros más rápidas. En todos los tipos celulares, la acción más intensa ocurre en el lado “hiperpolarizado” de la célula que mira hacia el campo entrante, donde las fuerzas se concentran. Esto significa que, al elegir la intensidad de campo adecuada para un tamaño celular dado, es posible favorecer la apertura de poros en células tumorales manteniendo bajo el daño a las células sanas vecinas, sentando las bases para tratamientos altamente selectivos.
Probar la idea con células reales en un chip
Para comprobar si las simulaciones coinciden con la realidad, los autores construyeron un chip microfluídico que combina electrodos de atrapamiento con una zona central de detección. Hicieron fluir una línea celular modelo de leucocitos (células THP‑1) por el canal y aplicaron voltajes crecientes a través de un hueco fijo. En lugar de observar los poros directamente, midieron cuán fácilmente pasaba una corriente alterna a través de la suspensión. A medida que el campo eléctrico aumentaba, la resistencia global de la mezcla celular disminuía y su comportamiento capacitivo se atenuaba, señales de que las membranas se habían vuelto más conductoras y menos como aislantes intactas. En los campos más altos probados, la respuesta eléctrica estuvo dominada por la conducción a través de poros abiertos, reflejando de cerca las tendencias predichas por el modelo por ordenador.
Qué podría significar esto para la atención oncológica futura
En pocas palabras, este estudio demuestra que un chip compacto puede tanto separar células cancerosas raras de la sangre como abrir sus membranas de forma controlada y delicada. Al adaptar la intensidad y el tiempo de los pulsos a cada tipo celular, el enfoque puede mantener las células vivas para análisis detallados y pruebas de fármacos, o bien llevarlas hacia un daño irreversible para su destrucción selectiva, todo ello minimizando el calentamiento y el daño a las células sanas. Para un público general, el mensaje clave es que con la “coreografía eléctrica” adecuada, podemos convertir corrientes minúsculas en herramientas poderosas para la detección temprana del cáncer, la entrega precisa de fármacos y, posiblemente, terapias oncológicas más seguras y focalizadas.
Cita: Sherif, S., Ghallab, Y.H. & Ismail, Y. Integrated electrical modeling of circulating tumor cells for enhanced dielectrophoretic trapping and electroporation. Sci Rep 16, 12072 (2026). https://doi.org/10.1038/s41598-026-45747-z
Palabras clave: células tumorales circulantes, electroporación microfluídica, dielectroforesis, diagnóstico del cáncer, lab-on-a-chip